Foram encontradas 36.142 questões.
Leia o texto a seguir para responder à questão:
A cassiterita, a bauxita e a hematita são minérios amplamente
explorados no Brasil, desempenhando um papel fundamental
na economia e na indústria nacional. Na metalurgia extrativa,
tecnologias avançadas são empregadas para transformar
esses minerais em materiais de alto valor, utilizando processos como a redução em altos-fornos, nos quais o coque atua
como agente redutor, e a eletrólise, que emprega coque como
eletrodo, essencial para a obtenção de materiais com elevada
pureza. Dessa forma, a exploração e o processamento desses
recursos garantem o abastecimento da indústria nacional e a
exportação para mercados globais.
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
A cassiterita, a bauxita e a hematita são minérios amplamente
explorados no Brasil, desempenhando um papel fundamental
na economia e na indústria nacional. Na metalurgia extrativa,
tecnologias avançadas são empregadas para transformar
esses minerais em materiais de alto valor, utilizando processos como a redução em altos-fornos, nos quais o coque atua
como agente redutor, e a eletrólise, que emprega coque como
eletrodo, essencial para a obtenção de materiais com elevada
pureza. Dessa forma, a exploração e o processamento desses
recursos garantem o abastecimento da indústria nacional e a
exportação para mercados globais.
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
O cobalto-60 é um radioisótopo muito empregado na área
médica e tecnológica. A sua produção é feita em reator nuclear
a partir do bombardeamento de partículas sobre um alvo constituído cobalto-59 de acordo com a reação nuclear representada na equação a seguir:
\({}^{59}_{27}\text{Co} + x \rightarrow {}^{60}_{27}\text{Co}\)
O cobalto-60 emite radiação gama (γ) de alta energia e decai
para o níquel-60 estável com a emissão de uma partícula radioativa conforme a equação a seguir:
\({}^{59}_{27}\text{Co} \rightarrow {}^{60}_{28}\text{Ni} + w + \gamma\)
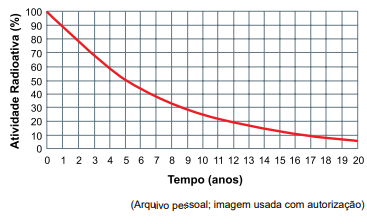
O seguinte gráfico apresenta a curva de decaimento radioativo
de uma fonte radioativa de cobalto-60:
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
O cobalto-60 é um radioisótopo muito empregado na área
médica e tecnológica. A sua produção é feita em reator nuclear
a partir do bombardeamento de partículas sobre um alvo constituído cobalto-59 de acordo com a reação nuclear representada na equação a seguir:
\({}^{59}_{27}\text{Co} + x \rightarrow {}^{60}_{27}\text{Co}\)
O cobalto-60 emite radiação gama (γ) de alta energia e decai
para o níquel-60 estável com a emissão de uma partícula radioativa conforme a equação a seguir:
\({}^{59}_{27}\text{Co} \rightarrow {}^{60}_{28}\text{Ni} + w + \gamma\)
O seguinte gráfico apresenta a curva de decaimento radioativo
de uma fonte radioativa de cobalto-60:

Provas
Questão presente nas seguintes provas
A hidroxiapatita (Ca10(PO4
)
6
(OH)2
) pode ser obtida
por meio da equação não balanceada representada
a seguir:
Ca(NO3 ) 2 (aq) + KH2 PO4 (aq) + NaOH (aq) →
Ca10(PO4 ) (OH)2 (aq) + KNO3 (aq) + NaNO3 (aq) + H2 O(l)
A soma dos coeficientes estequiométricos dos reagentes da equação balanceada que resulta na formação de 1 mol de hidroxiapatita é igual a
Ca(NO3 ) 2 (aq) + KH2 PO4 (aq) + NaOH (aq) →
Ca10(PO4 ) (OH)2 (aq) + KNO3 (aq) + NaNO3 (aq) + H2 O(l)
A soma dos coeficientes estequiométricos dos reagentes da equação balanceada que resulta na formação de 1 mol de hidroxiapatita é igual a
Provas
Questão presente nas seguintes provas
Uma análise química, realizada em uma mufla com
um cadinho aberto, empregou 6,36 g de uma amostra
constituída de uma mistura anidra de óxido de cálcio
(CaO) e carbonato de sódio (Na2
CO3
, massa molar
de 106,0 g/mol). Após aquecimento até 850 ºC, todo o
carbonato de sódio se decompôs, formando óxido de
sódio sólido e dióxido de carbono (CO2
, massa molar de
44 g/mol) gasoso. O óxido de cálcio não reagiu. Após
resfriamento em dessecador, a massa do conteúdo do
cadinho era de 5,04 g.
O percentual de carbonato de sódio na mistura era igual a
O percentual de carbonato de sódio na mistura era igual a
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química InorgânicaSoluções e Substâncias Inorgânicas
Em uma estação de tratamento de água (ETA), diversos
compostos químicos são utilizados para garantir a remoção de impurezas e tornar a água potável.
As funções dos principais produtos químicos empregados em uma ETA nas respectivas etapas são:
• Etapa 1: facilitam a aglutinação das partículas em suspensão, formando flocos maiores, que podem ser removidos na decantação.
• Etapa 2: ajustam o pH da água para otimizar a coagulação e evitar corrosão nas tubulações.
• Etapa 3: eliminam microrganismos patogênicos, tornando a água segura para consumo.
Os reagentes que atendem às funções apresentadas e que podem ser empregados, respectivamente, nas etapas 1, 2 e 3 são:
As funções dos principais produtos químicos empregados em uma ETA nas respectivas etapas são:
• Etapa 1: facilitam a aglutinação das partículas em suspensão, formando flocos maiores, que podem ser removidos na decantação.
• Etapa 2: ajustam o pH da água para otimizar a coagulação e evitar corrosão nas tubulações.
• Etapa 3: eliminam microrganismos patogênicos, tornando a água segura para consumo.
Os reagentes que atendem às funções apresentadas e que podem ser empregados, respectivamente, nas etapas 1, 2 e 3 são:
Provas
Questão presente nas seguintes provas
No esgoto urbano, a decomposição da matéria orgânica
por microrganismos anaeróbios e aeróbios gera diversos
gases. Os principais são os gases numerados a seguir:
1. Produzido por bactérias metanogênicas na digestão anaeróbica da matéria orgânica. É inflamável e contribui para o efeito estufa.
2. Formado pela degradação de compostos sulfurados na ausência de oxigênio. Tem um cheiro forte de ovo podre e é tóxico em altas concentrações.
3. Proveniente da degradação de proteínas e compostos nitrogenados. Tem odor forte e pode ser tóxico em grandes quantidades.
Os gases 1, 2 e 3 são, correta e respectivamente:
1. Produzido por bactérias metanogênicas na digestão anaeróbica da matéria orgânica. É inflamável e contribui para o efeito estufa.
2. Formado pela degradação de compostos sulfurados na ausência de oxigênio. Tem um cheiro forte de ovo podre e é tóxico em altas concentrações.
3. Proveniente da degradação de proteínas e compostos nitrogenados. Tem odor forte e pode ser tóxico em grandes quantidades.
Os gases 1, 2 e 3 são, correta e respectivamente:
Provas
Questão presente nas seguintes provas
Na tabela a seguir, são representadas as equações de reação de quatro sistemas em equilíbrios que ocorrem em sistema fechado em temperatura constante:
| Sistema em Equilíbrio | Equilíbrio Reacional |
|---|---|
| 1 | \(3\text{NO}_2\text{(g)} + \text{H}_2\text{O}(\ell) \rightleftharpoons 2\text{HNO}_3\text{(aq)} + \text{NO(g)}\) |
| 2 | \(2\text{HC}\ell\text{(g)} + \text{I}_2\text{(s)} \rightleftharpoons 2\text{HI(g)} + \text{C}\ell_2\text{(g)}\) |
| 3 | \(2\text{HC}\ell(\ell) \rightleftharpoons \text{H}_2\text{(g)} + \text{C}\ell_2\text{(g)}\) |
| 4 | \(2\text{NO(g)} + \text{O}_2\text{(g)} \rightleftharpoons 2\text{NO}_2\text{(g)}\) |
Com o aumento de pressão, os equilíbrios que são deslocados no sentido da formação dos produtos são os de número
Provas
Questão presente nas seguintes provas
O peróxido de hidrogênio (H2
O2
) reage com o íon iodeto
(I–
) em meio aquoso ácido e forma iodo (I2) e água.
Nessa reação, para cada 2 mol de água formada, a
quantidade de elétrons envolvidos é igual a e o
agente oxidante é o .
As lacunas são preenchidas, correta e respectivamente, por:
As lacunas são preenchidas, correta e respectivamente, por:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container