Foram encontradas 36.142 questões.
As erupções vulcânicas liberam para a atmosfera uma
grande massa de gases que interagem com a atmosfera
de várias formas.
Dentre esses gases, o que provoca a elevação do pH da água da chuva é o gás
Dentre esses gases, o que provoca a elevação do pH da água da chuva é o gás
Provas
Questão presente nas seguintes provas
Um professor de química dispõe de uma solução residual
de uma aula de laboratório que contém uma mistura de
íons cromato e dicromato de potássio. Para recuperar
esse resíduo e reutilizá-lo, o professor deverá cristalizar o
sal na forma de cromato. A equação a seguir representa o
equilíbrio químico que se estabelece entre esses íons em
solução.
2CrO4 2– (aq) + 2H+(aq) ⇄ Cr2 O7 2– (aq) + H2 O(l)
Para que o íon cromato seja o preponderante no sal cristalizado, deve-se adicionar _________à mistura que contém esses dois íons antes da cristalização.
A lacuna é preenchida corretamente por
2CrO4 2– (aq) + 2H+(aq) ⇄ Cr2 O7 2– (aq) + H2 O(l)
Para que o íon cromato seja o preponderante no sal cristalizado, deve-se adicionar _________à mistura que contém esses dois íons antes da cristalização.
A lacuna é preenchida corretamente por
Provas
Questão presente nas seguintes provas
A figura representa uma pilha construída em uma aula de química.
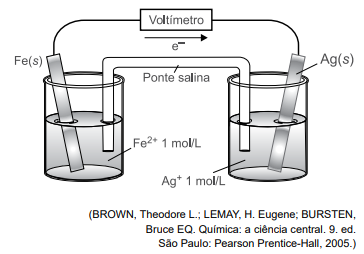
Os potenciais-padrão de redução dos componentes dos eletrodos são:
Fe2+(aq) + 2e– ⟶ Fe(s) Eº = –0,44 V
Ag+(aq) + e– ⟶ Ag(s) Eº = +0,80 V
O polo negativo e o potencial (ddp) dessa pilha são:
Provas
Questão presente nas seguintes provas
A presença de altas concentrações de matéria orgânica
em corpos d’água prejudica a qualidade dos recursos
hídricos, pois em condições de ausência de oxigênio dissolvido pode ocorrer decomposição dessa matéria orgânica, gerando um gás que reduz o pH do meio e provoca
mau cheiro.
Trata-se do gás
Trata-se do gás
Provas
Questão presente nas seguintes provas
Uma solução de ácido clorídrico foi preparada transferindo-se quantitativamente 5 mL de uma solução de HCl
com concentração 0,1 mol/L para um balão volumétrico
de 500 mL, completando-se o volume com água destilada até a marca de aferição de balão.
A 25 ºC, o pH da solução preparada é igual a
A 25 ºC, o pH da solução preparada é igual a
Provas
Questão presente nas seguintes provas
As estações de tratamento de água (ETA) realizam diversos procedimentos que envolvem o emprego de insumos
químicos para que a água seja disponibilizada potável
para o uso da população.
A respeito dos insumos químicos empregados nas estações de tratamento de água, é correto afirmar que o
A respeito dos insumos químicos empregados nas estações de tratamento de água, é correto afirmar que o
Provas
Questão presente nas seguintes provas
Uma reação química, que ocorre em uma única etapa
está representada pela equação a seguir.
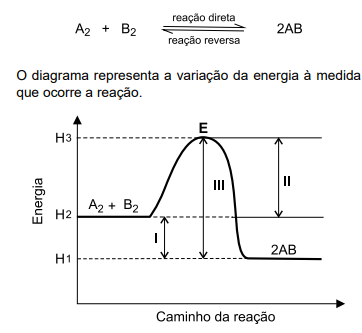
Os valores em módulo das energias representadas por meio das setas I e III são:
I = 40 kJ
III = 90 kJ
O termo referente ao acréscimo de energia representado no diagrama por meio do segmento II e o valor dessa energia são, respectivamente, energia de

Os valores em módulo das energias representadas por meio das setas I e III são:
I = 40 kJ
III = 90 kJ
O termo referente ao acréscimo de energia representado no diagrama por meio do segmento II e o valor dessa energia são, respectivamente, energia de
Provas
Questão presente nas seguintes provas
Uma solução saturada de nitrato de sódio (NaNO3
) foi
preparada usando-se 25g de H2
O a 10ºC. Essa solução
foi transferida quantitativamente para um balão volumétrico de 250mL e, em seguida, adicionou-se água destilada a 20ºC, até atingir o traço de aferição.
O gráfico apresenta a curva de solubilidade do nitrato de sódio.
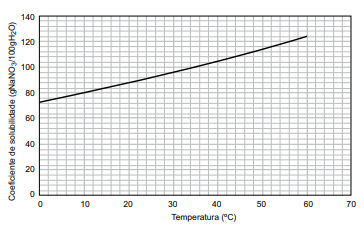
A concentração da solução de nitrato de sódio obtida no balão volumétrico após as operações descritas é igual a
O gráfico apresenta a curva de solubilidade do nitrato de sódio.

A concentração da solução de nitrato de sódio obtida no balão volumétrico após as operações descritas é igual a
Provas
Questão presente nas seguintes provas
As rochas calcáreas contêm alto teor de carbonato de
cálcio (CaCO3
), que é matéria-prima de diversos processos industriais. Sua decomposição térmica dá origem a
dois óxidos, de acordo com a equação.
CaCO3
(s) ⟶ CaO (s) + CO2
(g)
O carbonato de cálcio é também empregado na fabricação do cloreto de cálcio (CaCl2
) por meio da reação com
ácido clorídrico (HCl) com a formação de água e gás carbônico como subprodutos.
Na tabela são fornecidos os valores das entalpias de formação (ΔHºformação) dos compostos que participam das
reações envolvendo o carbonato de cálcio.
| Composto | ΔH0formação (kJ/mol) |
|---|---|
| CaCO3 (s) | -1207 |
| HCl (aq) | -167 |
| CaCl2 (aq) | -796 |
| CO2 (g) | -394 |
| H2O (l) | -286 |
Provas
Questão presente nas seguintes provas
As rochas calcáreas contêm alto teor de carbonato de
cálcio (CaCO3
), que é matéria-prima de diversos processos industriais. Sua decomposição térmica dá origem a
dois óxidos, de acordo com a equação.
CaCO3
(s) ⟶ CaO (s) + CO2
(g)
O carbonato de cálcio é também empregado na fabricação do cloreto de cálcio (CaCl2
) por meio da reação com
ácido clorídrico (HCl) com a formação de água e gás carbônico como subprodutos.
Na tabela são fornecidos os valores das entalpias de formação (ΔHºformação) dos compostos que participam das
reações envolvendo o carbonato de cálcio.
| Composto | ΔH0formação (kJ/mol) |
|---|---|
| CaCO3 (s) | -1207 |
| HCl (aq) | -167 |
| CaCl2 (aq) | -796 |
| CO2 (g) | -394 |
| H2O (l) | -286 |
As lacunas são preenchidas, correta e respectivamente, por
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container