Foram encontradas 36.174 questões.
Provas
Assinale a alternativa correta com base ao texto descrito acima.
Provas
Durante o processo de liofilização em laboratórios farmacêuticos, determinados gases são utilizados para preservar amostras em baixas temperaturas e pressões. Suponha que 2,00 mol de dióxido de carbono (CO₂), comportando-se como gás ideal, se expandam isotermicamente de um volume inicial de 10,0 L para 20,0 L a temperatura constante de 300 K. Qual é a variação de entropia do sistema nessa transformação? Utilize R = 8,0 J·mol⁻¹·K⁻¹ e ln2≈0,693.
Provas
Os diagramas de fases são ferramentas fundamentais para compreender o comportamento de substâncias puras sob diferentes condições de temperatura e pressão. No caso da água, seu diagrama de fases exibe particularidades incomuns, como a inclinação negativa da linha de equilíbrio sólido-líquido, refletindo suas propriedades anômalas. Considerando o diagrama de fases da água (Figura 6), analise o comportamento físico da substância quando a pressão aumenta gradualmente de 100 Torr para 1500 Torr, mantendo a temperatura constante em 90 °C. Assinale a alternativa que descreve corretamente as mudanças de fase e os estados físicos envolvidos nesse processo.
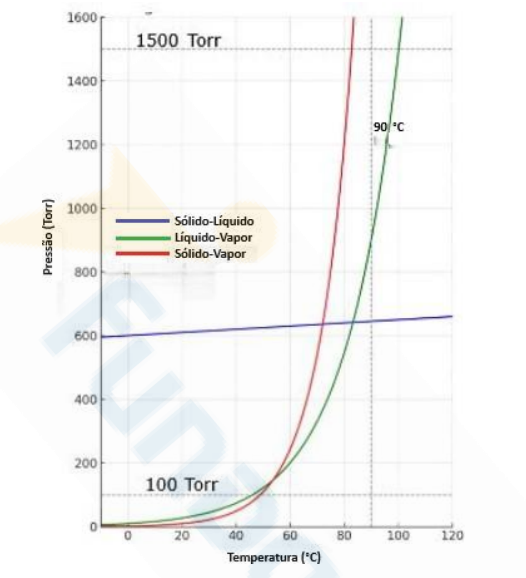
Figura 6 – Diagrama de fase da água
Provas
O ácido salicílico foi originalmente descoberto devido às suas ações antipirética e analgésica, porém, esse ácido tem uma ação corrosiva nas paredes do estômago, limitando o seu uso sistêmico (oral). Para contornar esse problema, em 1897, o químico alemão Felix Hoffmann produziu o ácido acetilsalicílico (AAS) a partir do ácido salicílico, o primeiro fármaco a ser sintetizado em laboratório e comercializado em escala, marcando o nascimento da indústria farmacêutica moderna. Abaixo, são apresentadas as fórmulas do ácido salicílico e do ácido acetilsalicílico:
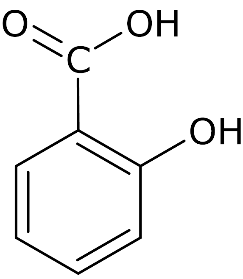
Ácido salicílico
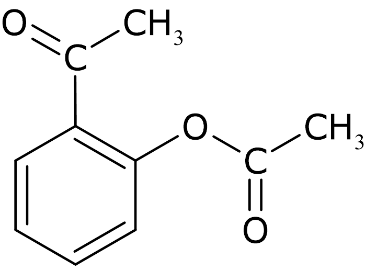
Ácido acetilsalicílico (AAS)
Sobre o tema, analise as assertivas a seguir:
I. O ácido salicílico e o ácido acetilsalicílico apresentam o grupo hidroxila, o que os caracteriza como fenóis.
II. O AAS possui um grupo carboxílico (–COOH) que reage com bases fortes em uma reação de neutralização.
III. No organismo, o ácido acetilsalicílico é convertido em ácido salicílico por uma reação de esterificação.
Quais estão corretas?
Provas
A padronização de uma solução é um procedimento essencial em química analítica para determinar com exatidão a concentração real de um reagente. Muitas soluções não podem ser preparadas com precisão direta, devido a fatores como impurezas, instabilidade ou higroscopicidade dos compostos. Para a padronização de uma solução de ácido sulfúrico, são realizados os seguintes procedimentos:
- Primeira etapa: secar o Na2CO3 em estufa a 110 °C por 24h para eliminar umidade.
- Segunda etapa: pesar 0,25 g do Na2CO3 anidro, transferir para um Erlenmeyer de 250 mL e dissolver em 50 mL de água destilada.
- Terceira etapa: adicionar 3 gotas de indicador alaranjado de metila.
- Quarta etapa: titular com a solução de H2SO4 até a viragem do indicador.
- Quinta etapa: anotar o volume gasto e repetir em triplicata.
Sobre o tema, assinale a alternativa correta.
Provas
O chumbo (Pb2+) é um metal pesado altamente tóxico, mesmo em baixas concentrações, e sua presença em efluentes industriais (baterias, mineração, tintas) exige tratamento rigoroso para atender a limites regulatórios (<0,01 mg·L-1 na água potável, conforme a OMS). A precipitação com sulfeto de sódio é um dos métodos mais eficazes para remover íons chumbo (Pb2+) de efluentes, formando o composto sulfeto de chumbo (PbS), o qual é extremamente insolúvel em água. Para tratar 1.000 L de efluente com 50 mg/L de Pb2+ foram utilizados 15,6 g de sulfeto de sódio. Sobre o procedimento anterior, assinale a alternativa correta.
Provas
O resveratrol é uma fitoalexina presente em uma ampla variedade de espécies vegetais. Em um experimento para determinar o teor de resveratrol em um extrato, utilizando um espectrofotômetro UV-Vis, 1,0 mL da amostra foi colocada num balão volumétrico de 10,0 mL diluída até a marca do balão. A absorbância em 320 nm foi de 0,840 numa cubeta de 1,0 cm de caminho óptico. A absorvidade molar para esse composto em 320 nm é ε = 17.400 L·mol-1cm-1.
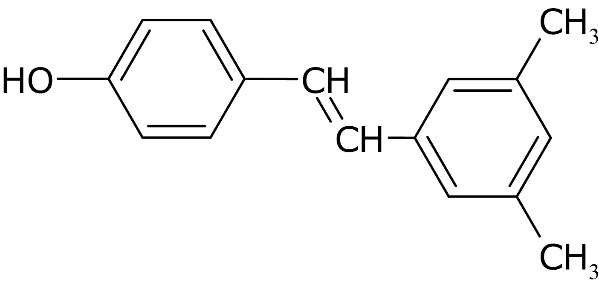
A partir dos dados expostos, nota-se que a ___________ do resveratrol na amostra inicial é de ____________________.
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do trecho acima.
Provas
Provas
Tabela - Valores das Energias de Ionização, Afinidades Eletrônicas e Entalpias
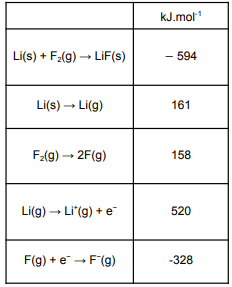
(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010.)
O valor da energia de rede para o fluoreto de lítio em kJ/mol é:
Provas
Caderno Container