Foram encontradas 36.242 questões.
Considere as duas semirreações abaixo:
Zn2+ (aq) + 2e → Zn(s) ; Eº = -0,76 V
AgBr(s) + e → Ag(s) + Br- (aq) ; Eº = +0,07 V
Com base nos seus potenciais padrões de redução, a reação global de oxirredução é
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Química Orgânica
- Transformações Químicas e EnergiaTermoquímica
Um técnico recebeu um frasco contendo um cloreto de
elemento alcalinoterroso (X) de aspecto cristalino e de coloração branca. Ele selecionou uma massa da amostra
para solubilizar completamente em água e, em seguida,
reagir com excesso de carbonato de potássio. O carbonato de X precipitado foi separado, seco e armazenado em
um dessecador.
Uma massa de 1,00 g desse carbonato foi aquecida, produzindo aproximadamente 0,223 g do gás CO2
, conforme
a reação a seguir.
XCO3(s) → XO(s) + CO2(g)
Considerando-se a pureza do carbonato e a sua decomposição assumidamente completa, o elemento X em questão é o
XCO3(s) → XO(s) + CO2(g)
Considerando-se a pureza do carbonato e a sua decomposição assumidamente completa, o elemento X em questão é o
Provas
Questão presente nas seguintes provas
Uma solução aquosa de hidróxido de sódio tem densidade igual a 1,40 g mL-1
e 40% de teor do soluto, em massa.
A concentração, em mol L-1 , do hidróxido na solução é
Dado M(NaOH) = 40 g mol-1
A concentração, em mol L-1 , do hidróxido na solução é
Dado M(NaOH) = 40 g mol-1
Provas
Questão presente nas seguintes provas
A decomposição do carbonato de cálcio produz CO2
,
como representado na reação termoquímica abaixo.
CaCO3(s) → CaO(s) + CO2(g); ΔH0 = +179 kJ
Considerando-se o comportamento ideal do gás e o rendimento máximo da reação, a energia necessária, em MJ, para produzir 36 m3 de CO2 , medido nas condições normais de temperatura e pressão (CNTP) é, aproximadamente,
Dado R × T = 24,4 atm L mol-1 M = 106
CaCO3(s) → CaO(s) + CO2(g); ΔH0 = +179 kJ
Considerando-se o comportamento ideal do gás e o rendimento máximo da reação, a energia necessária, em MJ, para produzir 36 m3 de CO2 , medido nas condições normais de temperatura e pressão (CNTP) é, aproximadamente,
Dado R × T = 24,4 atm L mol-1 M = 106
Provas
Questão presente nas seguintes provas
O dióxido de enxofre é um gás razoavelmente solúvel em
água, sendo usado para a produção industrial de ácido
sulfúrico. Uma matéria prima contendo enxofre elementar sofreu uma reação na presença de excesso de gás
oxigênio, para formar 50.000 L do gás SO2
, medido nas
condições normais de temperatura e pressão (CNTP) e
assumindo comportamento ideal dos gases, como mostrado na reação abaixo.
S(s) + O2(g) → SO2(g)
A reação do enxofre foi completa, e a massa da matéria prima era 80,0 kg.
A partir dessa informação, a percentagem, em massa, de enxofre elementar na matéria prima é, aproximadamente,
Dado R = 0,082 atm L mol-1 K-1
S(s) + O2(g) → SO2(g)
A reação do enxofre foi completa, e a massa da matéria prima era 80,0 kg.
A partir dessa informação, a percentagem, em massa, de enxofre elementar na matéria prima é, aproximadamente,
Dado R = 0,082 atm L mol-1 K-1
Provas
Questão presente nas seguintes provas
O 2-metil-pent-1-eno foi submetido a duas reações distintas. A primeira consistiu na reação desse composto com
KMnO4
em meio básico sob aquecimento, com posterior
acidificação. Na segunda reação, o 2-metil-pent-1-eno
foi submetido à reação com ozônio e posterior adição de
zinco e ácido acético.
Quando se compararam os produtos obtidos em ambas as reações, constatou-se a formação de
Quando se compararam os produtos obtidos em ambas as reações, constatou-se a formação de
Provas
Questão presente nas seguintes provas
No gráfico a seguir, está representada a curva de calibração, com uma solução-padrão de Cu+2, preparada por
uma técnica de espectroscopia de absorção molecular no
ultravioleta e visível.
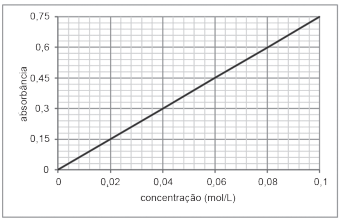
Uma amostra correspondendo a uma solução aquosa contendo Cu+2 passou pelo seguinte procedimento: uma alíquota de 10 mL dessa amostra foi completamente diluída em água até atingir um volume final de solução de 50 mL; uma alíquota dessa solução foi analisada no espectrômetro obtendo-se uma absorbância igual a 0,45.
A concentração de Cu+2 na amostra inicial, em mol L-1 , é

Uma amostra correspondendo a uma solução aquosa contendo Cu+2 passou pelo seguinte procedimento: uma alíquota de 10 mL dessa amostra foi completamente diluída em água até atingir um volume final de solução de 50 mL; uma alíquota dessa solução foi analisada no espectrômetro obtendo-se uma absorbância igual a 0,45.
A concentração de Cu+2 na amostra inicial, em mol L-1 , é
Provas
Questão presente nas seguintes provas
O cloro é um elemento químico que forma diferentes
ácidos.
Dentre os ácidos formados pelo cloro, aquele que apresenta o menor grau de ionização corresponde ao
Dentre os ácidos formados pelo cloro, aquele que apresenta o menor grau de ionização corresponde ao
Provas
Questão presente nas seguintes provas
Os métodos eletroquímicos que se baseiam na eletrólise
realizada em tempo suficiente para a oxidação ou redução do analito, para um produto de composição conhecida, são a
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em uma análise por espectroscopia de absorção molecular no ultravioleta e visível, a concentração do analito é
0,2 g L-1
, o caminho óptico é 1,0 cm, e a absorbância
determinada é 0,26.
Nessa análise, a absortividade do analito, em L g-1 cm-1 , é
Nessa análise, a absortividade do analito, em L g-1 cm-1 , é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container