Foram encontradas 35.934 questões.
Para um determinado experimento, o técnico em química deverá preparar 100 mL de solução de sacarose 0,02 mol/L seguindo
os seguintes procedimentos:
• Determinar a massa de sacarose a ser pesada;
• Pesar a quantidade calculada em um béquer de 50 mL;
• Adicionar, aproximadamente, 20 mL de água destilada ao béquer contendo a sacarose e dissolver o sólido com o auxílio de um bastão de vidro;
• Transferir essa solução para um balão volumétrico de 100 mL “quantitativamente”;
• Efetuar, pelo menos, 3 lavagens do béquer e do bastão de vidro com, no máximo, 20 mL de água destilada em cada lavagem, transferindo sempre para o balão volumétrico;
• Completar o volume do balão volumétrico com água destilada até o traço de aferição; e
• Agitar o balão volumétrico para homogeneizar a solução.
(Dados: MM sacarose: 342 g/mol.)
Qual a massa de sacarose a ser pesada para o preparo da solução?
• Determinar a massa de sacarose a ser pesada;
• Pesar a quantidade calculada em um béquer de 50 mL;
• Adicionar, aproximadamente, 20 mL de água destilada ao béquer contendo a sacarose e dissolver o sólido com o auxílio de um bastão de vidro;
• Transferir essa solução para um balão volumétrico de 100 mL “quantitativamente”;
• Efetuar, pelo menos, 3 lavagens do béquer e do bastão de vidro com, no máximo, 20 mL de água destilada em cada lavagem, transferindo sempre para o balão volumétrico;
• Completar o volume do balão volumétrico com água destilada até o traço de aferição; e
• Agitar o balão volumétrico para homogeneizar a solução.
(Dados: MM sacarose: 342 g/mol.)
Qual a massa de sacarose a ser pesada para o preparo da solução?
Provas
Questão presente nas seguintes provas
O técnico em química precisa determinar a concentração de cálcio em uma amostra de 200 mL de uma água natural. Para tal
análise, ele utilizou o método da gravimetria por precipitação seguindo os seguintes passos:
1. Adicionou a solução contendo amostra excesso de ácido oxálico;
2. Adicionou, também, amônia para neutralizar o ácido e provocar a precipitação completa do cálcio;
3. O precipitado formado foi filtrado, utilizando um cadinho de filtração que ele encontrou sobre a bancada do laboratório;
4.O precipitado filtrado foi seco e calcinado; e
5. Após o resfriamento, o precipitado juntamente ao cadinho de filtração foi pesado e a massa de óxido de cálcio encontrada.
Após seguir cada passo para determinar a concentração de cálcio em determinada amostra, o técnico em química cometeu quantos erros?
1. Adicionou a solução contendo amostra excesso de ácido oxálico;
2. Adicionou, também, amônia para neutralizar o ácido e provocar a precipitação completa do cálcio;
3. O precipitado formado foi filtrado, utilizando um cadinho de filtração que ele encontrou sobre a bancada do laboratório;
4.O precipitado filtrado foi seco e calcinado; e
5. Após o resfriamento, o precipitado juntamente ao cadinho de filtração foi pesado e a massa de óxido de cálcio encontrada.
Após seguir cada passo para determinar a concentração de cálcio em determinada amostra, o técnico em química cometeu quantos erros?
Provas
Questão presente nas seguintes provas
Para avaliar a qualidade da água para consumo humano, um dos parâmetros monitorados é o teor de cloreto. Em um laboratório
de análises, o químico precisava determinar esse teor de cloreto por titulação com uma solução padrão de AgNO3. Para isso, o
profissional prosseguiu com a análise através dos procedimentos descritos a seguir:
1. Com uma pipeta de 50 mL, pipete esse volume de NaCl;
2. Transfira esse volume de NaCl para um erlenmeyer de 50 mL;
3. Titule lentamente com a solução padronizada de AgNO3 0,05 mol/L até que mude a cor de forma permanente; e
4. Anote o volume consumido de AgNO3. (Observação: volume gasto de AgNO3 na titulação: 1 mL.)
A partir da realização de todas as etapas e das observações experimentais, analise as afirmativas a seguir.
I. O teor de cloreto é 0,001 mol/L.
II. A equação da reação envolvida é Cl(aq)- + AgNO3(aq) → AgCl(s) + NO3 - (aq)
III. A quantidade de matéria, em mol, de nitrato de prata presente no volume consumido no processo é 0,05 mol.
Está correto o que se afirma em
1. Com uma pipeta de 50 mL, pipete esse volume de NaCl;
2. Transfira esse volume de NaCl para um erlenmeyer de 50 mL;
3. Titule lentamente com a solução padronizada de AgNO3 0,05 mol/L até que mude a cor de forma permanente; e
4. Anote o volume consumido de AgNO3. (Observação: volume gasto de AgNO3 na titulação: 1 mL.)
A partir da realização de todas as etapas e das observações experimentais, analise as afirmativas a seguir.
I. O teor de cloreto é 0,001 mol/L.
II. A equação da reação envolvida é Cl(aq)- + AgNO3(aq) → AgCl(s) + NO3 - (aq)
III. A quantidade de matéria, em mol, de nitrato de prata presente no volume consumido no processo é 0,05 mol.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A identificação de determinado grupo funcional é feita com o reagente de Jones, que consiste em uma solução de ácido
crômico e ácido sulfúrico. O ácido ascórbico, que é um álcool, é oxidado pelo reagente de Jones, resultando em uma mudança
de sua estrutura química. O teste de Jones com o ácido ascórbico é representado pela equação a seguir; analise-a.
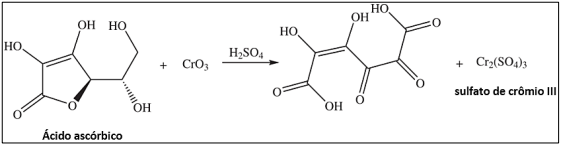
Considerando que uma massa de 200 g de ácido ascórbico (80% de pureza) sofre oxidação, qual a massa, em gramas, de sulfato de crômio III- Cr2(SO4)3 obtido?
(Considere a estequiometria da reação 1:1 / Dados: MM ácido ascórbico = 176 g/mol.)

Considerando que uma massa de 200 g de ácido ascórbico (80% de pureza) sofre oxidação, qual a massa, em gramas, de sulfato de crômio III- Cr2(SO4)3 obtido?
(Considere a estequiometria da reação 1:1 / Dados: MM ácido ascórbico = 176 g/mol.)
Provas
Questão presente nas seguintes provas
O manuseio e a conservação de reagentes químicos
exigem conhecimento sobre suas propriedades e
incompatibilidades para prevenir acidentes. Um técnico
precisa descartar um resíduo de ácido nítrico
concentrado (HNO3) e, separadamente, um resíduo de
acetona (CH3COCH3). Assinale a alternativa que
descreve a prática correta e segura para o manuseio e
descarte desses reagentes.
Provas
Questão presente nas seguintes provas
O modelo atômico atual, baseado na mecânica quântica,
descreve a distribuição dos elétrons em termos de
orbitais e números quânticos, superando as limitações do
modelo de Bohr. A combinação dos quatro números
quânticos define unicamente o estado de um elétron em
um átomo. Com base na distribuição eletrônica do íon Fe
3+(Z=26) em seu estado fundamental, assinale a
alternativa correta.
Provas
Questão presente nas seguintes provas
O gerenciamento de resíduos químicos, incluindo seu
armazenamento temporário e descarte final, é uma etapa
crítica da segurança e da gestão ambiental em um
laboratório. O conhecimento sobre a classificação e a
incompatibilidade química é fundamental. Assim, analise
as afirmativas a seguir.
I.Resíduos de ácidos fortes, como o ácido nítrico, e bases fortes, como o hidróxido de sódio, devem ser armazenados em recipientes separados e nunca misturados diretamente sem um procedimento de neutralização prévio, devido à reação de neutralização ser altamente exotérmica e potencialmente perigosa.
II.Solventes orgânicos halogenados (ex: clorofórmio) e não halogenados (ex: hexano) podem ser descartados no mesmo recipiente de resíduo, pois ambos são inflamáveis e o tratamento por incineração é o mesmo para ambos.
III.Pequenas quantidades de soluções aquosas contendo metais pesados, como sais de chumbo ou mercúrio, podem ser descartadas na pia com água corrente abundante, pois a diluição é um método de tratamento aceito pela legislação para reduzir a toxicidade a níveis seguros.
Está correto o que se afirma em:
I.Resíduos de ácidos fortes, como o ácido nítrico, e bases fortes, como o hidróxido de sódio, devem ser armazenados em recipientes separados e nunca misturados diretamente sem um procedimento de neutralização prévio, devido à reação de neutralização ser altamente exotérmica e potencialmente perigosa.
II.Solventes orgânicos halogenados (ex: clorofórmio) e não halogenados (ex: hexano) podem ser descartados no mesmo recipiente de resíduo, pois ambos são inflamáveis e o tratamento por incineração é o mesmo para ambos.
III.Pequenas quantidades de soluções aquosas contendo metais pesados, como sais de chumbo ou mercúrio, podem ser descartadas na pia com água corrente abundante, pois a diluição é um método de tratamento aceito pela legislação para reduzir a toxicidade a níveis seguros.
Está correto o que se afirma em:
Provas
Questão presente nas seguintes provas
Um Técnico de Laboratório recebe uma amostra de
efluente industrial desconhecido e é incumbido de
realizar uma análise completa. Na primeira etapa, ele
realiza testes de chama e reações de precipitação com
diferentes reagentes para identificar a presença ou
ausência de certos íons metálicos, como Cu2+, Pb2+ e Fe
3+ . Na segunda etapa, após identificar a presença de
cobre, ele utiliza a espectrofotometria de absorção
atômica para determinar a concentração exata de Cu2+
em mg/L. Considerando os princípios da Química
Analítica, as duas etapas do trabalho do técnico
correspondem, respectivamente, a quais tipos de
análise?
Provas
Questão presente nas seguintes provas
A isomeria é o fenômeno no qual compostos diferentes
apresentam a mesma fórmula molecular. A distinção
entre isômeros muitas vezes requer o uso de técnicas de
análise instrumental. Um técnico dispõe de duas
amostras puras, uma de propanal (um aldeído) e outra
de propanona (uma cetona), que são isômeros de função
com a fórmula C3H6O. Assinale a alternativa que
descreve uma técnica instrumental e o resultado
esperado que permitiria distinguir inequivocamente as
duas substâncias.
Provas
Questão presente nas seguintes provas
A separação de misturas é uma operação fundamental
em laboratório, e a escolha da técnica adequada
depende das propriedades físicas dos componentes.
Acerca dos princípios e aplicações de diferentes
métodos de separação, registre V, para as afirmativas
verdadeiras, e F, para as falsas:
(__)A destilação simples é o método de escolha para separar dois líquidos miscíveis com pontos de ebulição muito próximos, como o hexano (P.E. 69 °C) e o tolueno (P.E. 111 °C).
(__)A extração líquido-líquido, realizada em um funil de separação, é baseada na diferença de solubilidade de um soluto em dois solventes imiscíveis, permitindo a transferência seletiva do soluto de uma fase para outra.
(__)A decantação é um método eficiente para separar uma mistura heterogênea de um sólido finamente dividido e um líquido, como a argila em água, pois a sedimentação rápida garante a remoção completa do sólido.
(__)A filtração a vácuo, utilizando um funil de Büchner e um kitassato, é uma técnica utilizada para acelerar a separação de um sólido precipitado de uma fase líquida, sendo mais rápida e eficiente que a filtração simples por gravidade.
Após análise, assinale a alternativa que apresenta a sequência correta dos itens acima, de cima para baixo:
(__)A destilação simples é o método de escolha para separar dois líquidos miscíveis com pontos de ebulição muito próximos, como o hexano (P.E. 69 °C) e o tolueno (P.E. 111 °C).
(__)A extração líquido-líquido, realizada em um funil de separação, é baseada na diferença de solubilidade de um soluto em dois solventes imiscíveis, permitindo a transferência seletiva do soluto de uma fase para outra.
(__)A decantação é um método eficiente para separar uma mistura heterogênea de um sólido finamente dividido e um líquido, como a argila em água, pois a sedimentação rápida garante a remoção completa do sólido.
(__)A filtração a vácuo, utilizando um funil de Büchner e um kitassato, é uma técnica utilizada para acelerar a separação de um sólido precipitado de uma fase líquida, sendo mais rápida e eficiente que a filtração simples por gravidade.
Após análise, assinale a alternativa que apresenta a sequência correta dos itens acima, de cima para baixo:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container