Foram encontradas 36.167 questões.
Águas minerais sulfurosas contêm sais de:
Provas
Em um laboratório de análises clínicas, é necessário o preparo de 300mL de solução de NaCl 0,1mol/L. O volume em mililitros a ser utilizado de uma solução disponível e rotulada de NaCl 0,4mol/L é igual a:
Peso molecular NaCl = 58,44g/mol
Provas
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaMateriais homogêneos e heterogêneos. Separação de misturas.
Leia atentamente o trecho da reportagem abaixo:
“Cachaça é a denominação típica e exclusiva da aguardente de cana produzida no Brasil, com graduação alcoólica de 38% a 48%, obtida através de um conhecido processo de separação de mistura do mosto fermentado do caldo de cana-de-açúcar, com características sensoriais peculiares.”
(Fonte disponível em https://www.dinheirorural.com.br/a-nova-bebida-dos-deuses/ - 03/10/2022)
O conhecido processo de separação de mistura citado no texto é denominado:
Provas
Uma das maiores descobertas científicas da história foi a da estrutura do átomo. Ernest Rutherford, Niels Bohr e Max Planck foram alguns dos cientistas responsáveis pelos primeiros passos no sentido de entender a estrutura daquilo que seria a base para o desenvolvimento científico posterior. Bohr expôs suas ideias em quatro postulados que, apesar de aplicáveis ao átomo de hidrogênio, podem ser transpostos a outros átomos também. Um desses postulados está corretamente enunciado em:
Provas
Em uma aula de eletroquímica, o professor construiu uma pilha usando os metais níquel e ferro e soluções 1,0 mol/L de sais de seus cátions. A figura representa um esquema da pilha.
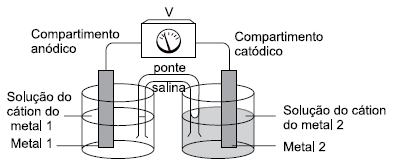
São dados os potenciais padrão de redução dos metais.
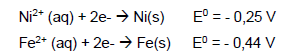
Em relação a essa pilha, é correto afirmar que durante seu funcionamento a 25oC forma-se
Provas
Uma solução aquosa de ácido sulfúrico H2SO4 foi preparada com procedimento quantitativo, a partir da diluição de 10,0 mL de ácido sulfúrico concentrado (98% em massa e densidade 1,84g/cm3) em certo volume de água destilada. Após atingir a temperatura ambiente, a solução diluída foi transferida quantitativamente para um balão volumétrico de 500 mL e em seguida completou-se o volume com água destilada até o traço de aferição do balão.
A concentração da solução no balão volumétrico é igual a, aproximadamente:
Provas
A reação de obtenção do cobre metálico pode ser realizada com o aquecimento do óxido de cobre(II) em presença de gás hidrogênio, a 400 ºC, em um sistema fechado. A equação que representa o equilíbrio dessa reação é dada a seguir.
![]()
A expressão da constante de equilíbrio, Kc, dessa reação a 400 ºC, é:
Provas
O composto orgânico de fórmula molecular C6H12O2. empregado na indústria de alimentos é obtido, em condições adequadas, por meio de uma reação representada na seguinte equação.
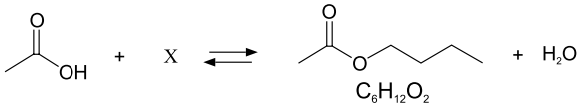
O reagente X é um composto orgânico que, ao ser aquecido na presença de ácidos fortes, sofre desidratação intermolecular, representada por
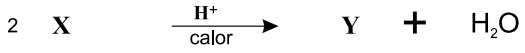
Provas
Foram feitos três experimentos para o estudo cinético da reação entre os gases monóxido de nitrogênio e hidrogênio que ocorre de acordo com a reação a seguir.
2NO (g) + 2 H2 (g) → N2 (g) + 2H2 O (g)
A evolução da reação foi monitorada por técnica experimental medindo-se a formação dos produtos.
A tabela apresenta as concentrações dos reagentes e as velocidades iniciais das reações, para os três experimentos.
Experimento | [NO] (mol.L–1) | [H2] (mol.L–1) | Velocidade inicial (mol.L–1.s–1) |
1 | 5 × 10–3 | 2 × 10–3 | 1,25 × 10–5 |
2 | 10 × 10–3 | 2 × 10–3 | 5 × 10–5 |
3 | 10 × 10–3 | 1 × 10–3 | 2,5 × 10–5 |
A ordem global dessa reação e as unidades de sua constante de velocidade são, correta e respectivamente:
Provas
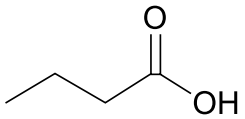
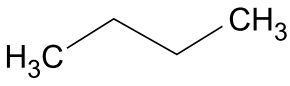
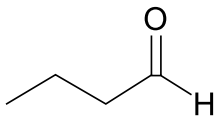
Considere as substâncias I, II, III e IV, cujas fórmulas estruturais estão representadas na tabela.
Substância | Fórmula estrutural |
I |
|
II |
|
III |
|
IV |
|
As substâncias do quadro que formarão interações intermoleculares do tipo ligação de hidrogênio com a água são as de números
Provas
Caderno Container