Foram encontradas 36.167 questões.
A tabela a seguir apresenta algumas informações a respeito de alguns ácidos graxos.
| Grupo | Nome sistemático |
Fórmula molecular |
| I |
Ácido n-dodecanoico Ácido n-hexadecanóico |
!$ CH_3(CH_2)_{10} COOH !$ !$ CH_3(CH_2)_{14}COOH !$ |
| II |
Ácido n-octadecanóico Ácido cis-9-octadecanóico |
!$ CH_3(CH_2)_{16}COOH !$ !$ CH_3(CH_2)_7CH = CH(CH_2)_7COOH !$ |
| III |
Ácido trans-9-octadecanóico Ácido cis-9-octadecanóico |
!$ CH_3(CH_2)_7CH = CH(CH_2)_7 COOH !$ !$ CH_3(CH_2)_7 CH(CH_2)_7 COOH !$ |
Dentro de cada grupo, I, II e III, os ácidos graxos que apresentam os pontos de fusão mais altos são, correta e respectivamente:
Provas
Na figura, é apresentada a fórmula de Haworth para a forma hemiacetálica cíclica de um monossacarídeo.
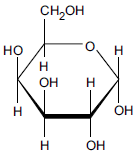
Trata-se de uma e a conformação do átomo de carbono anomérico é . Em relação à sua estrutura de cadeia aberta, a ciclização ocorreu entre os átomos de carbono de números .
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do texto.
Provas
Uma mistura de fenilamina, a anilina, C6H7N, e fenilmetanol, o álcool benzílico, C7H8O, foi submetida a um procedimento para separação, conforme representado no esquema da figura a seguir.
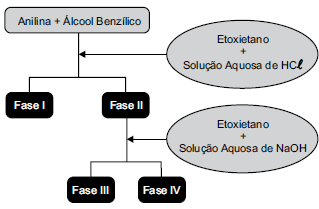
O álcool benzílico e um sal de amina estão presentes, preponderante e respectivamente, nas fases
Provas
O composto orgânico oxigenado, X, reage, em condições adequadas, de acordo com as equações de reação representadas a seguir.
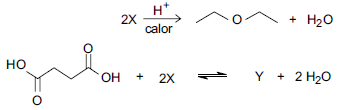
O composto Y tem a seguinte fórmula molecular:
Provas
Foi adicionada a uma bomba calorimétrica selada, com volume invariável a 25 ºC, uma mistura gasosa de um hidrocarboneto saturado e oxigênio, com pressão total P1, em proporção estequiométrica para reação de combustão completa. Após acionada a ignição, a mistura gasosa reagiu completamente.
Considerando que o volume do líquido formado na reação é desprezível em relação ao volume total do compartimento e que a pressão P2 no interior da bomba calorimétrica após a reação 25 ºC é igual a 0,5 x P1, a fórmula molecular do hidrocarboneto empregado no experimento é:
Provas
Foram misturados sob agitação Ag2S sólido e uma solução de saturada de H2S (0,1 mol/L) em H+ (0,15 mol/L).
Considerem-se as constantes de equilíbrio a 25 ºC:
!$ K = { \large [S^{2-}] x [H_3O^+]^2 \over [H_2 S]} = 1x 10^{21} !$
e !$ Kps = [Ag^+]^2 x [S^{2-}]=5 x 10^{51} !$
Nessa temperatura, ao se atingir o equilíbrio, a concentração de íons Ag+ na solução será:
Provas
Um procedimento para obtenção de estanho metálico foi realizado a partir do óxido de estanho (IV), em um compartimento selado que, após ser evacuado, foi preenchido com gás hidrogênio. Ao ser atingido o equilíbrio químico a 900 K, a atmosfera gasosa no interior do compartimento era composta por 45% gás hidrogênio, em volume. A constante de equilíbrio, Kp, para essa reação a 900 K é igual a, aproximadamente,
Provas
Os dados do estudo cinético de uma reação representada por
!$ 2\,\,A \rightarrow 2B + 3C !$
possibilitaram construção de uma curva de rapidez da reação, representada na figura a seguir.
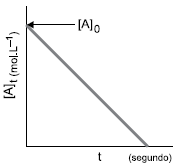
(P. Atkins; L. Jones; Princípios de Química: questionando a vida moderna e o meio ambiente. 5a ed. Trad. Ricardo Bicca de Alencastro. Porto Alegre: Bookman, 2012. Adaptado)
A ordem dessa reação e as unidades de sua constante de velocidade são:
Provas
Considere as seguintes representações de equações de reação:
I. !$ A(g) + B(g) \rightarrow AB(s)\,\,\,\,\triangle H^{ \circ} > 0 !$
II.!$ C ( \ell) + D (s) \rightarrow CD(g)\,\,\,\,\,\,\triangle H^{ \circ} > 0 !$
A respeito da espontaneidade dessas reações, é correto afirmar que
Provas
A reação da amônia com oxigênio pode ocorrer sob condições adequadas, de acordo com a equação a seguir.
Equação 1
!$ 2\,\,NH_3(g) + 3/2 O_2(g) \rightarrow N_2(g) + 3 H_2O(g) !$
Considere as seguintes equações termoquímicas envolvendo a amônia:
!$ 2\,\,NH_3(g) + 7/2 O_2(g) \rightarrow 2\,NO_2(g) + 3 H_2 O(g)\,\,\triangle H^{ \circ} = - 566\,KJ\\3\,\,NO_2(g) + 4\,NH_3(g) \rightarrow 7/2 N_2(g) + 6 H_2 O(g)\,\,\,\triangle H^{ \circ} = - 1370 KJ !$
A entalpia da reação da combustão de um mol de amônia representada na equação 1 é igual a, aproximadamente:
Provas
Caderno Container