Foram encontradas 35.936 questões.
Os experimentos apresentados abaixo, para a reação redox entre permanganato e oxalato de potássio em meio de ácido sulfúrico, apresentaram diferentes resultados; vide quadro 1.
|
QUADRO 1 |
|
|
Resultados experimentais, para cada uma das reações levadas a termo |
|
| I |
T= 10 ºC, resfriamento prévio, mais excesso de MnO4- ; não reage |
| II |
T= 25 ºC, aquecimento prévio, sem excesso de MnO4-; não reage |
| III |
T= 60 ºC, aquecimento prévio, mais excesso de MnO4-; reage |
| IV |
T= 90 ºC, aquecimento prévio, mais excesso de MnO4-; não reage (C2O4-2 decompõe a 90 ºC) |
Os potenciais padrões para as semirreações são dados a seguir: Eº MnO4-/Mn2+= 1,51 V e Eº H2C2O4/CO2= -0,46 V; e a equação para o cálculo do ΔG = -nFΔE.
Reação a ser avaliada, frente às diferentes condições experimentais, é apresentada abaixo, já balanceada:
2 MnO4- + 5 C2O4-2 + 16 H+ !$ \leftrightarrows !$ 2 Mn2+ + 10 CO2 + 8 H2O – (conduzida em meio fortemente ácido de H2SO4 2 mol L-1)
A partir das considerações e condições experimentais apresentadas anteriormente, para a realização das reações de I a IV, é correto afirmar que a condição efetiva é devida ao fato da reação redox
Provas
Leia o texto para responder a questão.
Uma solução aquosa de hidróxido de rubídio (RbOH) de concentração expressa em molar (mol L-1) foi preparada e necessitou ser quantificada. Para a quantificação da base, um analista titulou uma massa do padrão primário hidrogenoftalato de potássio (HF K; MM= 200 g mol-1) usando como indicador a fenolftaleína.
De acordo com o texto e os dados fornecidos a seguir, obtidos da titulação, é correto afirmar que a concentração analítica do RbOH, expresso em mol L-1, é
Dados: número de mol do HFKusado na titulação = 1,05x10-4 mol; Vgasto na titulação = 9,95 mL
Provas
Os experimentos realizados com tubos de raios catódicos permitiram evidenciar que os átomos contêm partículas subatômicas com cargas negativas ou elétrons e permitiu a um determinado cientista, à época, a proposição de que tais partículas encontravam-se dispersas em meio as cargas positivas. De posse do texto anterior é correto afirmar que o propositor de tal modelo atômico foi
Provas
O ácido acético (CH3COOH) é um ácido orgânico fraco (Ki~ 1,79 x 10-5) a 35 ºC. Este ácido, em sendo diluído em água, à mesma temperatura, permite a intensificação do brilho do filamento de uma lâmpada incandescente. O contato elétrico da lâmpada à solução aquosa, para permitir a passagem de corrente elétrica pelo sistema, é feito a partir de eletrodos de cobre, previamente conectados à energia elétrica (E= 220 V / 50 Hz). Assim, de acordo com o explanado, é correto afirmar que a quantidade relativa das espécies CH3COO- e H+ do ácido (expressa em %) em solução aumenta com o favorecimento da
Provas
A detecção de ácido acetilsalicílico (AAS) em fármacos é realizada a partir da reação de Trinder, em que íons Fe3+ formam um complexo violeta em presença de íons salicilato, derivados do AAS. A fórmula do AAS e a reação de formação do complexo salicilato-Fe(III) estão mostradas a seguir.
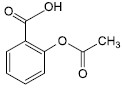
ácido acetilsalicílico (AAS)
Formação do complexo salicilato-Fe(III) de cor violeta
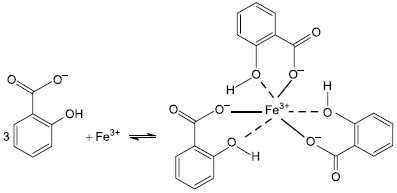
(qnesc.sbq.org.br)
Em uma determinação de AAS presente em um fármaco, verificou-se que 50 mL de uma solução de íons salicilato consumiram 5,6 mg de íons Fe3+. O nome da reação química responsável pela formação do íon salicilato a partir do AAS e a concentração de íons salicilato, em mol/L, na solução analisada são
Provas
Ensaios de corrosão atmosférica consistem em submeter diferentes materiais a vapores e a gases constituintes do ar atmosférico, em câmaras fechadas, com o objetivo de avaliar a resistência desses materiais à corrosão. Em quatro tubos de ensaio, 1, 2, 3 e 4, com tampa, peças de níquel (Ni), zinco (Zn), aço galvanizado (liga de ferro – Fe – revestida com zinco) e cobre (Cu) foram submetidas, separadamente, a uma atmosfera contendo vapor d’água e os gases oxigênio (O2), nitrogênio (N2) e dióxido de enxofre (SO2), conforme as figuras.
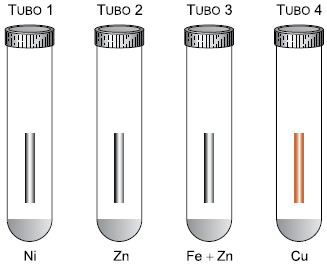
A tabela apresenta os potenciais de redução de algumas espécies químicas envolvidas nesse ensaio.
|
Equação |
Potencial padrão de redução (V) |
|
Zn2+ + 2e– → Zn |
- 0,76 |
|
Fe2+ + 2e– → Fe |
- 0,44 |
|
Ni2+ + 2e– → Ni |
- 0,23 |
|
2H+ + 2e– → H2 |
0,00 |
|
Cu2+ + 2e– → Cu |
+0,34 |
|
2H+ + !$ large{1 over 2} !$O2 + 2e– → H2O |
+1,23 |
Considerando que o SO2 gasoso reage com o vapor d’água da atmosfera do tubo produzindo quantidades adequadas de íons H+ (aq), nas condições padrão, ao final desse ensaio ocorrerá corrosão
Provas
O estudo da cinética de uma reação química elementar de ordem global igual a 3 mostrou que a velocidade da reação aumenta 4 vezes quando a concentração de um dos reagentes é dobrada. A equação balanceada dessa reação é:
Provas
O interior de submarinos é um ambiente hermético. Quando tripulado, a renovação do ar nesse ambiente ocorre pela reação entre o gás carbônico (CO2) exalado pelos tripulantes e o superóxido de potássio (KO2). Essa reação, além de remover o gás carbônico do ar, produz carbonato de potássio (K2CO3) e gás oxigênio (O2), que é liberado para o ambiente e utilizado na respiração. Considere que um tripulante de um submarino libere um volume de gás carbônico igual a 625 L por dia, e que o volume molar dos gases nas condições da atmosfera de um submarino seja igual a 25 L/mol. A massa de superóxido de potássio necessária para consumir totalmente o gás carbônico diário desse tripulante, considerando a reação com rendimento de 100%, é igual a
Provas
Uma situação inusitada ocorreu com uma atleta japonesa que ganhou uma medalha de ouro nas Olimpíadas de Tóquio: sua medalha teve de ser trocada por uma nova. O motivo foi o fato de o prefeito de sua cidade ter mordido a medalha em uma cerimônia, uma atitude considerada desrespeitosa e anti-higiênica. A prática de morder peças de ouro vem da Idade Média, quando comerciantes utilizavam esse recurso para verificar se as moedas dadas como pagamento eram de ouro puro, já que ele é bastante , deixando uma marca. No entanto, a confirmação da composição de materiais deve ser comprovada por outras propriedades específicas dos materiais, como a .
As lacunas do texto são respectivamente preenchidas por
Provas
Os vegetais são a base da cadeia alimentar; sem eles a vida no planeta Terra estaria destinada à extinção. Porque os vegetais são autotróficos capazes de captar CO2 gasoso e fixá-lo na forma de matéria orgânica, como demonstrado na equação geral a seguir:
6 CO2 + 12 H2O ![]() C6H1206 + 6 O2 +6 H20
C6H1206 + 6 O2 +6 H20
A esse respeito, é correto afirmar que a reação demonstrada constitui uma reação de fotossíntese que se caracteriza por
Provas
Caderno Container