Foram encontradas 35.936 questões.
No nosso dia a dia estamos o tempo todo fazendo uso ou mesmo preparando soluções. Soluções são preparadas com um solvente e um soluto e, quando o solvente é a água, chamamos de solvente aquoso.
A sequência que apresenta corretamente os exemplos de soluções presentes no nosso cotidiano está indicada em
Provas
Avalie o que se afirma sobre os métodos oficiais de análise de alimentos de origem animal.
I - A análise de desglaciamento é realizada em leite e produtos lácteos.
II - Mel e produtos apícolas são avaliados quanto ao ponto de saponificação turva.
III - A avaliação do pH é um método oficial para a avaliação de todos os produtos de origem animal.
IV - A determinação de colágeno é um método químico empregado na avaliação de carnes e de produtos cárneos.
V - A avaliação do número mais provável de Vibrio parahaemolyticus é realizada em amostras de ovos e derivados.
VI - A contagem de coliformes termotolerantes e coliformes totais em alimentos deve ser utilizada quando o limite máximo tolerado for igual ou superior a 100UFC/g ou mL.
Está correto apenas o que se afirma em
Provas
O texto seguinte servirá de base para responder às questões de 1 a 2.
Tabela periódica
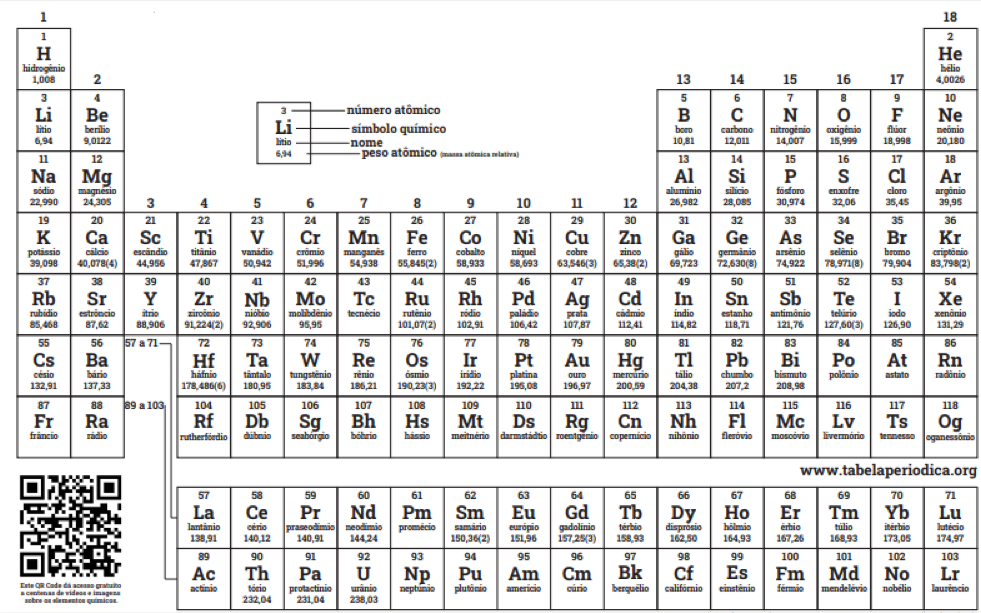
Licença de uso Creative Commons BY-NC-SA 4.0 - Use somente para fins educacionais Caso encontre algum erro favor avisar pelo mail luisbrudna@gmail.com Versão IUPAC/SBQ (pt-br) com 5 algarismos significativos, baseada em DOI:10.1515/pac-2015-0305 - atualizada em 23 de fevereiro de 2022
Sabendo-se que o elemento químico é o conjunto formado por átomos de mesmo número atômico (Z) e que o número de massa (A) de um elemento é a soma do número de prótons com o número de nêutrons presentes no núcleo de um átomo. Dessa forma, sobre o elemento sódio (Na), marque a alternativa INCORRETA.
Provas
Sobre o átomo e a estrutura atômica, pode-se afirmar que:
Provas
O estudo cinético das reações químicas tem grande impacto nas aplicações do cotidiano e na indústria. A rapidez de uma reação química pode ser influenciada por diversos fatores, tais quais o uso de catalisadores, a concentração das substâncias, a superfície de contato e a temperatura.
Porém, muitas ideias são manifestadas pelos estudantes, diferentes das concepções científicas (MALDANER, 2013).
Com relação à explicação dada pelos estudantes aos fatores que influenciam a rapidez de uma reação química, uma dessas ideias não-científicas seria:
Provas
Sabe-se que a acidez dos compostos orgânicos não é tão acentuada quanto nas substâncias inorgânicas. Por exemplo, enquanto ácidos como HCl podem chegar a valor extremo de pH igual a 2, os ácidos orgânicos mantêm-se em acidez bem mais leve (alguns em torno de 5 e 6). Os principais ácidos orgânicos são as cadeias que possuem o radical carboxila (-COOH). Alguns grupos químicos que interagem com carboxila (ligados a ela, ou próximas) podem interferir na acidez desses compostos. Observe as estruturas químicas abaixo, nas mesmas condições gerais, e marque a opção que apresenta o ácido mais forte.
Provas
Se uma corrente de 0,5 ampères fluir por um fio metálico por 2 horas, quantos elétrons fluirão através do fio?
Provas
Na reação do zinco com ácidos, ocorre liberação do gás hidrogênio. Em uma experiência de laboratório adicionam-se quantidades iguais de ácido em duas amostras de mesma massa de zinco, uma delas em raspas (A) e a outra em pó (B). Para experiência citada, assinale a letra que representa o gráfico que corresponda a produção de hidrogênio em função do tempo de reação.
Considere:
v = volume de gás hidrogênio produzido.
t = tempo decorrido.
Provas
De forma geral, uma bateria de automóvel esgotada possui a seguinte composição média aproximada: 32% Pb, 3% PbO, 17% PbO2 e 36% PbSO4. A média de massa da pasta residual de uma bateria usada é de 6 kg, onde 19% é PbO2, 60% PbSO4 e 21% Pb. Dentre esses compostos de chumbo presentes na pasta, o que mais preocupa é o sulfato de chumbo (II), pois nos processos pirometalúrgicos, em que as placas das baterias são fundidas, há a conversão de sulfato em dióxido de enxofre, gás muito poluente. Para reduzir o problema das emissões do gás SO2, a indústria pode utilizar o processo hidrometalúrgico, para a dessulfuração antes da fusão do composto de chumbo. Nesse caso, a redução de sulfato presente no PbSO4 é feita via lixiviação com solução de carbonato de sódio (Na2CO3) 1M a 45 °C, em que se obtém o carbonato de chumbo (II) com rendimento de 91%. Após esse processo, o material segue para a fundição para obter o chumbo metálico.
Com base na equação química:
PbSO4 + Na2CO3 !$ \rightarrow !$ PbCO3 + Na2SO4
Considerando uma massa de pasta residual de uma bateria de 6 kg, qual quantidade aproximada, em quilogramas, de PbCO3 é obtida?
(Use massas molares em g/mol: Pb = 207; S = 32; Na = 23; O = 16; C = 12).
Provas
!$ \bullet !$ O ácido fosfórico é uma substância muito utilizada em diversas áreas, a exemplo das indústrias alimentícias, farmacêuticas e químicas. É comumente utilizada em alimentos, como acidulantes e estabilizantes, bem como na produção de antibióticos, insulinas e outros produtos farmacêuticos, até na fabricação de fertilizantes agrícolas ou mesmo na produção de carvão, dentre outros. Esse ácido pode ser obtido por diferentes processos em escala industrial, incluindo a reação de rochas, que contém apatita, com H2SO4 formando o H3PO4 e outros compostos como H2S!$ i !$F6 e CaSO4. Também, pode ser obtido pela queima do fósforo formando P4O10 que depois sofre hidrólise para não formá-lo.
A partir das informações acima e sobre os elementos P e S, responda a questão.
(URCA/2022.1) Sobre os átomos, considere as afirmativas a seguir e abaixo marque a alternativa que corresponde APENAS às afirmações corretas.
I. Os números quânticos do elétron mais energético do P são !$ n=3,\,l=1,\,m=+1,\,s=+\dfrac{1}{2} !$
II. As espécies representadas por 31p e 32p são isóbaros por possuírem mesmo número de prótons.
III. A composição percentual em massa do P4O10 e do H3PO4 são de 31,61% para P, 3,09% para H e 65,31% para O, em relação ao ácido, e 43,64% para P e 56,36% para O, em relação ao óxido.
IV. O fósforo tem dois alótropos: branco e vermelho.
As diferenças entre eles são na quantidade de átomos nas moléculas e na geometria.
Provas
Caderno Container