Foram encontradas 35.936 questões.
Analise as afirmações a seguir referentes à aromaticidade e a compostos aromáticos.
I - O calor liberado na hidrogenação do benzeno é menor que o liberado na hidrogenação de um trieno não aromático.
II - O benzeno sofre reações de adição de bromo (Br2) nas suas duplas ligações.
III - Segundo a Teoria do Orbital Molecular (TOM), o benzeno possui três orbitais moleculares !$ \pi !$ ligantes preenchidos com elétrons, além de apenas um orbital molecular antiligante.
IV - Por possuir ligações duplas e simples, há ligações carbono-carbono com diferentes comprimentos no benzeno.
Está correto APENAS, o que se afirma em
Provas
Analise a reação representada a seguir, na qual o produto formado não é apresentado.
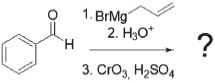
Qual o produto formado nas condições acima?
Provas
- Química InorgânicaSubstância e mistura: substância simples, substância composta e mistura. Alotropia
Dentre as classificações da matéria, tem-se substâncias puras, substâncias compostas e misturas de substâncias.
É um exemplo de substância pura o(a)
Provas
A técnica de proteção à corrosão no alumínio que consiste na deposição de uma camada de óxido de alumínio sobre a superfície é denominada
Provas
O tipo de corrosão que ocorre quando dois metais, com diferentes potenciais-padrão de redução, estão em contato em presença de um eletrólito é denominado corrosão
Provas
O processo de separação dos componentes de uma solução aquosa que se baseia na difusão desses componentes através de uma membrana polimérica, mediante um gradiente de concentração, é denominado
Provas
Numa célula eletroquímica, com dois eletrodos apropriados e contendo 100 mL de água, foram misturados 0,01 mol de FeCl3 e 0,01 mol de SnCl2. O sistema está a 25ºC e a 1 atm, e a adição dos sais não modificou o volume do conteúdo na célula.
Nessas condições, a diferença de potencial (!$ \Delta !$E) medida, em volts, é
Dado
Potências de redução versus eletrodo padrão de hidrogênio:
Fe3+ (aq) + e → Fe2+ (aq) !$ \quad !$ Eº = +0,77 V
Sn4+ (aq) + 2e → Sn2+ (aq) !$ \quad !$ Eº = +0,15 V
Equação de Nernst:
E = Eº redução – 0,06 log([produtos]n/[reagentes]m)
Provas
O óxido de prata é decomposto termicamente formando prata metálica e gás oxigênio como mostrado na reação:
Ag2O(s) → Ag(s) + ½ O2(g)
Considere o primeiro princípio da termodinâmica, o comportamento ideal dos gases e a perda de energia quando um sistema reacional se expande. Na reação de decomposição completa de 1 mol de óxido de prata, na temperatura de 300ºC, a variação de energia interna, em joules, é mais próxima de
Dado
!$ \Delta !$Hºf (Ag2O) = -31 kJ mol-1
!$ \Delta !$Hºf (573 K) = !$ \Delta !$Hºf (298 K)
pV = nRT
R = 8,3 J K mol-1
Provas
Um raio luminoso se propaga no ar e incide em um meio líquido. O ângulo de incidência do raio luminoso com a normal é indicado por !$ \alpha !$, e o ângulo de refração do raio luminoso com a normal é indicado por !$ \beta !$.
O índice de refração relativo do líquido em relação ao ar é indicado por
Provas
Em um equipamento de proteção radiológica, uma peça de 0,7 kg de chumbo tem sua temperatura elevada de 30ºC para 70ºC ao receber uma determinada quantidade de calor.
Sendo o calor específico do chumbo igual a 130 J kg-1K-1, a quantidade de calor, em joules, recebida pela peça é igual a
Provas
Caderno Container