Foram encontradas 1.896 questões.
A cromatografia líquida de alta eficiência é uma técnica de separação utilizada em análises de compostos não voláteis ou instáveis termicamente. Como a maioria dos compostos apresenta essas características, o campo de aplicação de HPLC é extremamente vasto. Em relação ao tema, avalie se as afirmativas a seguir são falsas (F) ou verdadeiras (V):
- O analito deve ser solúvel na fase móvel.
- O analito deve ser iônico.
- A fase móvel deve ser formada por um líquido polar puro.
As afirmativas são respectivamente:
Provas
Um laboratório dispõe de um cromatógrafo a gás com detector de ionização em chama. Com esse equipamento são realizados alguns ensaios por prestação de serviços. Considerando apenas este cromatógrafo, NÃO é possível fazer a determinação:
Provas
Para a determinação de chumbo em uma amostra de água subterrânea foi adotada a técnica potenciometria usando um eletrodo de íon seletivo. A curva analítica se mostrou linear para concentrações de chumbo entre 1,00x10–5 até 1,00x10–1 mol.L–1 , com coeficiente angular de 30 mV dec–1 . O potencial padrão do eletrodo, obtido por extrapolação, foi de 340 mV. O potencial apresentado pela amostra foi de 250 mV. A concentração de chumbo na amostra, em mol.L–1, é:
Provas
Uma solução padrão de β-caroteno em éter de petróleo com concentração 1,54 x 10–4 mol.L–1 apresentou no ultravioleta visível, absorbância igual a 0,400u.a. em comprimento de onda 450 nm em uma cubeta de 1 cm. Neste mesmo comprimento de onda, uma outra solução de β-caroteno em éter de petróleo com concentração desconhecida foi analisada. Nas mesmas condições de análise, a solução desconhecida apresentou absorbância igual a 0,850u.a. Nessas condições as amostras obedecem à lei de Beer. A concentração (em mol.L–1) da solução de concentração desconhecida de β-caroteno, nas condições da análise é igual a:
Provas
Na gravimetria por precipitação, o analito é convertido em um composto pouco solúvel. Após tratamento adequado, o composto final é separado e pesado. As relações estequiométricas definidas entre o composto final e o analito permitem a quantificação deste na amostra. Avalie se, para que esse método possa ser aplicado, o composto final obtido deve:
I. apresentar a composição química definida;
II. ter alta pureza ao precipitar;
III. deve ser filtrável apenas através de papel de filtro qualitativo.
Assinale a alternativa correta:
Provas
O teor de cobre em amostra de latão foi determinado por volumetria. 0,15g de amostra foi tratada com HNO3 à quente, até completa dissolução. Após resfriamento, adicionou-se soluções de H2SO4 e de H3PO4 e 10 mL de solução de iodeto de potássio 40%. Titulou-se a solução obtida com uma solução padrão 0,1 mol.L-1 de tiossulfato de sódio até aparecimento de coloração amarelo claro. Então se adicionou 3 mL de solução de amido (1%) e procedeu-se a titulação até desaparecimento da coloração azul por completo. O volume gasto de titulante foi 16,5 mL. O teor de cobre na amostra é:
Provas
Um técnico deseja confirmar a presença dos cátions Co2+, Ni2+, Zn2+ e Mn2+ em uma amostra. Para tanto, tomou uma pequena porção da amostra e adicionou solução NH4Cl/NH4OH e tioacetamida, sendo verificada, com aquecimento, a formação de precipitado. Este foi tratado com HCλ 6 mol.L-1 e centrifugado.
Sobrenadante e precipitado foram separados (sobrenadante 1 e precipitado 1). Ao sobrenadante 1 foi adicionado peróxido de hidrogênio e excesso de NaOH e um novo precipitado foi observado. A mistura foi centrifugada e o sobrenadante e o precipitado foram separados (sobrenadante 2 e precipitado 2). O precipitado 2 foi tratado com HNO3 concentrado e NaBiO3, formando uma solução púrpura. Ao sobrenadante 2 foi adicionado K4Fe(CN)6, porém não foi observada alteração significativa da coloração da solução, nem formação de precipitado. O precipitado 1 foi tratado com água régia, a quente.
Após a solubilização, o excesso de ácido foi neutralizado com solução de NaOH e a solução resultante foi dividida em duas parte: à primeira, adicionou-se NH4SCN e álcool amílico. Nenhuma alteração significativa foi observada. À segunda parte, foram adicionadas gotas de solução de dimetilglioxima e acetato de sódio, sendo observada a formação de precipitado rosa. O técnico então concluiu que está(ão) presente(s) na amostra apenas:
Provas
O clofibrato é um fármaco utilizado para diminuir as taxas de colesterol no sangue; este composto é sintetizado a partir do ácido p-cloro-fenoxiisobutírico, que possui temperatura de fusão 117-1180 C. O procedimento para a síntese do intermediário (ácido p-cloro-fenoxiisobutírico) descreve o seguinte: “(...) a um balão acoplado a um condensador, adicionar 4g de p-cloro-fenol, 30g de acetona anidra, 5g de clorofórmio e 7g de hidróxido de sódio em pastilhas. Aquecer sob refluxo durantes 4 horas. Eliminar, por destilação, o excesso de solvente. Adicionar 30mL de água quente e filtrar (...)”
Considere os seguintes esquemas de aparelhagens comuns no laboratório de química
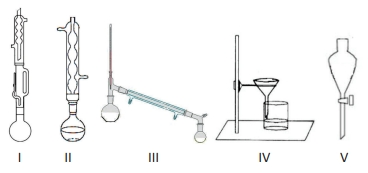
De acordo com o procedimento descrito para a síntese do ácido p-cloro-fenoxiisobutírico, foram utilizadas sequencialmente as aparelhagens:
Provas
O equilíbrio químico de um sistema pode ser estudado através da constante de equilíbrio de uma reação pois a lei de ação das massas de Guldberg e Waage estabelece que, no equilíbrio, a composição da mistura de reação pode ser expressa em termos de uma constante de equilíbrio. Considere o seguinte sistema em equilíbrio:
Ni(s) + 4CO(g) \( \rightleftarrows \) Ni(CO)4(g)
Sobre a constante desse equilíbrio, avalie as seguintes afirmativas:
I. Depende das concentrações das três substâncias no equilíbrio.
II. É diretamente proporcional a pressão parcial do Ni(CO)4.
III. É inversamente proporcional a pressão parcial do CO elevada a quarta potência.
Assinale a alternativa correta:
Provas
Entre os fatores que governam a velocidade das reações químicas podemos destacar a concentração de reagentes, a temperatura e o estado de agregação dos reagentes. As reações químicas são mais rápidas:
Provas
Caderno Container