Foram encontradas 80 questões.
Uma alíquota de 100 mL de uma solução que contém íons de Cr2+ e Cr3+ foi titulada com 200 mL de KMnO4 com concentração 0,01 mol/L (em ácido sulfúrico diluído), tendo sido todos os íons de Cr2+ oxidados a íons Cr3+. Em seguida, uma outra alíquota de 100 mL da solução original foi tratada com Fe metálico para converter todos os íons de Cr3+ em íons de Cr2+. A solução obtida consumiu 300 mL da mesma solução de KMnO4 para a oxidação de todos os íons a Cr3+. A equação iônica simplificada é: KMnO4 + 5Cr2+ \( \rightarrow \) Mn2+ + 5Cr3+ + 4H2O + K+
As concentrações molares de Cr2+ e de Cr3+ na solução original são:
Provas
“Amianto” é o nome genérico de muitos minerais fibrosos de silicatos. O amianto mais importante, o crisótilo, é um silicato de magnésio hidratado. O íon silicato do crisótilo é estruturado como linha dupla de tetraedros formados por átomos de Silício (círculos pretos) e de Oxigênio (círculos brancos) como representado na figura abaixo.
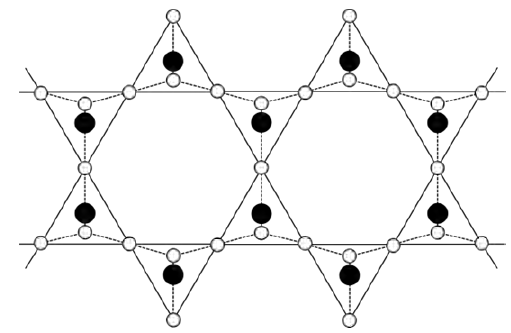
Diante do exposto, a composição geral do íon silicato do crisótilo é:
Provas
Na figura abaixo encontra-se ilustrada uma mistura em equilíbrio composta por BaCO3(s), BaO(s) e CO2(g), em sistema fechado, resultante da decomposição endotérmica do carbonato de bário.
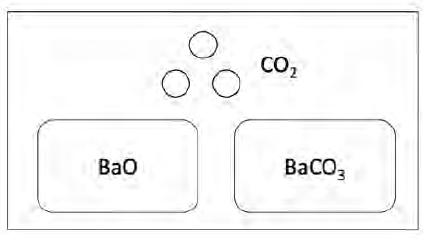
Considere as seguintes situações, tendo por base as moléculas de CO2(g):
i) o equilíbrio após uma adição de moléculas de CO2(g), de forma a triplicar a quantidade desse gás; e
ii) a mistura em equilíbrio a uma temperatura mais elevada.
A alternativa que melhor ilustra as situações i e ii, respectivamente, é:
Provas
O gás hélio, raro na Terra, origina-se notadamente do decaimento radioativo dos tipos e dos elementos Urânio-238 e Tório-234, sendo encontrado em depósitos de gás natural.
Sabe-se que o esquema de decaimentos até a ocorrência do isótopo Tório-230 é:
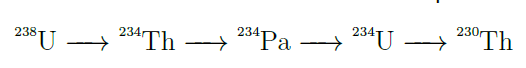
Portanto, a partir de 1 mol de Urânio-238 e de 1 mol de Tório-234, até a ocorrência de Tório-230, obtém-se, no máximo:
Provas
O cálcio metálico reage com hidrogênio gasoso para produzir hidreto metálico. A pressão de equilíbrio do hidrogênio gasoso em função do inverso da temperatura absoluta dessa reação segue o gráfico a seguir.
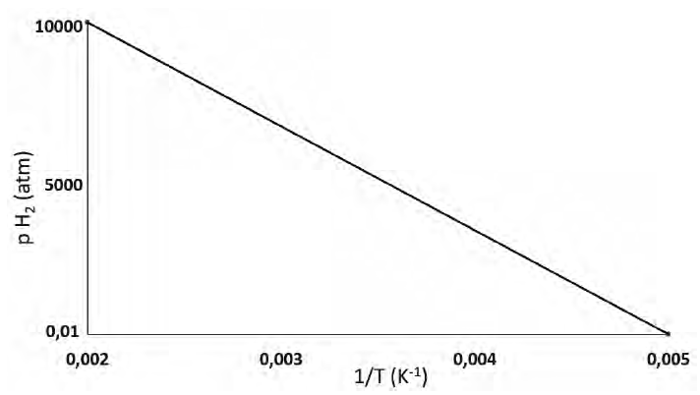
Dados:
• R = 8,0 J/(mol.K)
• ln(10) = 2,3
O calor, em kJ, envolvido na produção de 1 mol desse hidreto, a pressão constante de 1 atm, considerando comportamento de gás ideal, é aproximadamente igual a:
Provas
Considere cinco recipientes rígidos com o mesmo volume interno, nos quais são admitidas amostras de gases que são mantidas nas condições especificadas em cada opção abaixo. Levando em conta o comportamento de gases ideais, a alternativa que corresponde à maior pressão é:
Provas
Com relação aos compostos de interesse bioquímico abaixo, a alternativa INCORRETA é:
Provas
Um drone submarino estava navegando a 90 m de profundidade e a uma pressão de 10 atm, quando o casco sofreu uma avaria. Para trazê-lo à superfície, foi acionado um dispositivo de emergência, que produz hidrogênio por uma célula eletroquímica contendo 2 L de solução aquosa de H2SO4 com concentração 2 mol/L. A eletrólise foi encerrada quando o drone atingiu a superfície. Nesse momento, o restante da solução aquosa de H2SO4 foi analisado nas CNTP, tendo sido verificado que sua concentração era de 8 mol/L. A única alternativa correta é:
Provas
Considere o esboço parcial da Tabela Periódica representado abaixo.
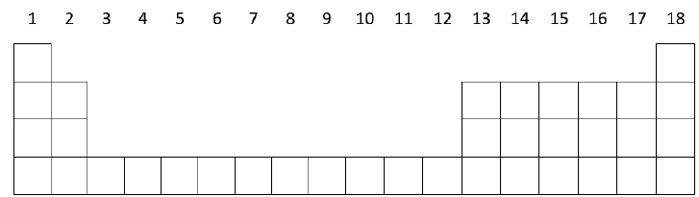
Sabe-se que um cátion trivalente apresenta o seguinte diagrama de preenchimento orbital:
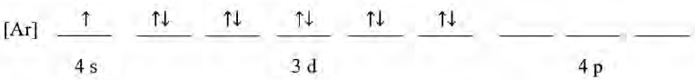
O elemento químico correspondente a esse cátion é o:
Provas
Considere as reações na sequência abaixo:
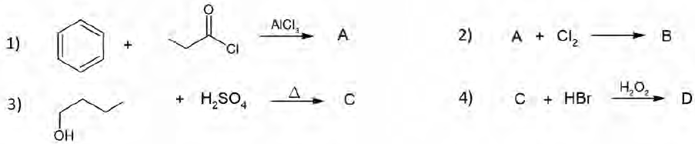
Sabendo que A, B, C e D representam os compostos orgânicos formados majoritariamente em cada uma das reações, a alternativa que contém as nomenclaturas viáveis para cada um desses compostos, respectivamente, é:
Provas
Caderno Container