Foram encontradas 2.410 questões.
Considere que as seguintes reações químicas paralelas competem em um processo industrial.
I. !$ A \, \rightarrow \, B \,\, -r_{A_I} \, = \, k_I c_A !$
II. !$ A \, \rightarrow \, C \,\, -r_{A_{II}} \, = \, k_{II} c^2_A !$
Nessas equações, !$ r_{A_I} !$ e !$ r_{A_{II}} !$ representam as taxas de reação de A nas reações I e II, respectivamente, !$ k_I !$ e !$ K_{II}, !$ as constantes de velocidade para as reações I e II, respectivamente, e !$ c_A, !$ a concentração em quantidade de matéria de A. A energia de ativação da primeira reação é aproximadamente o dobro da energia de ativação da segunda reação.
Considerando essas informações, julgue o seguinte item.
Um aumento da temperatura da câmara de reação fará que a razão !$ \dfrac {K_I} {K_{II}} !$ aumente.
Provas
Considere que as seguintes reações químicas paralelas competem em um processo industrial.
I. !$ A \, \rightarrow \, B \,\, -r_{A_I} \, = \, k_I c_A !$
II. !$ A \, \rightarrow \, C \,\, -r_{A_{II}} \, = \, k_{II} c^2_A !$
Nessas equações, !$ r_{A_I} !$ e !$ r_{A_{II}} !$ representam as taxas de reação de A nas reações I e II, respectivamente, !$ k_I !$ e !$ K_{II}, !$ as constantes de velocidade para as reações I e II, respectivamente, e !$ c_A, !$ a concentração em quantidade de matéria de A. A energia de ativação da primeira reação é aproximadamente o dobro da energia de ativação da segunda reação.
Considerando essas informações, julgue o seguinte item.
Do ponto de vista cinético, o emprego de maiores concentrações de A aumenta a seletividade do produto B em relação ao produto C no processo.
Provas
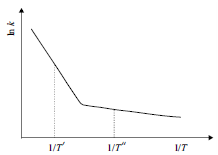
A figura acima apresenta um gráfico de ln !$ k !$ em função de !$ 1/T !$ para determinada reação química, em que !$ k !$ representa a constante de velocidade da reação e !$ T, !$ a temperatura de reação.
A partir dessas informações, julgue o item que se seguem.
O aspecto do gráfico demonstra que um mesmo mecanismo de reação pode apresentar duas energias de ativação diferentes.
Provas

A figura acima apresenta um gráfico de ln !$ k !$ em função de !$ 1/T !$ para determinada reação química, em que !$ k !$ representa a constante de velocidade da reação e !$ T, !$ a temperatura de reação.
A partir dessas informações, julgue o item que se seguem.
A energia de ativação da reação em questão é maior na temperatura !$ T' !$ que na temperatura !$ T". !$
Provas
Considerando o desempenho dos reatores de mistura perfeita e dos reatores pistonados, julgue o próximo item.
Um aumento da ordem de reação com relação aos reagentes minimiza as diferenças de desempenho entre os reatores de mistura perfeita e os reatores pistonados.
Provas
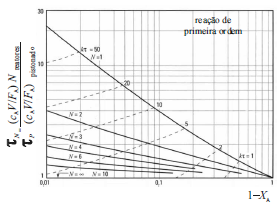
V. M. A.Calado e Edgard Blücher. Engenharia
das reações químicas, 3.ª ed., 2000, p.105.
A figura acima apresenta a comparação de desempenho de uma série de !$ N !$ reatores de mistura perfeita de mesma capacidade com o desempenho de um reator pistonado, para a reação de primeira ordem !$ A \, \rightarrow \, R, !$ com fator de expansão igual a zero. Nessa figura, !$ N !$ representa o número de reatores de mistura perfeita acoplados em série; !$ \tau_N !$ e !$ \tau_p, !$ os tempos espaciais dos !$ N !$ reatores de mistura perfeita acoplados e do reator pistonado, respectivamente; !$ c_A, !$ a concentração em quantidade de matéria de A na corrente de carga; !$ V, !$ o volume dos reatores (para reatores de mistura perfeita, !$ V !$ é a soma dos volumes individuais dos !$ N !$ reatores); !$ F_A, !$ a vazão de alimentação e !$ X_A, !$ a fração de conversão do reagente A.
A partir das informações e do gráfico fornecidos, julgue o item subsequente.
Um aumento do número de reatores de mistura perfeita acoplados em série faz que o desempenho do sistema se aproxime daquele de um reator pistonado.
Provas

V. M. A.Calado e Edgard Blücher. Engenharia
das reações químicas, 3.ª ed., 2000, p.105.
A figura acima apresenta a comparação de desempenho de uma série de !$ N !$ reatores de mistura perfeita de mesma capacidade com o desempenho de um reator pistonado, para a reação de primeira ordem !$ A \, \rightarrow \, R, !$ com fator de expansão igual a zero. Nessa figura, !$ N !$ representa o número de reatores de mistura perfeita acoplados em série; !$ \tau_N !$ e !$ \tau_p, !$ os tempos espaciais dos !$ N !$ reatores de mistura perfeita acoplados e do reator pistonado, respectivamente; !$ c_A, !$ a concentração em quantidade de matéria de A na corrente de carga; !$ V, !$ o volume dos reatores (para reatores de mistura perfeita, !$ V !$ é a soma dos volumes individuais dos !$ N !$ reatores); !$ F_A, !$ a vazão de alimentação e !$ X_A, !$ a fração de conversão do reagente A.
A partir das informações e do gráfico fornecidos, julgue o item subsequente.
Se a taxa de processamento e a alimentação forem iguais, a obtenção de uma mesma fração de conversão por meio do emprego de um reator de mistura perfeita e de um reator pistonado só será possível se o volume do reator de mistura perfeita for maior que o volume do reator pistonado.
Provas
Se a vazão de alimentação de um reator for modificada, então a taxa de reação do reagente A !$ (r_A) !$ e a concentração molar de A na corrente de saída !$ (C'_A) !$ irão variar; a figura abaixo traz um gráfico do log(-rA) em função do log!$ (C'_A) !$ para uma série de experimentos.
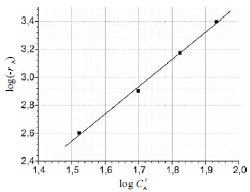
Com base nas informações prestadas, julgue o próximo item.
A reação que acontece no reator é de “ordem 1” em relação ao reagente A.
Provas
Um reagente puro gasoso A, com concentração em quantidade de matéria !$ C_A, !$ é alimentado a uma vazão volumétria !$ v_0 !$ em um reator estacionário ideal de mistura perfeita com volume !$ V. !$
Nesse reator, o reagente A se dimeriza para formar o produto P, também gasoso, segundo a equação 2A !$ \rightarrow !$ P. A taxa de reação de A é rA e a fração de conversão do reagente A é XA.
Considerando o sistema em questão e as informações fornecidas, julgue o item que se seguem.
A taxa de reação do produto P, !$ r_p, !$ relaciona-se com a taxa de reação do reagente A por meio da equação !$ r_p \, = \, - \, r_A. !$
Provas
Um reagente puro gasoso A, com concentração em quantidade de matéria !$ C_A, !$ é alimentado a uma vazão volumétria !$ v_0 !$ em um reator estacionário ideal de mistura perfeita com volume !$ V. !$
Nesse reator, o reagente A se dimeriza para formar o produto P, também gasoso, segundo a equação 2A !$ \rightarrow !$ P. A taxa de reação de A é rA e a fração de conversão do reagente A é XA.
Considerando o sistema em questão e as informações fornecidas, julgue o item que se seguem.
A taxa de consumo do reagente A pode ser calculada com auxílio da expressão !$ r_A \, = \, \dfrac {-C_A X_A} {V}. !$
Provas
Caderno Container