Foram encontradas 2.410 questões.
A energia específica superior (poder calorífico superior) de uma amostra de carvão, à pressão constante, vale 8,05 kcal/g.
A composição percentual mássica desse carvão é 78% de carbono, 6% de hidrogênio, 7% de oxigênio, 3% de nitrogênio, 2% de enxofre e 4% de cinzas. Considere que M(H) = 1,0 u, M(O) = 16,0 u e que, para a água líquida entre 20 ºC e 50 ºC, o calor de vaporização valha 586 cal/g, a capacidade calorífica específica (calor específico), 1,0 cal.g-1.ºC-1 e a densidade, 1,0 g/mL.
Considerando essas informações, julgue o seguinte item.
O poder calorífico inferior, à pressão constante, do carvão em questão é menor que 8 kcal/g.
Provas
O poder calorífico de uma amostra de carvão (PCc), cuja unidade no SI é J/kg, foi determinado em um calorímetro de combustão que opera a volume constante. Para isso, primeiramente foi realizada a queima de ácido benzoico, cujo poder calorífico a volume constante, PCa, é bem conhecido.
A variação de temperatura no calorímetro, quando da queima da massa ma de ácido benzoico, foi !$ \Delta T_a. !$ A seguir, foi realizada, sob condições idênticas, a queima de uma massa mc da amostra de carvão, quando se verificou uma variação de temperatura !$ \DeltaT_c !$ no calorímetro. Como a massa de amostra queimada é muito pequena comparada à massa do restante do conjunto, considere que a capacidade calorífica do sistema — calorímetro, oxigênio não reagido e produtos da combustão — seja invariável entre um experimento e outro.
Com relação à situação apresentada, julgue o próximo item.
A seguinte expressão é adequada para se determinar o poder calorífico da amostra de carvão em análise (PCc).
!$ P_{Cc} \, = \, \dfrac {P_{Ca} m_a \Delta T_a} {m_c \Delta T_c} !$
Provas
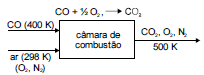
Em uma câmara de combustão, 1 kmol de CO disponível a 400 K é queimado completamente com 20% de excesso de ar, que é injetado na câmara a 298 K, conforme ilustra o esquema acima. Os gases de combustão saem da câmara de combustão a 500 K e 1 atm de pressão. Considere que a entalpia-padrão de combustão do CO, a 298 K, seja de -283 kJ/mol, que o ar seja composto por 20% de O2 e 80% de N2 (em quantidade de matéria) e que a capacidade calorífica à pressão constante do CO2 não varie entre 298 K e 300 K. Na tabela abaixo são informadas as entalpias molares de alguns gases !$ (\hat {H}º), !$ a 1 atm de pressão, para diferentes temperaturas, tendo como referência a temperatura de 298 K.
|
temperatura (K) |
!$ (\hat {H}º) !$ (J/mol) | |||
|
N2 |
O2 | CO |
CO2 |
|
|
298 |
0 | 0 | 0 | 0 |
| 300 | 58 | 58 | 58 | 74 |
| 400 | 2.967 | 3.020 | 2.971 |
3.991 |
| 500 | 5.916 | 6.079 | 5.924 |
8.292 |
Com base na situação descrita, nas considerações feitas e nos dados fornecidos, julgue o item que se seguem.
A capacidade calorífica à pressão constante do CO2, no intervalo de temperaturas entre 298 K e 300 K, é menor que 50 J.K-1 . mol-1.
Provas

Em uma câmara de combustão, 1 kmol de CO disponível a 400 K é queimado completamente com 20% de excesso de ar, que é injetado na câmara a 298 K, conforme ilustra o esquema acima. Os gases de combustão saem da câmara de combustão a 500 K e 1 atm de pressão. Considere que a entalpia-padrão de combustão do CO, a 298 K, seja de -283 kJ/mol, que o ar seja composto por 20% de O2 e 80% de N2 (em quantidade de matéria) e que a capacidade calorífica à pressão constante do CO2 não varie entre 298 K e 300 K. Na tabela abaixo são informadas as entalpias molares de alguns gases !$ (\hat {H}º), !$ a 1 atm de pressão, para diferentes temperaturas, tendo como referência a temperatura de 298 K.
|
temperatura (K) |
!$ (\hat {H}º) !$ (J/mol) | |||
|
N2 |
O2 | CO |
CO2 |
|
|
298 |
0 | 0 | 0 | 0 |
| 300 | 58 | 58 | 58 | 74 |
| 400 | 2.967 | 3.020 | 2.971 |
3.991 |
| 500 | 5.916 | 6.079 | 5.924 |
8.292 |
Com base na situação descrita, nas considerações feitas e nos dados fornecidos, julgue o item que se seguem.
A energia térmica liberada na câmara de combustão é menor que 200 MJ.
Provas

Em uma câmara de combustão, 1 kmol de CO disponível a 400 K é queimado completamente com 20% de excesso de ar, que é injetado na câmara a 298 K, conforme ilustra o esquema acima. Os gases de combustão saem da câmara de combustão a 500 K e 1 atm de pressão. Considere que a entalpia-padrão de combustão do CO, a 298 K, seja de -283 kJ/mol, que o ar seja composto por 20% de O2 e 80% de N2 (em quantidade de matéria) e que a capacidade calorífica à pressão constante do CO2 não varie entre 298 K e 300 K. Na tabela abaixo são informadas as entalpias molares de alguns gases !$ (\hat {H}º), !$ a 1 atm de pressão, para diferentes temperaturas, tendo como referência a temperatura de 298 K.
|
temperatura (K) |
!$ (\hat {H}º) !$ (J/mol) | |||
|
N2 |
O2 | CO |
CO2 |
|
|
298 |
0 | 0 | 0 | 0 |
| 300 | 58 | 58 | 58 | 74 |
| 400 | 2.967 | 3.020 | 2.971 |
3.991 |
| 500 | 5.916 | 6.079 | 5.924 |
8.292 |
Com base na situação descrita, nas considerações feitas e nos dados fornecidos, julgue o item que se seguem.
Na reação de combustão em apreço, o CO desempenha o papel de carburente.
Provas
Considere que o seguinte equilíbrio químico ocorra em uma solução aquosa.
[Cu(H2O)4]2+(aq) + 4 C!$ \ell^- !$(aq) !$ \rightleftharpoons !$ [CuC!$ \ell !$4]2-(aq) + 4 H2O (!$ \ell !$)
Estando a água em grande excesso, sua atividade pode ser considerada constante e a expressão da constante de equilíbrio da reação (K) se resume a:
!$ K \, = \, \dfrac {a_{[CuC \ell_4]^{2-}}} {a_{[Cu(H_2O)_4]^{2+} \times a^4_{C \ell^-}}} !$
Com relação à solução em que ocorre o equilíbrio químico citado, julgue o item abaixo.
Se o volume da solução for dobrado pela adição de água, o equilíbrio químico será deslocado no sentido da formação dos reagentes.
Provas
|
concentração inicial (mol/L) |
Velocidade inicial em relação a BrO3- (mol.L-1.s-1) |
||
|
BrO3- |
Br- | H+ | |
|
0,10 |
0,10 | 0,10 |
1,2 × 10-3 |
|
0,20 |
0,10 | 0,10 |
2,4 × 10-3 |
|
0,10 |
0,30 | 0,10 |
3,6 × 10-3 |
|
0,20 |
0,10 | 0,20 |
9,6 × 10-3 |
Os dados da tabela acima referem-se ao estudo, pelo método das velocidades iniciais, da cinética da reação a seguir
BrO3- (aq) + 5 Br- (aq) + 6 H+ (aq) !$ \rightarrow !$ 3 Br2 (aq) + 3 H2O (l)
Considerando essa reação e os dados fornecidos, julgue o item abaixo.
A constante de velocidade da reação em questão é igual a 10 L3.mol-3.s-1.
Provas
As capacidades caloríficas molares a pressão constante costumam ser expressas na forma geral !$ \overline {C}_{p} \, = \, a \, + \, bT \, + \, cT^2, !$ em que !$ T !$ representa a temperatura absoluta (em Kelvin) e a, b e c são parâmetros característicos de cada espécie química. Para o intervalo de temperaturas compreendido entre 298 K e 1.500 K, considere que aH2, bH2 e cH2 sejam os valores dos parâmetros em questão para o H2 (g); que aC!$ \ell !$2, bC!$ \ell !$2 e cC!$ \ell !$2 sejam os valores desses parâmetros para o C!$ \ell !$2 (g); e que aHC!$ \ell !$, bHC!$ \ell !$, e cHC!$ \ell !$ sejam os valores dos mesmos parâmetros para o HC!$ \ell !$(g). A tabela abaixo apresenta as entalpias de algumas ligações químicas (Hlig) a 298 K e 1 bAR.
|
ligação |
Hlig (kJ/mol) |
|
H—C!$ \ell !$ |
431 |
|
C!$ \ell !$—C!$ \ell !$ |
242 |
|
H—H |
436 |
Considerando a reação !$ ^1/_2 !$ H2 (g) + !$ ^1/_2 !$ C!$ \ell !$2 (g) !$ \rightarrow !$ HC!$ \ell !$(g) e os dados fornecidos, julgue o item a seguir.
A variação de entalpia dessa reação a uma temperatura !$ T !$ qualquer entre 298 K e 1.500 K pode ser corretamente calculada por meio da expressão a seguir, em que !$ \Delta H_T !$ representa a variação de entalpia da reação à temperatura !$ T !$ e !$ \Omega !$H298, a variação de entalpia da reação a 298 K.
!$ \Delta H_T \, = \, \Delta H_{298} \, + \, \begin {pmatrix} \dfrac {2a_{HC\ell} - a_{H2} - a_{C \ell2}} {2} \end {pmatrix} (T \, - \, 298) !$
!$ + \, \begin {pmatrix} \dfrac {2b_{HC\ell} - b_{H2} - b_{C \ell2}} {4} \end {pmatrix} (T^2 \, - \, 298^2) !$
!$ + \, \begin {pmatrix} \dfrac {2c_{HC\ell} - c_{H2} - c_{C \ell2}} {6} \end {pmatrix} (T^3 \, - \, 298^3) !$
Provas
As capacidades caloríficas molares a pressão constante costumam ser expressas na forma geral !$ \overline {C}_{p} \, = \, a \, + \, bT \, + \, cT^2, !$ em que !$ T !$ representa a temperatura absoluta (em Kelvin) e a, b e c são parâmetros característicos de cada espécie química. Para o intervalo de temperaturas compreendido entre 298 K e 1.500 K, considere que aH2, bH2 e cH2 sejam os valores dos parâmetros em questão para o H2 (g); que aC!$ \ell !$2, bC!$ \ell !$2 e cC!$ \ell !$2 sejam os valores desses parâmetros para o C!$ \ell !$2 (g); e que aHC!$ \ell !$, bHC!$ \ell !$, e cHC!$ \ell !$ sejam os valores dos mesmos parâmetros para o HC!$ \ell !$(g). A tabela abaixo apresenta as entalpias de algumas ligações químicas (Hlig) a 298 K e 1 bAR.
|
ligação |
Hlig (kJ/mol) |
|
H—C!$ \ell !$ |
431 |
|
C!$ \ell !$—C!$ \ell !$ |
242 |
|
H—H |
436 |
Considerando a reação !$ ^1/_2 !$ H2 (g) + !$ ^1/_2 !$ C!$ \ell !$2 (g) !$ \rightarrow !$ HC!$ \ell !$(g) e os dados fornecidos, julgue o item a seguir.
A variação de entalpia da reação em questão, a 298 K e 1 bAR, situa-se na faixa entre -100 kJ/mol e -90 kJ/mol.
Provas
O eteno (C2H4), gás de grande utilidade na indústria química, pode ser produzido a partir da desidrogenação catalítica do etano (C2H6), cuja equação é mostrada a seguir.
C2H6 (g) !$ \xrightarrow{\text{catalisador}} !$ C2H4 (g) + H2 (g)
No reator, ocorre também a seguinte reação paralela.
C2H6 (g) + H2 (g) !$ \rightarrow !$ 2CH4 (g)
A carga é alimentada no reator à vazão v, com frações molares de etano e gases inertes iguais a !$ x_{C_2H_6} !$ e !$ x_{in}, !$ respectivamente. O produto efluente do reator tem vazão !$ V' !$ e frações molares de etano, eteno, H2, CH4 e gases inertes iguais a !$ x'_{C_2H_6}, \, x'_{C_2H_4}, \, x'_{H_2}, \, x'_{CH_4} \,\, e \,\, x'_{in}, !$ respectivamente.
Considerando as reações em questão e as informações fornecidas, julgue o seguinte item.
A entalpia-padrão da reação de desidrogenação do etano gasoso (!$ \Delta !$Hº), a 25 ºC, pode ser calculada com auxílio da expressão a seguir, em que !$ \Delta !$Hºf (C2H6, g) representa a entalpia-padrão de formação do eteno gasoso a 25 ºC e !$ \Delta !$Hºf (C2H4, g) representa a entalpia-padrão de formação do etano gasoso a 25 ºC.
!$ \Delta !$Hº = !$ \Delta !$Hºf (C2H6, g) - !$ \Delta !$Hºf (C2H4, g)
Provas
Caderno Container