Foram encontradas 50 questões.
O sulfeto de sódio é um composto químico de fórmula molecular Na2S e que em água forma uma solução incolor. O Na2S e alguns derivados são perigosos e devem ser manuseados com cuidado, pois são cáusticos e causam queimaduras na pele. Quando exposto à umidade do ar, o Na2S começa a se degradar e libera o gás sulfeto de hidrogênio, que tem cheiro parecido com ovos podres e é altamente tóxico. Considere uma solução de um litro de 0,1 M de Na2S completamente dissolvido em água ultrapura. Qual é o pH dessa solução de sulfeto de sódio?
(Considere: Ka (H2S) = 1 x 10–7; massa molar (g/mol): Na2S = 78,05; H2S = 34,08.)
Provas
Foram realizados 3 experimentos para medir a velocidade de uma determinada reação (A + B → C). Os resultados obtidos, variando as concentrações molares dos reagentes e mantendo a temperatura constante, são apresentados a seguir. Sabe-se que a equação da velocidade dessa reação é: v = k . [A]X . [B]Y.
| Experimento |
[A] (mols/L) | [B] (mols/L) | Velocidade (mols/L.min) |
| 1 | 1,0 |
4,0 | 4 x 10-2 |
| 2 | 2,0 | 4,0 | 32 x 10-2 |
| 3 | 1,0 |
2,0 | 2 x 10-2 |
Com base nos valores encontrados, os valores X e Y da equação da velocidade são, respectivamente,
Provas
Analise o gráfico apresentado, que indica o comportamento de solubilização de dois sais: A e B. Em relação ao gráfico é INCORRETO afirmar que
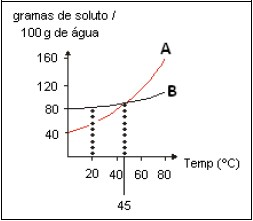
Provas
A tabela apresenta uma série de substâncias inorgânicas e orgânicas com diferentes características ácidas. Para cada uma das substâncias são fornecidos os respectivos valores de suas constantes de ionização ácida (Ka), bem como seus valores de pKa. Todos os valores se referem à acidez das substâncias em água e em uma temperatura de 25°C.
|
Substância |
Ka |
pKa |
|
H2CO3 |
4,2 x 10-7 |
6,38 |
|
HCN |
4,0 x 10-10 |
9,40 |
|
C6H5COOH |
6,3 x 10-5 |
4,20 |
|
H3PO4 |
7,5 x 10-3 |
2,12 |
|
HClO |
3,5 x 10-8 |
7,46 |
|
HNO2 |
4,5 x 10-4 |
3,35 |
A partir dos dados da tabela, assinale a alternativa INCORRETA.
Provas
A espectroscopia na região da radiação ultravioleta visível é uma importante técnica de análises quantitativas e um ótimo auxiliar na análise estrutural de compostos, principalmente orgânicos. Sobre a espectroscopia UV-visível, assinale a alternativa INCORRETA.
Provas
A gasolina é um combustível constituído basicamente por hidrocarbonetos e, em menor quantidade, por outros produtos oxigenados e sulforados. Esses hidrocarbonetos são, em geral, formados por moléculas de cadeias com 4 a 12 átomos de carbono. O 2,2,4-trimetilpentano é um alcano de cadeia ramificada, isômero do octano, conhecido como isooctano e presente na gasolina. O isooctano é utilizado como padrão na escala de octanagem da gasolina e queima no ar formando água e dióxido de carbono, conforme a equação apresentada.
2 C8H18 (l) + 25 O2 (g) → 16 CO2 (g) + 18 H2O (l) \( Δ \)H = – 10,92 kJ
Se 1 dm3 de isooctano for queimado, qual será a quantidade de calor liberada?
(Considere densidade do isooctano = 0,69 g/mL; massa molar C8H18 (g/mol) = 114,26.)
Provas
Numa estação espacial, cada tripulante exala ao redor, 19,6 litros de gás carbônico por hora. Uma forma de eliminar esse gás das estações espaciais é fazer a reação com hidróxido de sódio sólido. Os produtos dessa reação são o carbonato de sódio sólido e a água. Para efeito de cálculos, imagine que a reação se processe nas CNTP. Calcule e assinale a alternativa que apresenta o valor da massa de hidróxido de sódio necessário para que 4 tripulantes, com mesma taxa metabólica, permaneçam no espaço por uma semana. (Considere: R = 0,082 L.atm/mol.K; massas atômicas (g/mol): Na = 22,99; O = 16,00; H = 1,01; C = 12,01.)
Provas
O óxido nítrico (NO) é conhecido por monóxido de nitrogênio ou monóxido de azoto. O NO é um gás solúvel, altamente lipofílico, sintetizado pelas células endoteliais, macrófagos e certo grupo de neurônios do cérebro. Quando o NO reage com oxigênio, forma-se um novo gás marrom, o dióxido de nitrogênio (NO2), conforme a equação a seguir.
2 NO (g) + O2 (g) → 2 NO2 (g) \( Δ \)H = – 114 kJ
Assinale a alternativa que indica, respectivamente, o tipo de reação (endotérmica ou exotérmica), o valor variação de entalpia por cada mol de NO gasto na reação e qual o valor da energia envolvida na reação de 11,25 g de NO. (Considere massa molar (g/mol): NO = 30,01.)
Provas
Foi adicionado 1 x 10–9 mols de HCl em 1 litro de água ultrapura. Considerando que o HCl está 100% ionizado, qual o pH aproximado da solução? (Considere massa molar (g/mol): HCl = 36,46.)
Provas
Uma solução A foi produzida pela mistura de 20,05 g de HCl com água deionizada suficiente para completar o volume de 1 L em balão volumétrico. Uma solução B foi produzida pela mistura de 43,75 g com água deionizada para completar o volume de 500 mL em balão volumétrico. A partir das soluções A e B foram produzidas duas novas soluções (C e D). Uma solução C foi feita pela mistura de 650 mL da solução A com 150 mL da solução B. A solução D foi feita pela adição de 750 mL de água em 250 mL da solução C. A concentração em mols/L da solução C e a concentração em g/L da solução D são, respectivamente,
(Considere massa molar (g/mol): HCl = 36,46.)
Provas
Caderno Container