Foram encontradas 50 questões.
O metano (CH4) é um gás incolor. Sua molécula é tetraédrica e apolar, praticamente insolúvel em água e, quando em contato com o ar, forma uma mistura de alta inflamabilidade. É o mais simples dos hidrocarbonetos que reage com oxigênio, produzindo gás carbônico e água, conforme apresentado na equação 1.
Equação 1: CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g) \( Δ \)H = – 802,4 kJ/mol
Por outro lado, o metanol (CH3OH), também conhecido como álcool metílico, é um composto químico líquido, inflamável e possui chama invisível. É o álcool mais simples e que reage com oxigênio, também liberando gás carbônico e água, conforme apresentada na equação 2.
Equação 2: CH3OH (g) + 3/2 O2 (g) → CO2 (g) + 2 H2O (g) \( Δ \)H = – 676,0 kJ/mol
Sob condições especiais e controladas, é possível fazer o metano reagir com oxigênio e produzir metanol, conforme apresentado na equação 3.
Equação 3: CH4 (g) + 1/2 O2 (g) → CH3OH (g) \( Δ \)H = X
O valor da variação de entalpia relativa à terceira equação é
Provas
As aminas são compostos orgânicos pertencentes às classes dos derivados nitrogenados da amônia (NH3). São obtidas pela substituição total ou parcial do hidrogênio da amônia por ramificação alquilas ou arilas. O grau de substituição dos hidrogênios gera as aminas primárias, secundárias e terciárias. Além disso, se as ramificações das aminas forem iguais, são chamadas aminas simples, e seus substituintes forem diferentes são denominadas aminas compostas. As aminas são compostos orgânicos caracteristicamente básicos em água, e a sua estrutura química fornece uma boa aproximação de sua basicidade. A seguir, são apresentadas 5 aminas e 5 constantes de dissociação básica (Kb). Relacione as forças básicas dos compostos aos respectivos valores da constante de dissociação básica (Kb).
Substância
1. Amônia.
2. Metilamina.
3. Dimetilamina.
4. Trimetilamina.
5. Fenilamina.
Kb
( ) Kb = 4,3 x 10–4
( ) Kb = 5,3 x 10– 4
( ) Kb = 1,8 x 10–5
( ) Kb = 4,0 x 10– 10
( ) Kb = 5,5 x 10– 5
A sequência está correta em
Provas
Uma solução A foi produzida pela mistura de 575 cm3 de HCl 0,20 M com 425 mL de HCl 0,40 M. Uma solução B foi feita pela mistura de toda a solução A com 0,5 mL de uma solução de NaCl 0,35 M. Considere que todos os solutos estejam 100% dissociados e não ocorra nenhum tipo de reação. Assinale a alternativa que apresenta, respectivamente, as concentrações em g/L do HCl na solução A e do NaCl na solução B. (Considere massas molares (g/mol): HCl = 36,46; NaCl = 58,44.)
Provas
Um alvejante comercial utilizado para retirar manchas de roupas brancas foi produzido pela dissolução de 521,5 g de NaClO em água suficiente para que a solução final tenha concentração 0,70 mols/L. Assinale o volume de água que deve receber os 521,5 g de NaClO para que a solução resultante tenha concentração 0,70 mols/L.
(Considere massa molar (g/mol): NaClO = 74,5.)
Provas
A radiação infravermelha (IV) corresponde à parte do espectro eletromagnético situado entre as regiões do visível e das micro-ondas. A porção do espectro de maior utilidade na região da IV, para a análise de grupos funcionais de estruturas orgânicas, está situada entre os números de ondas 4000 e 400 cm–1. Diversos grupos funcionais, como hidroxilas, carbonilas e outros, apresentam comportamentos vibracionais específicos, quando submetidos à radiação IV, determinando os grupos funcionais presentes numa amostra. Assinale a alternativa INCORRETA.
Provas
Analise o gráfico, que representa a energia envolvida numa reação química em função do seu caminho reacional.
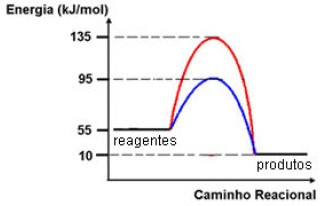
Assinale a afirmativa INCORRETA.
Provas
Catalisadores são substâncias químicas importantes em processos industriais. Sobre os catalisadores, assinale a afirmativa INCORRETA.
Provas
Ácido fórmico, ácido acético e ácido caproico são nomes usuais de alguns ácidos orgânicos muito comuns e amplamente utilizados em laboratórios. Assinale a alternativa que apresenta, respectivamente, os nomes oficiais dos ácidos fórmico, acético e caproico.
Provas
32 Uma das características das soluções do hidróxido de sódio é a capacidade de absorver gás carbônico (CO2). A equação desta reação é representada por: NaOH (aq) + CO2 (g) → A + B. As substâncias A, B e o volume de CO2 consumido na reação de 750 g de NaOH 80% são, respectivamente,
(Considere o volume molar do CO2 nas condições da reação como igual a 24 L/mol. Massas molares (g/mol): NaOH = 40,0; CO2 = 44,0.)
Provas
Estima-se que o cobre (Cu) tenha sido o primeiro metal utilizado pelo homem, sendo conhecido há pelo menos 10.000 anos. Os egípcios descobriram que a adição de pequenas quantidades de estanho facilitava a fusão do cobre e, a partir daí, aperfeiçoaram os métodos de obtenção do bronze. Atualmente, é possível produzir industrialmente o cobre metálico (Cu) utilizando-se o processo de ustulação do mineral calcosita. A equação Cu2S(s) + O2(g) → 2Cu(s) + SO2(s) representa a reação de ustulação da calcosita. Se uma tonelada de calcosita que contém 35% de impureza ocorrer com um rendimento de 54%, qual será a massa de cobre obtida? (Considere massas atômicas (g/mol): Cu = 63,55; S = 32,06; O = 16,00.)
Provas
Caderno Container