Foram encontradas 849 questões.
A proteção catódica é um dos métodos sugeridos para prevenção da biocorrosão em estruturas de aço-carbono. Em relação à técnica, é INCORRETO afirmar que
Provas
Um dos critérios mais usuais na avaliação da eficácia da proteção catódica por corrente impressa de uma estrutura enterrada é a medição do potencial eletroquímico. Como boa prática de medição do potencial, de forma que seja garantido que o sistema esteja efetivamente promovendo a proteção catódica da estrutura, deve-se
Provas
Vários casos práticos de biodegradação de substâncias e materiais por presença de organismos vivos são observados industrialmente. Dentre os casos de biodegradação relacionados, qual NÃO é observado na prática?
Provas
A medição do potencial de corrosão de metais ocorre em laboratórios que realizam projetos de pesquisa em corrosão eletroquímica. Diante do exposto, é correto afirmar que
Provas
Em relação às reações de oxidação-redução que ocorrem nos processos de corrosão eletroquímica, é INCORRETO afirmar que
Provas
A biocorrosão é um tipo de corrosão que pode ser encontrada em diversos sistemas, como, por exemplo, de resfriamento, envolvendo reações eletroquímicas. Ao imergir um eletrodo de aço-carbono em um meio contendo determinados micro-organismos, pode ocorrer a formação de tubérculos. Com relação aos processos que ocorrem nessa condição, é INCORRETO afirmar que
Provas
“A maioria das enzimas são proteínas que apresentam atividade catalítica. A região da estrutura terciária de uma enzima, responsável pela atividade catalítica, denomina-se sítio ativo ou sítio catalítico. De forma geral, o sítio catalítico ocupa cerca de 10 a 20% do volume total da enzima e é nesta região que o substrato se liga para ser transformado em produto. Para o substrato se ligar ao sítio ativo é necessário força entre as duas moléculas que ajude a estabilizar e ajustar o complexo formado entre a enzima e o substrato.” Diante do exposto, marque V para as afirmativas verdadeiras e F para as falsas.
( ) O substrato pode se ligar às enzimas por meio de interações eletrostáticas. Essas interações são formadas pelos grupos funcionais ionizáveis do substrato e estão carregados em solução aquosa (ou próxima ao pH 7) que se ligam, via complexo de cargas, com grupos ionizáveis de cargas opostas do sítio ativo da enzima. Do ponto de vista energético, a energia típica deste tipo de interação está na faixa de 25 a 50 kJ/mol e a sua força é inversamente proporcional à distância entre estas duas cargas.
( ) O substrato pode se ligar às enzimas por meio das interações (ou ligações) de hidrogênio. Este tipo de interação é formado entre pares de elétrons não ligantes de átomos de N (aminas, por exemplo) e O (alcoóis, por exemplo) de um aminoácido com átomos de H ácidos (hidroxilas alcoólicas, por exemplo) de outro aminoácido (ligações de hidrogênio intermoleculares), sendo amplamente utilizado para ligar grupos funcionais polares dos aminoácidos do substrato com a enzima. A força das ligações de hidrogênio depende da natureza química e da geometria do alinhamento dos grupos que interagem entre si. A energia associada a este tipo de interação varia na faixa de 2 a 25 kJ/mol, dependendo da polaridade e cargas dos aminoácidos ligantes.
( ) O substrato pode se ligar às enzimas por meio das interações (ou ligações) de Van der Waals, também chamadas de interações não polares. Este tipo de interação ocorre entre os dipolos momentâneos formados pelo movimento dos elétrons nas nuvens eletrônicas dos aminoácidos do substrato e da enzima. Embora, de forma geral, a soma da energia do conjunto total de interações de Van der Waals seja muito significativa nas interações enzima-substrato (cerca de 50 a 100 kJ/mol), sabe-se que individualmente cada interação de Van der Waals possui baixa energia (5 a 8 kJ/mol).
( ) O substrato pode se ligar às enzimas por meio das interações hidrofóbicas. Se o substrato possui grupos hidrofóbicos em sua estrutura (anel aromático, por exemplo) é possível estabelecer interações ligantes favoráveis às regiões hidrofóbicas do sítio ativo da enzima. Estas interações hidrofóbicas podem ser entendidas como uma tendência das moléculas orgânicas apolares (ou regiões apolares) se agregarem em soluções aquosas.
A sequência está correta em
Provas
Aminoácidos são moléculas orgânicas essenciais à formação das proteínas. Basicamente, as proteínas formadas do organismo humano são construídas por apenas vinte aminoácidos. Os aminoácidos têm características químicas inerentes às suas funções orgânicas. A figura a seguir apresenta a curva de titulação do aminoácido glicina (0,1 M e 25°C) com solução de NaOH (0,1 M e 25°C). Sobre essa curva, é correto afirmar que
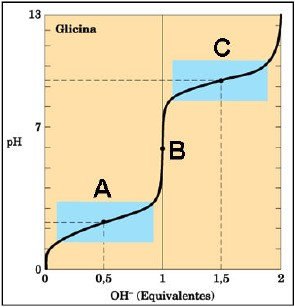
(Nelson e Cox. Princípios de Bioquímica de Lehninger. Ed. Artmed, 2011. – Com adaptações.)
Provas
Se as proteínas são as moléculas biológicas mais versáteis, por outro lado as macromoléculas mais abundantes são os carboidratos (também conhecidos como sacarídeos ou hidratos de carbono). Estima-se que, anualmente, 100 bilhões de toneladas de CO2 e H2O são convertidos em celulose e, outros subprodutos, pelas plantas. Classicamente, e de forma geral, os carboidratos são definidos como um composto derivado de estruturas polihidroxi aldeído ou um polihidroxi cetona. Entretanto, algumas classes de derivados de carboidratos podem apresentar outras funções orgânicas como aminas, amidas e ácidos carboxílicos. As três maiores classes de carboidratos são: monossacarídeos, dissacarídeos e polissacarídeos.
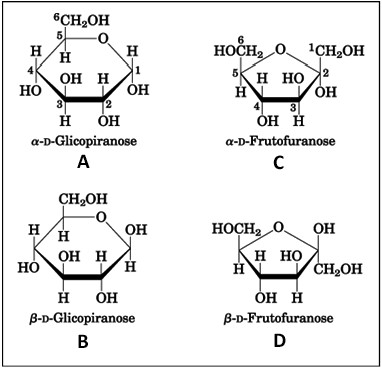
(Nelson e Cox. Princípios de Bioquímica de Lehninger. Ed. Artmed, 2011. – Com adaptações.)
Analise as estruturas químicas anteriores e assinale a alternativa INCORRETA.
Provas
É senso comum entre os cientistas que as proteínas são as macromoléculas mais versáteis dos sistemas vivos e cruciais para o correto funcionamento dos sistemas vivos. Esta classe de moléculas atua nas células desempenhando funções, tais como catalisadores biológicos, transporte de moléculas, suporte mecânico, resistência imunológica e controle do crescimento e diferenciação celular. Assinale a alternativa INCORRETA.
Provas
Caderno Container