Foram encontradas 760 questões.
Em Baku, capital do Azerbaijão (ex-União Soviética) aconteceu uma das maiores tragédias já ocorridas em metrô: 337 pessoas foram mortas em conseqüência de um incêndio em 28/10/1995. O fogo atingiu os vagões lotados quando o tremestava entre duas estações, o que dificultou a fuga das vítimas. A maioria dos mortos foi envenenada pelo monóxido de carbono que infestou o ar do túnel.
Internet: <www.super.abril.com.br/revista/237> (com adaptações).
O monóxido de carbono (CO) é um gás incolor, sem cheiro e muito tóxico. Não é muito reativo, em grande parte, devido à sua entalpia de ligação (1.074 kJ × mol-1). O CO é muito usado na formação de complexos com átomos do bloco d da tabela periódica, pois ele pode formar ligações com esses átomos, tanto partilhando o par de elétrons isolados do carbono para formar uma ligação quanto utilizando seu orbital !$ \pi !$ antiligante para acomodar elétrons cedidos por esses átomos para formar uma ligação. Um complexo de CO muito conhecido é o níquel tetracarbonila (Ni(CO)4), um líquido formado em uma das etapas de um antigo processo de refino do níquel.
Segundo a teoria do campo cristalino, o complexo formado apresenta a configuração !$ e_g^4\,t_{2g}^4 !$ , ou seja, os dois orbitais eg têm energia abaixo da energia média enquanto os três orbitais t2g têm energia acima da energia média.
A formação de complexos é também responsável pela toxicidade do CO, que se liga mais fortemente ao ferro (II) do grupo heme na hemoglobina que o oxigênio e impede que o oxigênio do ar presente nos pulmões passe para a corrente sanguínea.
Considerando os textos acima, julgue o item seguinte.
Todos os elementos do bloco d da tabela periódica são metais.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
As equações I e II representam, respectivamente, a ionização do cloreto de sódio e a dissociação da água.
Provas
Derramamentos de óleo flutuante de origem desconhecida ocorrem frequentemente em rios, águas abertas e vias navegáveis litorais.
Em 2002, um derramamento de milhares de litros de óleo nos rios Rouge e Detroit impactou aproximadamente 43 km das linhas costeiras dos EUA e do Canadá. Podia-se observar um brilho intenso sobre a maioria da área impactada dos rios. Na costa, o óleo apareceu como um revestimento preto com 0,2 mm a 1,0 mm de espessura. Amostras do óleo foram coletadas e analisadas por peritos. A análise, feita por cromatografia gasosa,revelou que o óleo era composto, em sua maior parte, de óleo lubrificante usado, contendo principalmente alcanos de 15 a 40 carbonos e parafinas cíclicas, misturado com uma parcela menor de dísel combustível, sendo que o óleo dísel encontrava-se gasto e degradado. Hidrocarbonetos aromáticos policíclicos (PAH = polycyclic aromatic hydrocarbons) pirogênicos, produzidos provavelmente por processos de combustão e lubrificação de motores, também foram encontrados nas amostras do derramamento.
Considerando as informações do texto acima, julgue o item a seguir.
Caso, além do derramamento de óleo, houvesse também um derramamento de ácido nítrico nos rios citados, de forma que este ácido entrasse em contato com o óleo, e caso houvesse também uma fonte termal que aquecesse a água dos rios, poderia ocorrer a nitração dos componentes do óleo, formando compostos em que hidrogênios seriam substituídos por grupos –NO2.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
A reação anódica é de redução.
Provas
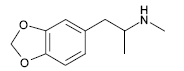
O ecstasy, cuja fórmula estrutural é mostrada acima, é uma droga psicoativa semi-sintética, da família das anfetaminas. Seu consumo provoca um grande efeito estimulante e pequenos efeitos visuais. É considerada principalmente uma droga de recreação, mas é usada também para práticas de transcendência — meditação, terapia psicodélica etc. O ecstasy é proibido em muitos países, incluindo o Brasil, e sua posse, produção ou venda pode resultar em processo criminal.
Considerando o texto acima e a fórmula estrutural do ecstasy, julgue os itens que se seguem.
O ecstasy, quando em solução aquosa, forma ligações de hidrogênio com as moléculas de água.
Provas
As aplicações forenses da espectroscopia UV-VIS incluem a análise de narcóticos e os testes para drogas. No teste do bafômetro, por exemplo, a quantidade de álcool no sangue pode ser determinada borbulhando-se o ar da respiração em uma solução acidificada de K 2 Cr 2 O 7 . O etanol presente na respiração é oxidado pelo dicromato, produzindo ácido acético e Cr 3+ . A concentração de etanol na amostra de respiração é determinada com base na diminuição da concentração do íon dicromato na solução que pode ser monitorada pela diminuição da absorvância a 440 nm.
Com base nessas informações, julgue os itens seguintes.
O texto permite inferir que a banda de absorção do íon dicromato ocorre a 440 nm.
Provas
O processo de desenvolvimento de um fármaco inicia-se com a síntese e a determinação das características físico-químicas do princípio ativo. Essa análise inicial garante que a atividade observada nos ensaios in vivo é decorrente do princípio ativo no medicamento. A respeito dos parâmetros físico-químicos que podem ser utilizados durante o desenvolvimento de um xarope, julgue os itens a seguir.
O volume molar do xarope é muito maior quando comparado ao de um gás.
Provas

O ecstasy, cuja fórmula estrutural é mostrada acima, é uma droga psicoativa semi-sintética, da família das anfetaminas. Seu consumo provoca um grande efeito estimulante e pequenos efeitos visuais. É considerada principalmente uma droga de recreação, mas é usada também para práticas de transcendência — meditação, terapia psicodélica etc. O ecstasy é proibido em muitos países, incluindo o Brasil, e sua posse, produção ou venda pode resultar em processo criminal.
Considerando o texto acima e a fórmula estrutural do ecstasy, julgue os itens que se seguem.
O ecstasy possui um anel aromático e os grupos funcionais éter e amina secundária.
Provas
Em 1916, o monge russo Rasputin sofreu uma tentativa de envenenamento por cianeto. Durante um banquete, o príncipe Yussopoff e seus amigos ofereceram a Rasputin um pudim que continha cianeto de potássio em quantidade suficiente para matar várias pessoas. Embora Rasputin tenha comido grande quantidade desse pudim, ele não morreu. Por esse motivo e pelo fato de serem atribuídos poderes satânicos ao monge, criou-se uma lenda de sobrenaturalidade envolvendo o fato. A lenda só foi desfeita em 1930, quando foi descoberto que alguns açúcares, como a glicose e a sacarose, se combinam com o cianeto por meio da carbonila, formando uma substância praticamente sem toxicidade, denominada cianidrina. Um possível mecanismo dessa reação é apresentado a seguir:
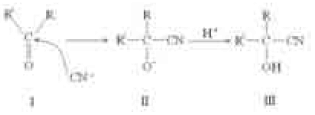
A ação tóxica do HCN deve-se à sua capacidade de inibir a enzima citocromoxidase, fundamental para as célulasconsumirem o gás oxigênio transportado pelo sangue. O íon cianeto provoca, então, a parada da respiração celular.
Considerando o texto apresentado, julgue o item subsequente.
Na reação entre o íon cianeto e o grupo carbonila, o cianeto comporta-se como nucleófilo.
Provas
Até meados do século XIX, as cirurgias eram realizadas sem anestesia, às vezes com a administração de quantidades apreciáveis de álcool, justificada pela crença de que o paciente ficaria entorpecido. Em 1846, William Morton conseguiu demonstrar que o éter dietílico podia ser usado para produzir inconsciência temporária durante os procedimentos cirúrgicos. Um problema dessa prática era o fato de o éter formar com o oxigênio do ar uma mistura explosiva, e qualquer choque entre os instrumentos metálicos cirúrgicos podia resultar em uma centelha e consequentemente em ignição. Outra substância usada como anestésico, o clorofórmio !$ H CC \ell_3 !$ 3 foi considerado melhor que o éter, pois a recuperação era mais rápida e menos desagradável. No entanto, alguns pacientes morriam; apesar disso, os riscos associados eram considerados pequenos. A partir de 1857, o clorofórmio tornou-se o anestésico preferido para os partos sem dor, na Europa e nos Estados Unidos. Atualmente, o clorofórmio não é mais usado para tal fim.
Acerca das substâncias citadas no texto, julgue o item a seguir.
O clorofórmio pertence à classe dos haletos de alquila.
Provas
Caderno Container