Foram encontradas 760 questões.
Acerca dos métodos de análise, julgue os itens subseqüentes.
Na gravimetria, para se obter precipitados fáceis de filtrar, é preciso usar soluções concentradas, fazer a adição rápida de reagente precipitante, agitar a solução e trabalhar a quente.
Provas
Aproximadamente 140 milhões de toneladas de gás amoníaco são produzidos anualmente pelo processo de Haber, que combina nitrogênio retirado do ar com gás hidrogênio, conforme representa a equação não-balanceada a seguir. O gás amoníaco é matéria-prima para a produção de ácido nítrico e NH4NO3, este último empregado como fertilizante e explosivo.
!$ N_2(g) + H_2(g) \rightleftharpoons NH_3(g) !$
Considerando as informações acima e sabendo que M(H) = 1 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
O composto iônico de amônio empregado como fertilizante pode ser obtido conforme a equação a seguir.
!$ NH_3(g) + HNO_3 \overset{evaporação} { (aq) \rightarrow} NH_4 NO_3(s) !$
Provas
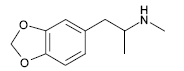
O ecstasy, cuja fórmula estrutural é mostrada acima, é uma droga psicoativa semi-sintética, da família das anfetaminas. Seu consumo provoca um grande efeito estimulante e pequenos efeitos visuais. É considerada principalmente uma droga de recreação, mas é usada também para práticas de transcendência — meditação, terapia psicodélica etc. O ecstasy é proibido em muitos países, incluindo o Brasil, e sua posse, produção ou venda pode resultar em processo criminal.
Considerando o texto acima e a fórmula estrutural do ecstasy, julgue os itens que se seguem.
O espectro de infravermelho do ecstasy deve apresentar uma banda relativa ao estiramento C–O–C, uma banda fraca e outra de intensidade média, provocadas pela absorção da ligação C=C no anel aromático, e outra banda de absorção média referente à ligação N– H da amina, entre outras.
Provas
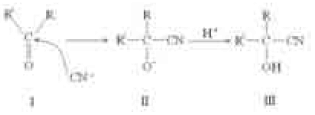
Em 1916, o monge russo Rasputin sofreu uma tentativa de envenenamento por cianeto. Durante um banquete, o príncipe Yussopoff e seus amigos ofereceram a Rasputin um pudim que continha cianeto de potássio em quantidade suficiente para matar várias pessoas. Embora Rasputin tenha comido grande quantidade desse pudim, ele não morreu. Por esse motivo e pelo fato de serem atribuídos poderes satânicos ao monge, criou-se uma lenda de sobrenaturalidade envolvendo o fato. A lenda só foi desfeita em 1930, quando foi descoberto que alguns açúcares, como a glicose e a sacarose, se combinam com o cianeto por meio da carbonila, formando uma substância praticamente sem toxicidade, denominada cianidrina. Um possível mecanismo dessa reação é apresentado a seguir:
A ação tóxica do HCN deve-se à sua capacidade de inibir a enzima citocromoxidase, fundamental para as célulasconsumirem o gás oxigênio transportado pelo sangue. O íon cianeto provoca, então, a parada da respiração celular.
Considerando o texto apresentado, julgue o item subsequente.
A citocromoxidase atua como catalisador, por diminuir a entalpia da reação catalisada.
Provas
Derramamentos de óleo flutuante de origem desconhecida ocorrem frequentemente em rios, águas abertas e vias navegáveis litorais.
Em 2002, um derramamento de milhares de litros de óleo nos rios Rouge e Detroit impactou aproximadamente 43 km das linhas costeiras dos EUA e do Canadá. Podia-se observar um brilho intenso sobre a maioria da área impactada dos rios. Na costa, o óleo apareceu como um revestimento preto com 0,2 mm a 1,0 mm de espessura. Amostras do óleo foram coletadas e analisadas por peritos. A análise, feita por cromatografia gasosa,revelou que o óleo era composto, em sua maior parte, de óleo lubrificante usado, contendo principalmente alcanos de 15 a 40 carbonos e parafinas cíclicas, misturado com uma parcela menor de dísel combustível, sendo que o óleo dísel encontrava-se gasto e degradado. Hidrocarbonetos aromáticos policíclicos (PAH = polycyclic aromatic hydrocarbons) pirogênicos, produzidos provavelmente por processos de combustão e lubrificação de motores, também foram encontrados nas amostras do derramamento.
Considerando as informações do texto acima, julgue o item a seguir.
É possível usar um espectrômetro de massa como detector no sistema de cromatografia gasosa. Comparado a um detector de UV-VIS, um detector de massa tem a vantagem de ser mais sensível e preciso, porém não permite identificar os compostos eluentes como o primeiro.
Provas
O processo de desenvolvimento de um fármaco inicia-se com a síntese e a determinação das características físico-químicas do princípio ativo. Essa análise inicial garante que a atividade observada nos ensaios in vivo é decorrente do princípio ativo no medicamento. A respeito dos parâmetros físico-químicos que podem ser utilizados durante o desenvolvimento de um xarope, julgue os itens a seguir.
As forças de Van der Waals geradas no xarope são maiores do que as geradas em um gás.
Provas
Aproximadamente 140 milhões de toneladas de gás amoníaco são produzidos anualmente pelo processo de Haber, que combina nitrogênio retirado do ar com gás hidrogênio, conforme representa a equação não-balanceada a seguir. O gás amoníaco é matéria-prima para a produção de ácido nítrico e NH4NO3, este último empregado como fertilizante e explosivo.
!$ N_2(g) + H_2(g) \rightleftharpoons NH_3(g) !$
Considerando as informações acima e sabendo que M(H) = 1 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Considerando que o NH3 tenha comportamento de gás ideal, em CNTP, o volume de gás amoníaco produzido anualmente é inferior a 200 mil m3.
Provas
Derramamentos de óleo flutuante de origem desconhecida ocorrem frequentemente em rios, águas abertas e vias navegáveis litorais.
Em 2002, um derramamento de milhares de litros de óleo nos rios Rouge e Detroit impactou aproximadamente 43 km das linhas costeiras dos EUA e do Canadá. Podia-se observar um brilho intenso sobre a maioria da área impactada dos rios. Na costa, o óleo apareceu como um revestimento preto com 0,2 mm a 1,0 mm de espessura. Amostras do óleo foram coletadas e analisadas por peritos. A análise, feita por cromatografia gasosa,revelou que o óleo era composto, em sua maior parte, de óleo lubrificante usado, contendo principalmente alcanos de 15 a 40 carbonos e parafinas cíclicas, misturado com uma parcela menor de dísel combustível, sendo que o óleo dísel encontrava-se gasto e degradado. Hidrocarbonetos aromáticos policíclicos (PAH = polycyclic aromatic hydrocarbons) pirogênicos, produzidos provavelmente por processos de combustão e lubrificação de motores, também foram encontrados nas amostras do derramamento.
Considerando as informações do texto acima, julgue o item a seguir.
Uma das vantagens de se usar cromatografia gasosa no referido tipo de análise é que ela é um método de separação adequado para compostos orgânicos voláteis, encontrados na matriz analisada.
Provas
Aproximadamente 140 milhões de toneladas de gás amoníaco são produzidos anualmente pelo processo de Haber, que combina nitrogênio retirado do ar com gás hidrogênio, conforme representa a equação não-balanceada a seguir. O gás amoníaco é matéria-prima para a produção de ácido nítrico e NH4NO3, este último empregado como fertilizante e explosivo.
!$ N_2(g) + H_2(g) \rightleftharpoons NH_3(g) !$
Considerando as informações acima e sabendo que M(H) = 1 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Sabendo que a solubilidade do NH3 ,em 1 L de água, a 0 °C e 1 atm de pressão, é de 1.300 L, é correto concluir que as substâncias NH3 e H2O são fortemente polarizadas.
Provas
Em 1916, o monge russo Rasputin sofreu uma tentativa de envenenamento por cianeto. Durante um banquete, o príncipe Yussopoff e seus amigos ofereceram a Rasputin um pudim que continha cianeto de potássio em quantidade suficiente para matar várias pessoas. Embora Rasputin tenha comido grande quantidade desse pudim, ele não morreu. Por esse motivo e pelo fato de serem atribuídos poderes satânicos ao monge, criou-se uma lenda de sobrenaturalidade envolvendo o fato. A lenda só foi desfeita em 1930, quando foi descoberto que alguns açúcares, como a glicose e a sacarose, se combinam com o cianeto por meio da carbonila, formando uma substância praticamente sem toxicidade, denominada cianidrina. Um possível mecanismo dessa reação é apresentado a seguir:

A ação tóxica do HCN deve-se à sua capacidade de inibir a enzima citocromoxidase, fundamental para as célulasconsumirem o gás oxigênio transportado pelo sangue. O íon cianeto provoca, então, a parada da respiração celular.
Considerando o texto apresentado, julgue o item subsequente.
A espécie II do mecanismo apresentado é um estado de transição.
Provas
Caderno Container