Foram encontradas 743 questões.
Uma solução de carbonato de potássio (K2C03) foi preparada a partir da solubilização de 6,99 desse sal em 10mL de água a 20ºC. Essa solução foi transferida sem perdas para um balão volumétrico de 500mL, que foi avolumado com água deionizada até o traço de aferição. Um técnico coletou uma alíquota de 200mL dessa última solução e adicionou 600mL de solução aquosa de !$ Na C\ell !$0,5 mol.L-1. À concentração de K2CO3, em mol.L-1?, na solução salina preparada pelo técnico corresponde a:
!$ [M_a(u);\,K = 39; C \ell = 35,5; Na= 23; O = 16; C=12 ] !$
Provas
O Diagrama de Hommel, conhecido pelo código NFPA 704, é uma simbologia empregada para expressar os riscos de uma substância de acordo com a figura abaixo:
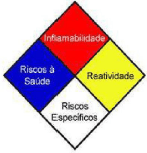
Em cada uma das cores, exceto branco, é utilizada uma escala de zero (0 — substância sem risco) a quatro (4 — risco sério ou grave). Para o losango branco, utilizam-se códigos para riscos específicos, como OXI (oxidante), ACID (ácido), IX (reage com água de maneira perigosa) etc.
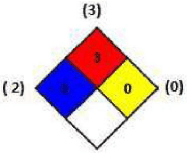
A substância que apresenta o diagrama de Hommel abaixo é
Provas
Soluções podem ser definidas como
Provas
Um certo tipo de titânio utilizado em implantes na coluna vertebral pesa em média 18g. O número de átomos de titânio presente nesse tipo de parafuso é de
!$ (Considere\,N_A = 6,0 X 10^{23}\,e\,M_a(u): Ti = 48) !$
Provas
Uma amostra de minério de ferro de 3,5g foi dissolvida em !$ HC \ell !$ concentrado e depois diluída em água. Adicionou-se !$ NH_3 !$ à solução para precipitar o ferro da amostra na forma de óxido de ferro hidratado !$ Fe_2O_3 !$ ∙ !$ xH_2O !$. O precipitado foi separado por filtração, lavado e o resíduo foi calcinado a alta temperatura, gerando 2,2g de !$ Fe_2O_3 !$ puro. A porcentagem de ferro presente na amostra é de
!$ [M_a(u): Fe = 56; C \ell = 35,5; O = 16; N = 14; H=1] !$
Provas
Analise as afirmativas a seguir, em relação às grandezas químicas:
I. O número de átomos, íons ou moléculas por mol é aproximadamente 6,0221 × 1023.
II. A massa de um átomo é dada pela média das massas dos isótopos naturais ponderada pela ocorrência de cada isótopo.
III. A massa molar de uma substância é resultante do somatório do número total de átomos multiplicado pela constante de Avogadro.
IV. Um mol de espécies contém um determinado número de espécies igual ao número de átomos que existem em precisamente 12g de carbono-12.
V. O volume molar de um gás é constante e igual a 22,41 L.mol-1 em quaisquer condições.
Assinale
Provas
É correto afirmar, quanto às propriedades físicas dos compostos orgânicos, que
Provas
A fluoresceína é um composto sintético largamente utilizado em tingimentos industriais e em análises de determinação de elementos químicos como bromo e iodo. A molécula da substância é mostrada abaixo:

Assinale a alternativa em que as funções orgânicas presentes na molécula de fluoresceína estejam corretamente listadas.
Provas
Uma medida de dispersão em torno de uma média populacional de uma variável aleatória é calculada pela raiz quadrada da razão entre o somatório dos desvios quadrados dos dados em relação à média da população e o número de dados que compõem a população. Tal medida é largamente empregada na análise estatística de dados e é conhecida como
Provas
De acordo com a Portaria 344/1998, todas as classes de substâncias e medicamentos listadas nas alternativas a seguir estão sujeitas a controle especial, À EXCEÇÃO DE UMA. Assinale-a.
Provas
Caderno Container