Foram encontradas 90 questões.
A icterícia, condição bastante comum em recém-nascidos, é caracterizada pela cor amarelada da pele. Esse problema relaciona-se à dificuldade do fígado para metabolizar a bilirrubina, um pigmento gerado pelo metabolismo das células vermelhas do sangue. A principal terapia em uso para icterícia é a fototerapia, com a exposição do recém-nascido a uma fonte luminosa.
Devido às propriedades da bilirrubina e da pele, a luz mais efetiva para esse tratamento é a com comprimentos de onda predominantemente entre 425 nm e 475 nm, no espectro da cor azul. Luzes de outras cores, como a verde, têm espectro de emissão fora do espectro de absorção da molécula de bilirrubina. Já a luz ultravioleta emitida pelas lâmpadas de fototerapia é praticamente absorvida em sua totalidade pelo vidro da lâmpada e pela cobertura da unidade de fototerapia.
(Scientia Medica, v. 15, abril/junho de 2005. Adaptado.)
A figura mostra a curva de absorção da bilirrubina em função do comprimento de onda da luz.
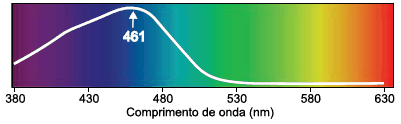
(www.sarda.org.ar. Adaptado.)
Adotando-se c = 3 x 108 m/s, sabendo que 1 nm = 10– 9 m e de acordo com as informações do texto e da figura, tem-se que
Provas
A escala Brix, com valores expressos em ºBx (graus brix), é uma escala numérica que indica a quantidade de sólidos solúveis em uma solução de sacarose. Essa escala é utilizada na indústria de alimentos para medir a porcentagem aproximada de açúcares em sucos de fruta, vinhos, bebidas carbonatadas etc. Uma solução de 25 ºBx, por exemplo, tem 25 gramas de açúcar de sacarose por 100 gramas da solução. O gráfico mostra a relação entre a escala Brix e o índice de refração absoluto de uma solução de sacarose.
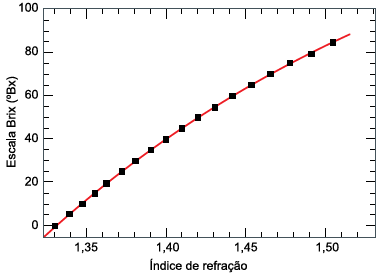
(www.omega.com. Adaptado.)
Considere um raio de luz monocromática que, propagando-se pelo ar, incide na superfície que separa o ar de uma solução de sacarose de 40 ºBx. Adotando c = 3 x 108 m/s, quando esse raio refratar-se para a solução de sacarose, terá velocidade de propagação de, aproximadamente,
Provas
Em uma brincadeira, uma pessoa coloca um copo com a boca para baixo, encostada na superfície parada da água de uma piscina e, cuidadosamente, o afunda 2,5 m abaixo da superfície da água, onde mantém o copo em repouso, ainda de boca para baixo, com um pouco de ar aprisionado em seu interior e com um pouco de água que entrou no copo. A figura mostra o copo nessas duas posições.
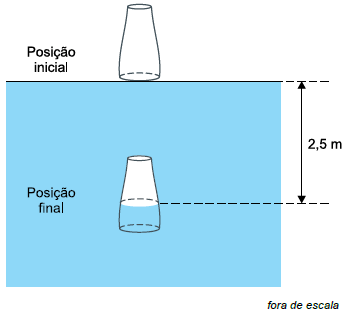
Considere o ar um gás ideal e os valores \( 10^3{\large{kg \over m^3}} \) para a densidade da água da piscina, 105 Pa para a pressão atmosférica local e \( 10{\large{m \over s^2}} \) para a aceleração da gravidade. Sendo V1 o volume ocupado pelo ar no copo na posição inicial, V2 o volume ocupado pelo ar no copo na posição final, e considerando a temperatura do ar dentro do copo constante nesse processo, o valor da razão \( {\large{V_2 \over V_1}} \) é
Provas
A figura 1 representa uma molécula de DNA, que se assemelha a uma escada contorcida, isto é, tem o formato de uma dupla hélice. Analisado quimicamente, o DNA apresenta duas fitas complementares unidas por ligações existentes entre os pares de bases nitrogenadas, que podem ser adenina, citosina, timina ou guanina.
Figura 1

(www.biologianet.com. Adaptado.)
Considere que as duas bases nitrogenadas, B1 e B2, representadas na figura 2 por suas fórmulas estruturais, sejam ligadas uma à outra apenas pelas ações das forças elétricas F1, F2, F3 e F4 decorrentes das combinações O ... H – N e N – H ... N, mostradas em destaque, e que essas combinações sejam paralelas entre si.
Figura 2
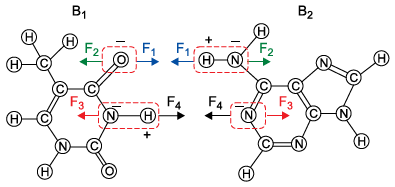
(Hugh D. Young e Roger A. Freedman. Física III. Eletromagnetismo, 2016. Adaptado.)
Sabendo que as intensidades das forças são F1 = 8,0 x 10– 9 N, F2 = 3,0 x 10– 9 N, F3 = 2,6 x 10– 9 N e F4 = 6,4 x 10– 9 N, e considerando os possíveis pareamentos entre as bases nitrogenadas no DNA, as bases B1 e B2 são, respectivamente,
Provas
Uma pessoa estava parada com seu veículo em um semáforo. Quando a luz verde do semáforo se acendeu, o veículo partiu e o movimento realizado até o seu destino pode ser dividido em quatro trechos:
Trecho 1: veículo em movimento acelerado;
Trecho 2: veículo em movimento uniforme;
Trecho 3: percebendo que havia passado do endereço para onde ia, a pessoa freou o veículo até parar, e inverteu o sentido de seu movimento, com a mesma aceleração escalar com que havia freado;
Trecho 4: nova frenagem, chegando ao seu destino, onde parou o veículo.
Os três gráficos, I, II e III, mostram como variaram, em função do tempo, três grandezas escalares associadas ao movimento desse veículo, sem identificá-las, nos quatro trechos descritos.
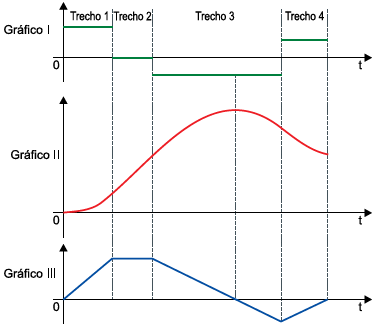
Sabendo que, enquanto se movia nesse trajeto, o veículo só esteve em movimento uniforme ou em movimento uniformemente variado, os gráficos I, II e III representam, respectivamente, as grandezas
Provas
Uma das etapas da fermentação láctea consiste na transformação de ácido pirúvico em ácido láctico, pela reação representada pela equação:
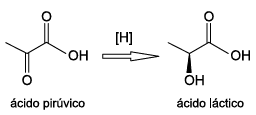
Na transformação de ácido pirúvico em ácido láctico ocorre do grupo de um composto opticamente , formando um composto opticamente .
As lacunas do texto são preenchidas, respectivamente, por:
Provas
Água de cal é o nome dado à solução aquosa saturada de cal hidratada [hidróxido de cálcio, Ca(OH)2]. A concentração dessa solução saturada a 20 ºC é de 1,7 g/L. A partir desse dado, estima-se que o valor da constante do produto de solubilidade em água (Kps) nessa temperatura é próximo de
Provas
Analise a tabela, que apresenta valores da entalpia padrão de combustão completa (ΔcH0) de três substâncias diferentes.
|
Substância |
Fórmula | Produtos da combustão completa |
ΔcH0 de combustão completa (kJ/mol) |
|
Ácido acético |
C2H4O2 (\( \ell \)) | CO2 (g) e H2O (l) |
– 874 |
|
Carbono |
C (s,grafita) | CO2 (g) |
– 394 |
|
Hidrogênio |
H2 (g) | H2O (l) |
– 286 |
A partir desses valores de entalpia de combustão, é possível calcular a entalpia de formação do ácido acético, que é, em kJ/mol, igual a
Provas
A montagem de laboratório ilustrada na figura destina-se à coleta e medida do volume de produto gasoso gerado numa reação química.
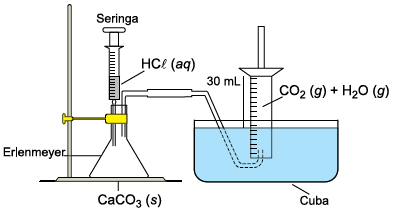
Em um experimento, envolvendo a produção de dióxido de carbono gasoso, CO2 (g), a partir da reação entre carbonato de cálcio, CaCO3 (s), e solução aquosa diluída de ácido clorídrico, HC\( \ell \) (aq), o líquido empregado para a coleta do gás foi a água acidulada. Um comprimido de CaCO3 foi triturado e uma porção do pó resultante foi colocada no erlenmeyer da montagem e posta para reagir com solução de HC\( \ell \), adicionada a partir da seringa da montagem. Após a reação, o produto gasoso coletado no cilindro graduado teve seu volume determinado, sendo igual a 30 mL. Sabe-se que o produto gasoso recolhido é uma mistura de dióxido de carbono gasoso e vapor de água.
Considerando que o experimento foi realizado sob pressão atmosférica de 726,7 mmHg e temperatura de 27 ºC, que a pressão de vapor da água a 27 ºC é igual a 26,7 mmHg e que a constante universal dos gases, R, é igual a 62,3 mmHg · L · mol–1 · K–1, a massa de carbonato de cálcio que reagiu na produção de dióxido de carbono gasoso foi de, aproximadamente,
Provas
O sistema Li/MnO2 é o exemplo mais representativo das pilhas primárias (de uso único) de lítio.

(www.smartkits.com.br)
Essas pilhas empregam eletrólitos dissolvidos em solventes não aquosos, em recipientes selados.
O processo de descarga dessa pilha envolve a reação 4Li + MnO2 → 2Li2O + Mn
Essa pilha fornece uma diferença de potencial (voltagem) em torno de 3,0 V à temperatura ambiente, mas mostra excelente desempenho em temperaturas superiores.
A grande vantagem das pilhas à base de lítio é a ausência de metais pesados reconhecidamente danosos ao meio ambiente, como mercúrio, cádmio e chumbo. Porém, os perigos relativos à pilha Li/MnO2 são de outra natureza, estando relacionados ao seu descarte e reciclagem. Após a corrosão do invólucro externo, é liberado o solvente não aquoso, inflamável e tóxico. O lítio metálico não reagido, em contato com água e umidade do ar, desprende calor e gás inflamável (hidrogênio), podendo levar à ignição do produto descartado. Por isso, a presença de voltagem residual nesse resíduo é um problema, pois significa a presença de lítio metálico.
As características listadas para a pilha de lítio tornam a disposição final inadequada e até mesmo a reciclagem uma operação de risco, pela possibilidade de fogo e explosão.
(Jéssica Frontino Paulino et al. “Processamento de pilhas Li/MnO2 usadas”. Quim. Nova, vol. 30, 2007. Adaptado.)
Para tornar a reciclagem dessa pilha mais segura, o ideal seria o seu descarregamento completo antes do descarte, evitando assim a
Provas
Caderno Container