Foram encontradas 13.432 questões.
ln 0,50 = –0,69.
Provas
Provas
Provas
Provas
Para responder a questão, utilize o enunciado a seguir.
Diversas aplicações industriais de soluções exploram, simplesmente, os efeitos da presença de partículas de umsoluto num sistema, independentemente da sua natureza. Uma das situações mais familiares é a adição de etilenoglicol (“anticongelante”) ao líquido de arrefecimento dos radiadores dos carros. Isto é necessário, pois o congelamento da água no motor pode provocar danos na estrutura devido à expansão da água (aumento de volume) durante o congelamento. O etilenoglicol diminui a temperatura de congelamento da água (crioscopia), prevenindo o congelamento em dias de temperatura abaixo de 0 °C; este aditivo também aumenta o ponto de ebulição (ebulioscopia) permitindo que o sistema do motor opere acima de 100 ºC sem criar altas pressões; a pressão de vapor também diminui (tonoscopia), e o fluxo de solvente é afetado quando uma solução é separada do solvente puro por uma membrana semipermeável (osmose). Estas são propriedades coligativas de soluções.
Forças intermoleculares podem dar origem a soluções não ideais que exibem pressão de vapor total da mistura líquida diferente daquela esperada pela Lei de Raoult. Em função da natureza e magnitude das forças entre as moléculas, a pressão de vapor pode ser maior (desvio positivo) ou menor (desvio negativo).
Prediga os desvios da Lei de Raoult, quando existir, e numere os parênteses associando-os com as classificações dadas para os desvios.
1 → Solução ideal ou aproximadamente ideal (pressão de vapor total que se aproxima daquela calculada pela Lei de Raoult; desvio praticamente inexistente)
2 → Desvio positivo (pressão de vapor total maior daquela calculada pela Lei de Raoult)
3 → Desvio negativo (pressão de vapor total menor daquela calculada pela Lei de Raoult)
( ) benzeno e n-hexano.
( ) n-hexano e 2,2,4-trimetilpentano.
( ) etileno glicol e tetracloreto de carbono.
( ) metanol e acetona.
( ) ácido acético e n-propanol.
A sequência correta é
Provas
A cana-de-açúcar pode servir como matéria prima para produção de combustíveis como etanol e biodiesel. No caso do biodiesel, é necessária a utilização de uma bactéria especial que transforma caldo de cana em óleo. Abaixo são apresentadas, de forma geral, as principais etapas de produção desses combustíveis.
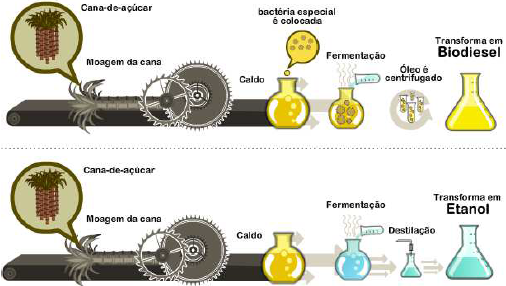
Disponível em: <http://g1.globo.com>. Acesso em: 15 nov. 2016.
O processo de separação para a obtenção do biodiesel e do etanol são distintos, pois
Provas
As cores que observamos são uma consequência da interação da radiação eletromagnética com a matéria. Equipamentos modernos permitem aos cientistas de diversas áreas, inclusive da química, selecionar regiões do espectro eletromagnético para investigar processos moleculares específicos, tais como transições eletrônicas e vibrações moleculares.
Considere as seguintes afirmações:
I → Uma solução de um complexo que está sobre a bancada de trabalho de um químico tem coloração vermelha. Portanto, o espectro UV-visível desta solução deve apresentar pelo menos uma banda de absorção na região de comprimento de onda próxima do vermelho (620 - 800 nm).
II → A radiação na região de micro-ondas pode ser usada no estudo de transições rotacionais de moléculas poliatômicas.
III → Um espectro registrado na região do infravermelho contém informações sobre transições vibracionais. Tais transições, que decorrem da absorção na região do infravermelho, também são acompanhadas por transições rotacionais.
Está(ão) correta(s)
Provas
A formação das cores dos objetos está relacionada com a região visível do espectro eletromagnético, que abrange a faixa de 400 até 760 nm. A cor apresentada pelo objeto depende do comprimento de onda absorvido !$ (λ) !$, pois assim ele é removido e não atinge o nervo ótico, fazendo com que o cérebro interprete como cor do objeto a cor complementar do comprimento de onda absorvido.
Considere os espectros de absorção representados na figura a seguir.

Agora, analise as seguintes informações:
I → O espectro C pertence a um material de cor vermelha.
II → O espectro A pode ser de um vidro transparente.
III → O objeto que gera o espectro B deve ser violeta.
IV → Todos os objetos que originam os espectros da figura absorvem no ultravioleta.
Está(ão) correta(s)
Provas
Uma grandeza útil para avaliar o grau de desvio do comportamento do modelo ideal por um gás real é o fator de compressibilidade Z, que corresponde à razão entre o volume molar do gás real e o volume molar do gás ideal. O gráfico a seguir traz a relação de Z coma pressão para alguns gases comuns.
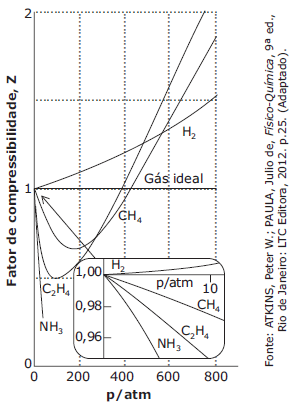
Considerando o gráfico e as informações expostas, analise as seguintes afirmativas.
I → O desvio do comportamento ideal pelo H2 é justificado pela forte interação atrativa existente entre as moléculas constituintes do gás.
II → Em baixas pressões, o valor de Z para o etano é menor do que para o metano devido à maior interação atrativa por forças de dispersão no etano.
III → A amônia apresenta desvio acentuado por causa de fortes ligações de hidrogênio.
IV → Em pressões maiores que 400 atm, as interações repulsivas no metano são maiores que as do etano.
Está(ão) correta(s)
Provas
"É impossível executar uma análise química que seja totalmente livre de erros ou incertezas. Tudo o que podemos fazer é minimizar os erros e estimar seu tamanho com a exatidão adequada. Uma das primeiras questões a ser respondida antes de uma análise é: qual é o erro máximo que eu posso tolerar no resultado? A resposta desta pergunta definirá o tempo necessário para executar o trabalho e o nível de investimento. E ninguém quer perder tempo gerando dados que sejam mais confiáveis do que o necessário”.
SKOOG, Douglas, A., WEST, Donald, M., HOLLER, F. James.
Fundamentals of Analytical Chemistry, 7a ed.,
Nova Iorque: Saunders College Publishing, 1996, pág 11, (traduzido).
Considerando as definições dos termos relacionados ao tratamento de dados experimentais e tipos de erros, numere as afirmações dos parênteses, associando-as aos termos a seguir.
1 → Erro absoluto
2 → Erro relativo
3 → Erro randômico ou aleatório
4 → Erro sistemático
5 → Erro constante
6 → Erro proporcional
( ) Afeta a exatidão da medida.
( ) Afeta a precisão da medida.
( ) Corresponde à diferença entre o valor medido e o valor real. Pode ser nulo, ou ter um sinal positivo ou negativo.
( ) Depende do tamanho da amostra.
( ) Não depende do tamanho da amostra.
( ) Corresponde à diferença entre o valor medido e o valor real, dividida pelo valor real.
Agora, assinale a sequência correta.
Provas
Caderno Container