Foram encontradas 13.249 questões.
Provas
Os principais processos utilizados numa Estação de Tratamento de Esgotos (ETE) são definidos de acordo com o poluente a ser removido. Sobre isso, assinale a alternativa INCORRETA.
Provas
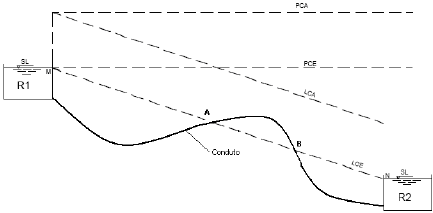
PCE – Plano de Carga Estático;
LCA – Linha de Carga Absoluta;
LCE – Linha de Carga Efetiva.
Provas
Provas
Acerca da estatística aplicada à química analítica, relacione a primeira coluna, que apresenta as técnicas para redução de erros sistemáticos, à segunda, que apresenta as descrições dessas técnicas, e, em seguida, assinale a opção correta.
I – Determinação do branco da amostra
II – Análise de controle
III – Adição padrão
IV – Padrões internos
( ) Análise de uma substância padrão nas condições experimentais usadas na análise da amostra.
( ) Adição de uma quantidade fixa de um material de referência a uma série de amostras de concentrações conhecidas da substância a ser determinada. Os valores obtidos permitem a construção de um gráfico que propicia a determinação da concentração de uma amostra desconhecida, após a adição à amostra da mesma quantidade do material de referência, e de sua localização no gráfico.
( ) Adição à amostra de uma quantidade conhecida do constituinte a ser determinado. Analisa-se, a seguir, a amostra para determinar a quantidade total do constituinte.
( ) Execução de uma análise nas mesmas condições experimentais usadas na análise da amostra, porém na ausência do constituinte de interesse.
A sequência correta é:
Provas
Os fenóis e seus derivados aparecem nas águas naturais por meio das descargas de efluentes industriais. Indústrias de processamento da borracha, colas e adesivos, resinas impregnantes, componentes elétricos (plásticos) e as siderúrgicas, entre outras, são responsáveis pela presença de fenóis nas águas naturais. Os fenóis constituem-se em padrão de potabilidade, sendo imposto o limite máximo bastante restritivo de 0,001mg/L.
Internet: www.cetesb.sp.gov.br. Acesso em 29/1/2010 (com adaptações).
O fenol pode ser quantificado por espectrofotometria de absorção. O comprimento de onda indicado para a realização da medida de absorção de fenol é 293nm. Acerca desse método, julgue os itens abaixo como Verdadeiros (V) ou Falsos (F) e, em seguida, assinale a opção correta.
I – A espectrofotometria descrita utiliza radiação eletromagnética da região do visível.
II – Quanto maior a concentração de fenol, maior será a intensidade da luz transmitida.
III – O coeficiente de absorção molar do fenol, que é um parâmetro necessário para a determinação da concentração de fenol na amostra, depende do comprimento de onda da luz incidente, da temperatura e do solvente.
A sequência correta é:
Provas
A presença de fluoreto em água pode ser determinada por potenciometria, empregando um eletrodo seletivo de fluoreto e um eletrodo de referência, geralmente o eletrodo de calomelano. Com base nisso, julgue os itens abaixo e, em seguida, assinale a opção correta.
I – No método apresentado no texto, mede-se a diferença de potencial entre o eletrodo seletivo e o de referência para determinar a concentração da espécie iônica em solução.
II – Na potenciometria com eletrodo seletivo, é necessária a realização de calibração empregando soluções padrão.
III – A utilização do método da adição padrão dispensa a determinação da curva de calibração.
IV – O aparelho que mede a força eletromotriz da célula formada pelos eletrodos seletivo e de referência é, em última análise, um voltímetro.
V – No método em apreço, o potencial é mantido fixo e a corrente fornecida pelo sistema é medida, sendo proporcional à concentração do fluoreto na amostra.
A quantidade de itens certos é igual a
Provas
O método padrão para determinação de cálcio em água é a titulação dos íons cálcio com EDTA (Y). A equação geral pode ser escrita como: Ca2+ + Y4- ⇌ CaY2-. Para a análise de 50ml de água para a determinação de cálcio foram gastos 10ml de EDTA (0,01mol/L). Sabendo que M(Ca)=40g/mol, assinale a opção que apresenta a massa de cálcio presente em 1L da água analisada.
Provas
O sulfato presente em meio aquoso pode ser determinado com uma reação com o cloreto de bário, a qual forma um precipitado, o sulfato de bário, que depois é pesado. Entretanto, antes da pesagem, é fundamental proceder à calcinação do sulfato de bário entre 600ºC e 800ºC. Acerca da calcinação, assinale a opção correta.
Provas
Provas
Caderno Container