Foram encontradas 13.249 questões.
A pérola de vidro ou de impacto é uma das partes que compõem o dispositivo de nebulização e queima por mistura prévia, usado em espectroscopia de absorção atômica. A função de pérola de vidro ou de impacto é de
Provas
Questão presente nas seguintes provas
Alíquotas de 25,00 mL de cinco soluções distintas (I a V - tabela abaixo) contendo NaOH, Na2CO3 e NaHCO3, isoladamente ou em combinação compatível, foram tituladas com HCl 0,1000 mol L-1 usando a fenolftaleína como indicador. Outras alíquotas de 25,00 mL das mesmas soluções foram tituladas usando dessa vez o verde de bromocresol como indicador. Os resultados das titulações estão expressas na tabela abaixo.
| SOLUÇÃO | V (mL) de HCl 0,1000 mol L-1 | |
| fenolftaleína | verde de bromocresol | |
| I | 20,0 | 20,0 |
| II | 10,0 | 40,0 |
| III | 0 | 20,0 |
| IV | 10,0 | 20,0 |
| V | 30,0 | 40,0 |
Sabendo que o intervalo de pH de mudança de cor da fenolftaleína é 8,2 - 10,0 e do verde de bromocresol é 3,8 - 5,4, a solução que apresenta corretamente as massas, em mg, dessas espécies em 25,00 mL, de acordo com os dados das titulações, é
Provas
Questão presente nas seguintes provas
A titulação potenciométrica de 25,00 mL de um ácido fraco monoprótico por uma solução de NaOH 0,100 mol L−1 gerou os dados de pH em função do volume de NaOH 0,100 mol L−1, a partir dos quais foi construído o gráfico da derivada segunda, !$ \Delta !$( !$ \Delta !$pH/ !$ \Delta !$V)/ !$ \Delta !$V x V (mL).
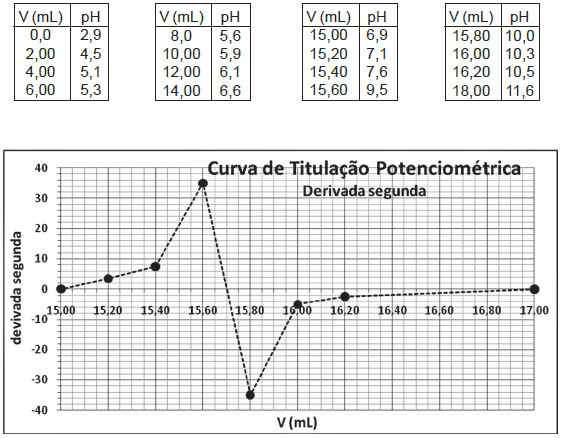
De acordo com os dados da tabela e do gráfico acima, o volume de equivalência e o valor do pKa desse ácido fraco são, respectivamente,
Provas
Questão presente nas seguintes provas
Em um método gravimétrico, foi constatada uma perda de 0,3 mg de Zn, que por sua vez corresponde a um erro relativo de 0,5%. De acordo com esse resultado, a massa de zinco analisada foi de
Provas
Questão presente nas seguintes provas
Uma das características da espectroscopia de absorção atômica com chama é que a (o)
Provas
Questão presente nas seguintes provas
Uma mistura, contendo 6,4 g de gás oxigênio e certa massa de gás nitrogênio, foi colocada em um recipiente de 10 L. Sabendo-se que para esse sistema uma pressão total de 107 kPa foi medida a uma temperatura de 303 K, a massa de gás nitrogênio na mistura, em g, era igual a
Dado: R = 0,082 L atm K-1 mol-1 = 8,31 JK-1 mol-1
Provas
Questão presente nas seguintes provas
Deseja-se neutralizar 5,0 L de uma solução de ácido perclórico, de pH igual a 2,0, pela adição de hidróxido de sódio sólido. Desprezando-se variações de volume e considerando- se que a pureza do reagente empregado (NaOH) é de 95%, a massa dessa base necessária para neutralização completa da solução ácida, em g, é igual a
Provas
Questão presente nas seguintes provas
A espectrofotometria de absorção na região visível do espectro eletromagnético é uma das ferramentas mais utilizadas para análise quantitativa. Sua aplicação se baseia na Lei de Beer, sobre a qual foram feitas as afirmações a seguir.
I - Em uma série de soluções-padrão, de um determinado analito quanto mais fraca for a cor da solução, maior será a transmitância.
II - O caminho ótico é o diâmetro externo da cubeta e não o seu diâmetro interno.
III - A absorvância é diretamente proporcional ao poder radiante e ao comprimento de onda.
Está correto APENAS o que se afirma em
Provas
Questão presente nas seguintes provas
A reação:
2N2O(g) !$ \rightleftharpoons !$ 2N2(g) + O2 (g) !$ \Delta !$H0 = - 55,0 kJ.mol-1
apresenta energia de ativação igual a 121 kJ.mol-1, se ouro for empregado como catalisador e 134 kJ.mol-1 se, alternativamente, platina for empregada como catalisador. Sobre esse sistema fechado, considere as afirmativas a seguir.
I – Um aumento de temperatura diminuiria o tempo para se atingir o equilíbrio e aumentaria o rendimento do processo.
II – O emprego de ouro como catalisador conduz o processo mais rapidamente ao equilíbrio, quando comparado ao emprego de platina.
III – A uma dada temperatura, o emprego dos catalisadores ao processo altera a velocidade da reação, no entanto as concentrações dos gases no equilíbrio permanecem inalteradas.
IV – Um aumento da pressão total do sistema (pela diminuição do volume) levaria a um aumento do rendimento da reação no equilíbrio.
Estão corretas APENAS as afirmativas
Provas
Questão presente nas seguintes provas
A fim de se determinar a densidade de um determinado líquido, um laboratorista realiza uma experiência. Sobre uma balança digital, coloca um becker graduado, contendo o líquido em questão. Nesse primeiro procedimento, a leitura da balança é 5,52 kg, e o nível do líquido no becker está na marca 1250 mililitros. Um objeto esférico e metálico é amarrado a uma extremidade de um pedaço de fio, inextensível e de volume desprezível. A outra extremidade do fio é sustentada pela mão do laboratorista. Quando o objeto é mergulhado no becker, o nível do líquido se eleva, alcançando a marca de 1500 mililitros, e a balança passa a indicar 5,92 kg. A figura abaixo ilustra dois momentos distintos da experiência.
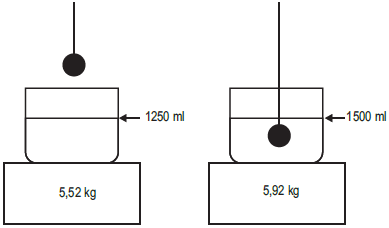
Nesse caso, a densidade do líquido, determinada corretamente pelo laboratorista, em g/cm3, é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container