Foram encontradas 36.174 questões.
A compreensão sobre os principais conceitos
referentes ao estudo da Química é importante
para situar o indivíduo dentro de um contexto
repleto de informações de relevância
inquestionável para a melhoria da qualidade de
vida e longevidade do ser humano, além de
contribuírem para a consecução do
conhecimento científico. Sobre alguns desses
conceitos e aspectos concernentes à Química, é
improcedente afirmar:
Provas
Questão presente nas seguintes provas
Sobre os fundamentos teóricos da Química, julgue os
itens a seguir como Verdadeiros (V) ou Falsos (F):
(__)Nem todas as reações químicas são reversíveis.
(__)Os alcanos são compostos que apresentam apenas carbono e hidrogênio em ligações simples, os mesmos não possuem grupos funcionais.
(__)A mudança de entalpia de uma reação é o calor absorvido ou liberado sob pressão constante durante uma reação.
Assinale a alternativa com a sequência CORRETA de cima para baixo.
(__)Nem todas as reações químicas são reversíveis.
(__)Os alcanos são compostos que apresentam apenas carbono e hidrogênio em ligações simples, os mesmos não possuem grupos funcionais.
(__)A mudança de entalpia de uma reação é o calor absorvido ou liberado sob pressão constante durante uma reação.
Assinale a alternativa com a sequência CORRETA de cima para baixo.
Provas
Questão presente nas seguintes provas
Um médico recebeu um paciente com um quadro grave de infecção do trato urinário e,
após exames, prescreveu um antibiótico em gotas. O medicamento deveria ser
administrado em quantidades de 4 mg por quilograma de massa corporal, não podendo,
entretanto, exceder 250 mg por dose. Sabendo que cada gota contém 10 mg de
antibiótico, o número de gotas que o paciente de 60 kg deve tomar é
Provas
Questão presente nas seguintes provas
Considere a fórmula molecular do paracetamol a seguir.

O paracetamol foi introduzido na terapêutica depois de uma descoberta acidental da acetanilida, sendo utilizado como medicamento desde 1878 até os dias atuais como analgésico e antipirético. O paracetamol apresenta
Provas
Questão presente nas seguintes provas
A partir das amostras expostas no quadro abaixo, o técnico em laboratório de química
deve identificar quais substâncias apresentam ligações iônicas.
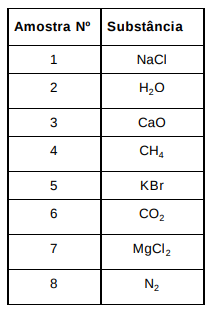
Sendo assim, o técnico deve identificar as amostras

Sendo assim, o técnico deve identificar as amostras
Provas
Questão presente nas seguintes provas
O técnico em laboratório de química precisa realizar um experimento de destilação simples. A vidraria necessária para a execução desse processo de separação é:
Provas
Questão presente nas seguintes provas
Para determinar a concentração de metais pesados, durante uma análise de amostras de
água de um rio, um laboratorista optou por utilizar a técnica de espectrometria de
absorção atômica (EAA). Essa técnica mede a
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
As fórmulas estruturais são representações gráficas que detalham a organização espacial
dos átomos em uma molécula e as ligações químicas entre eles. Elas são fundamentais
para entender a geometria molecular, as interações químicas e a polaridade das ligações.
Nesse sentido, analise, abaixo, as fórmulas estruturais de algumas substâncias químicas
e suas respectivas descrições.
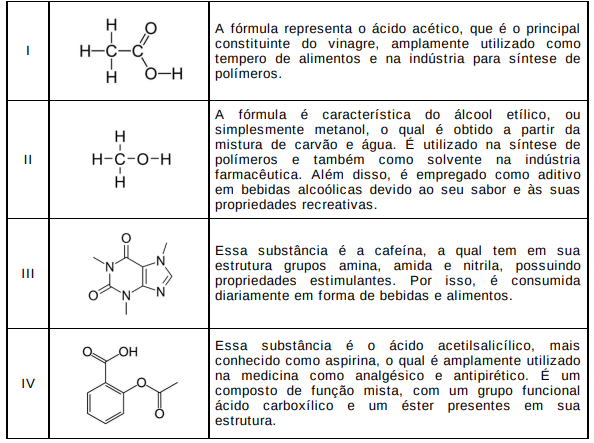
As fórmulas estruturais estão descritas corretamente em

As fórmulas estruturais estão descritas corretamente em
Provas
Questão presente nas seguintes provas
Durante um experimento de espectroscopia, um pesquisador observou que uma amostra
de composto orgânico absorve luz na região ultravioleta e visível do espectro
eletromagnético. Analise as afirmativas a seguir referentes ao processo de absorção
molecular nessa região.
I Quando a amostra absorve luz na região ultravioleta e visível, há um aumento da energia de radiação do feixe de luz.
II A absorção da luz ultravioleta e visível depende do número e do arranjo dos elétrons que constituem as moléculas de uma substância. Dessa forma, o pico de absorção pode ser relacionado com o tipo de ligação presente na amostra, possibilitando a identificação de seus grupos funcionais.
III A amostra absorve luz na região ultravioleta e visível, porque os átomos na molécula são ionizados pelos fótons de luz, resultando na emissão de radiação luminosa.
IV No caso de uma luz monocromática, a absorvância é diretamente proporcional à concentração das espécies absorventes na amostra.
Das afirmativas, estão corretas
I Quando a amostra absorve luz na região ultravioleta e visível, há um aumento da energia de radiação do feixe de luz.
II A absorção da luz ultravioleta e visível depende do número e do arranjo dos elétrons que constituem as moléculas de uma substância. Dessa forma, o pico de absorção pode ser relacionado com o tipo de ligação presente na amostra, possibilitando a identificação de seus grupos funcionais.
III A amostra absorve luz na região ultravioleta e visível, porque os átomos na molécula são ionizados pelos fótons de luz, resultando na emissão de radiação luminosa.
IV No caso de uma luz monocromática, a absorvância é diretamente proporcional à concentração das espécies absorventes na amostra.
Das afirmativas, estão corretas
Provas
Questão presente nas seguintes provas
Durante uma aula de química, um professor compartilhou com os estudantes algumas das
técnicas utilizadas para o balanceamento de equações químicas. Além disso, ele destacou a
relevância do processo de balanceamento, enfatizando não só o aspecto teórico mas também
a sua utilidade prática em procedimentos industriais e experimentações em laboratório. Como
parte final da aula, o docente propôs um exercício prático em que os alunos deveriam aplicar
o conhecimento adquirido para balancear duas equações químicas específicas, as quais
podem ser observadas abaixo.

Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container