Foram encontradas 36.167 questões.
O metal tungstênio, W (s), é produzido a partir do óxido de tungstênio(VI), WO3 (s), pela reação, em alta temperatura, desse óxido com hidrogênio, H2 (g). O outro produto dessa reação é a água no estado gasoso.
Volframita – mineral fonte de tungstênio

(https://mct.ufop.br/)
Sabendo que o volume molar de gás nas Condições Ambiente de Temperatura e Pressão (CATP) é igual a 25 L/mol, para cada mol de tungstênio que se forma nessa reação, o volume de hidrogênio que reage, medido nas CATP, é próximo de
Provas
Um raio de luz monocromática, propagando-se pelo ar, incide sobre um líquido em equilíbrio contido em um recipiente, é refratado e passa a propagar-se por esse líquido em uma direção inclinada de um ângulo !$ \alpha !$ em relação à superfície do líquido, conforme a figura.
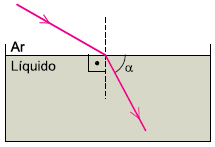
A tabela apresenta cinco líquidos que podem estar no interior desse recipiente e seus respectivos índices de refração absolutos.

Dos líquidos apresentados na tabela, aquele para o qual o ângulo !$ \alpha !$ assume o menor valor possui fórmula estrutural:
Provas
Considere a estrutura do polímero conhecido pela sigla PET (polietilenotereftalato).
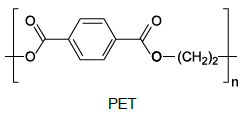
O exame dessa estrutura mostra que o PET é
Provas
O óxido de cério (CeO2), utilizado em catalisadores automotivos, é obtido pela reação entre cério metálico e oxigênio. Nessa reação, o número de oxidação do cério varia de para , sendo, portanto, o agente .
As lacunas do texto são preenchidas, respectivamente, por
Provas
Quando cianeto de hidrogênio, um gás extremamente tóxico, é borbulhado em água, ocorre a produção de uma solução aquosa de ácido cianídrico, que se ioniza conforme a equação:
HCN (aq) !$ \rightleftharpoons !$ H+ (aq) + CN– (aq)
Uma solução aquosa 0,2 mol/L de ácido cianídrico apresenta pH = 5 na temperatura de 25 ºC. A partir desse dado, pode-se estimar o valor da constante Ka desse ácido nessa temperatura. Esse valor é, aproximadamente,
Provas

(www.aviacaocomercial.net)
Para se calibrar o pneu do carro num posto de serviços, a recomendação é colocar cerca 30 PSI, sigla em inglês para a unidade de pressão “libra-força por polegada quadrada”. Para o pneu de um avião, que é preenchido com nitrogênio puro em vez de ar, a regulagem recomendada é cerca de 200 PSI à temperatura ambiente de 300 K. No entanto, no momento do pouso, essa pressão interna pode aumentar significativamente, como consequência do calor gerado pelo impacto e atrito com o solo e pela ação dos freios, com a temperatura podendo atingir 1 200 K.
(www.uol.com.br. Adaptado.)
Supondo que o volume do pneu não se altere, a pressão interna de nitrogênio no pneu durante o pouso pode atingir o valor de
Provas
A “barrilha leve”, carbonato de sódio (Na2CO3), é um produto de grande uso industrial, sendo também utilizado no tratamento da água de piscinas. A obtenção da barrilha leve envolve o processo Solvay, no qual dióxido de carbono gasoso (CO2) é borbulhado em uma solução aquosa que contém amônia (NH3) e cloreto de sódio (NaC!$ \ell !$), de acordo com a reação:
CO2 (g) + NH3 (aq) + Na+ (aq) + C!$ \ell !$ – (aq) + H2O (!$ \ell !$) →
→ NH4 + (aq) + HCO3 – (aq) + Na+ (aq) + C!$ \ell !$ – (aq)
A solução iônica resultante desse processo é resfriada de modo que apenas o bicarbonato de sódio, NaHCO3 (s), forma um precipitado, e os demais íons permanecem em solução. O NaHCO3 (s) é separado da mistura por filtração e submetido a aquecimento, decompondo-se e originando o carbonato de sódio, Na2CO3 (s).
Em princípio, como resultado do processo Solvay, seria possível obter várias substâncias iônicas por precipitação. Entretanto, nessa etapa, somente o bicarbonato de sódio sólido, NaHCO3 (s), se separa como precipitado. Isso ocorre porque, dentre as demais substâncias possíveis de serem formadas no processo Solvay, o NaHCO3 (s) é a substância iônica que apresenta a
Provas
“A composição química aproximada do basalto é de 43 a 47% de SiO2, 11 a 13% de Al2O3, 10 a 12% de CaO e 8 a 10% de MgO, além de outros óxidos que estão presentes em percentagens inferiores a 5%” (Schiavon, et al. 2007). O CaO e o MgO são óxidos classificados como básicos. Sobre os óxidos básicos, é correto afirmar que:
Provas
A figura abaixo representa três balões volumétricos idênticos e preenchidos até seus volumes nominais máximos de 50,00 mL com cada uma das soluções aquosas informadas nos rótulos.
Os balões estão identificados pelas letras A, B e C.

Analise as afirmativas abaixo, atribuindo (V) para as sentenças verdadeiras e (F) para as sentenças falsas.
( ) A solução contida no balão C é preparada dissolvendo-se 0,555 g de CaC!$ ell_2 !$ em água até o volume final de 50,00 mL.
( ) O balão C contém uma solução tampão.
( ) Ao misturar a solução do balão A com a solução do balão B, haverá uma reação exotérmica de neutralização.
( ) A solução contida no balão C possui íons cloreto na concentração 0,200 mol L-1.
( ) O pH da solução contida no balão B aumentará se a essa solução for adicionado NaOH.
( ) Se a solução contida no balão B for completamente utilizada em uma diluição para o volume final de 100,00 mL, a concentração nominal de HC!$ ell !$ na solução final será a metade da concentração da solução original.
( ) O número de mol de KNO3 contido na solução A será mantido constante, mesmo se todo o conteúdo do balão for misturado com 1,00 L de água pura.
( ) Se forem pipetados 5,00 mL da solução contida no balão C e diluídos para um volume final de 150,00 mL, será formada uma solução com concentração de CaC!$ ell_2 !$ 1,00x10-3 mol L1.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Sobre instrumentos frequentemente utilizados em laboratórios de química, analise as afirmativas abaixo e assinale a alternativa correta.
I. Muflas são fornos frequentemente utilizados para calcinar substâncias químicas sob a ação de temperaturas elevadas.
II. Dessecadores são receptáculos utilizados para armazenamento de substâncias e amostras sob condições de baixa umidade.
III. Rotaevaporadores são empregados para extrair e purificar compostos orgânicos obtidos em processos de síntese por meio da percolação em colunas de troca iônica.
IV. Refratômetros são empregados para medir a polarização da radiação eletromagnética promovida por substâncias orgânicas com centros quirais.
V. Medidores de ponto de fusão utilizam microbalanças para aferir a quantidade de gás produzida a partir da decomposição térmica de substâncias puras.
Provas
Caderno Container