Foram encontradas 1.090 questões.
No desenvolvimento de atividades laboratoriais, é importante utilizar os equipamentos de proteção para se evitar ou minimizar os riscos de acidente de trabalho. São exemplos de equipamentos de proteção individual (EPI) e equipamentos de proteção coletivo (EPC), respectivamente:
Provas
Como as reações envolvem a quebra e a formação de ligações, as respectivas velocidades dependem da natureza dos reagentes em si. No entanto, existem quatro fatores que permitem a variação das velocidades nas quais reações específicas ocorrem. Esses fatores são:
Provas
No equilíbrio, a velocidade na qual os produtos são formados a partir dos reagentes é igual à velocidade na qual os reagentes são formados a partir dos produtos. As reações podem atingir o equilíbrio em diferentes condições de concentração. Considere a reação abaixo como uma situação de equilíbrio e em seguida veja os gráficos com as possibilidades de concentrações.
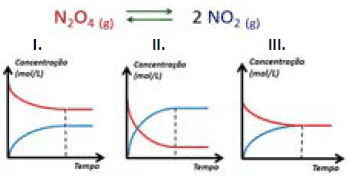
Baseado nessas informações, podemos afirmar CORRETAMENTE que quando atingido o equilíbrio:
Provas
O grupo funcional dos fenóis é a hidroxila (OH). É o mesmo grupo funcional dos álcoois. De acordo com os conhecimentos sobre funções orgânicas, analise os compostos abaixo a respeito dos álcoois e fenóis.
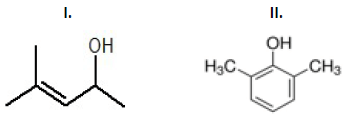
Segundo a IUPAC, União Internacional de Química Pura e Aplicada, a nomenclatura para os compostos I e II, respectivamente, será:
Provas
Energia de ativação (Ea) é a energia mínima que as moléculas devem possuir para reagir, ao se chocarem (isto é, para termos uma colisão efetiva).
Os gráficos I e II, a seguir, mostram exemplos de energias de ativação:
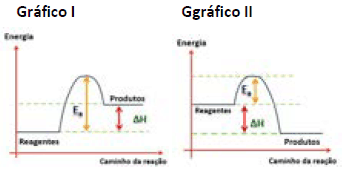
Conforme os gráficos acima, é CORRETO afirmar que:
Provas
O estudo da velocidade das reações químicas e dos fatores que influenciam nessa velocidade é chamada de cinética química. Logo abaixo, podemos observar 2 gráficos que variam as concentrações das substâncias em função do tempo:

Baseado nas informações sobre velocidade de reação, pode-se afirmar CORRETAMENTE que:
Provas
Segundo Arrhenius, nos estudos sobre as principais funções químicas inorgânicas, podemos destacar os ácidos, compostos em solução aquosa que se ionizam, produzindo como íon positivo apenas cátion hidrogênio (H+) e bons condutores de eletricidades. E as bases, compostos que, por dissociação iônica, liberam, como íon negativo, apenas o ânion hidróxido (OH-) e também bons condutores de eletricidades.
Sobre os conhecimentos de ácidos-base, analise as afirmativas abaixo:
I. O gás HCl ao ser borbulhado em água sofre ionização tornando o meio ácido com liberação de H-.
II. Se consideradas concentrações idênticas entre o H2SO4 e o H2SO3, a substância que apresenta maior acidez é o H2SO4.
III. As bases formadas com elementos da família 1A (metais alcalinos) são consideradas bases fortes e cujo grau de dissociação é praticamente 100% em água.
IV. As bases formadas com elementos da família 2A (metais alcalinos - terrosos) são consideradas bases muito solúveis em água.
Nas afirmativas citadas, pode-se afirmar CORRETAMENTE que:
Provas
Ligação iônica é a força que mantém os íons unidos, depois que um átomo cede definitivamente um, dois ou mais elétrons para outro átomo. Em geral, é bastante forte e mantém os íons firmemente “presos” no reticulado. Por isso, os compostos iônicos são sólidos e, em geral, têm ponto de fusão e ponto de ebulição elevados. Quando se comparam as espécies químicas CH4, CaCO3, NH3, NaCl e Na2SO4, pode-se afirmar que os átomos estão unidos por ligações iônicas, somente, nos compostos:
(Dados: 1H1; 6C12; 7N14; 8O16; 11Na23; 16S32; 17Cl35; 20Ca40)
Provas
Um átomo adquire estabilidade quando possui 8 elétrons na camada eletrônica mais externa, ou 2 elétrons quando possui apenas a camada K. Na prática, quando dois átomos vão se unir, eles “trocam elétrons entre si” ou “usam elétrons em parceria”, procurando atingir a configuração eletrônica de um gás nobre. Surgem daí os três tipos comuns de ligação química – iônica, covalente e metálica. A ligação covalente, por exemplo, ocorre quando os dois átomos têm a tendência de ganhar elétrons. Com base nos conhecimentos sobre Ligações, jugue os itens abaixo em (V) verdadeiro ou (F) falso:
(Dados: 1H1; 17Cl35; 8O16)9
( ) Na reação de formação da molécula de hidrogênio (H2) há união entre dois átomos do elemento hidrogênio (H) por meio de uma ligação iônica. ( ) Na molécula (Cl2), há um par de elétrons compartilhado pelo os dois átomos de cloro, constituindo uma ligação simples, denominada pi (!$ \pi !$).
( ) Na formação de uma ligação dupla entre os átomos, que é indicada por dois traços, como na representação, O=O, é constituída por uma ligação do tipo sigma (!$ σ !$) e a outra do tipo pi (!$ \pi !$).
( ) Em geral, os pontos de fusão e ebulição das substâncias moleculares são maiores que os das substâncias iônicas.
De acordo com as afirmativas acima, a alternativa CORRETA de cima para baixo é:
Provas
Tanto no laboratório quanto na indústria química, é muito importante calcular as quantidades das substâncias que são utilizadas ou produzidas nas reações químicas. Aliás, esse cálculo é importante também em nosso cotidiano. Ao preparar um bolo, por exemplo, devemos misturar os ingredientes (farinha, ovos, açúcar etc.) numa proporção adequada. A produção da amônia, o NH3, por exemplo, acontece por meio da reação do gás hidrogênio, H2, com o gás nitrogênio, N2, a alta temperatura e sob alta pressão, conforme equação química não balanceada mostrada abaixo:
N2 (g) + H2 (g) → NH3 (g)
Para que 340 g de amônia possa ser produzida, utilizando o gás hidrogênio em excesso, seria necessário consumir:
(Dados: H = 1,00g/mol; N = 14,00g/mol)
Provas
Caderno Container