Foram encontradas 612 questões.
A informação a seguir se refere a questão abaixo:
A maior parte da produção industrial do magnésio é obtida a partir da água do mar, onde o elemento químico magnésio se encontra na forma de íons Mg2+(aq), em concentração média de 1,3 g.L–1. O processo segue as seguintes etapas:
I. Precipitação de Mg(OH)2 por adição de cal viva.
II. Conversão a MgC!$ \ell !$2 por adição de HC!$ \ell !$.
III. Eletrólise ígnea do MgC!$ \ell !$2.
Sabendo que a constante de Faraday é 9,65×104 C.mol–1, a quantidade de carga elétrica necessária para obter todo o magnésio contido em 1 m3 de água do mar é de, aproximadamente,
Provas
Considere a estrutura a seguir:
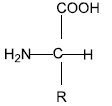
A estrutura química representada é a fórmula geral dos . A formação de cadeia polimérica dessas estruturas se dá por , formando um .
As lacunas são preenchidas, correta e respectivamente, por:
Provas
A reação a seguir representa uma reação de substituição nucleofílica.
2 CH3OH + (CH3)3 CC!$ \ell !$ → (CH3)3 COCH3 + CH3OH2 + + C!$ \ell !$–
Nessa reação, o nome do reagente oxigenado e a função orgânica do produto não iônico são, respectivamente,
Provas
A equação representa uma etapa das reações do processo Claus, técnica utilizada na remoção do enxofre presente no petróleo.
2 H2S(g) + SO2(g) !$ \rightleftharpoons !$ 3 S(s) + 2 H2O(g); ΔH < 0
Ocorre o deslocamento do equilíbrio no sentido dos produtos quando, nesse sistema,
Provas
O equilíbrio 2SO2(g) + O2(g) !$ \rightleftharpoons !$ 2SO3(g), uma das etapas de formação do ácido sulfúrico, apresentou os seguintes valores de pressões parciais à temperatura de 726 ºC.
|
PSO2 (bar) |
PO2 (bar) |
PSO3 (bar) |
|
0,70 |
0,40 |
0,080 |
A constante de equilíbrio para esse sistema tem valor de
Provas
Considere as moléculas apolares a seguir:
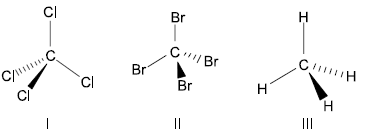
A ordem crescente de temperatura de ebulição dessas substâncias e a molécula que apresenta maior polarizabilidade, são, respectivamente,
Provas
Apesar da molécula de NO ser altamente reativa, ela desempenha um papel importante na fisiologia humana, tanto que, em 1998, valeu o prêmio Nobel de Medicina para três pesquisadores que descobriram a sua função “sinalizadora” no sistema cardiovascular.
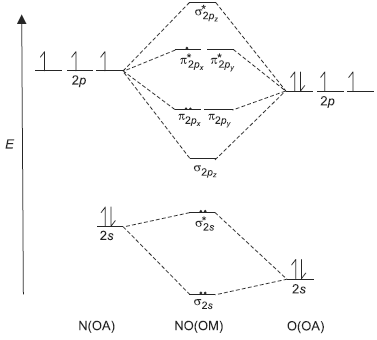
Tendo como base o diagrama do orbital molecular apresentado, conclui-se que a ordem de ligação para essa molécula é:
Provas
A dissolução em água de um comprimido antiácido efervescente forma alguns equilíbrios químicos, entre eles, o sistema carbonato/bicarbonato representado a seguir:
CO3 2–(aq) + H2O(!$ \ell !$) !$ \rightleftharpoons !$ HCO3 –(aq) + OH–(aq)
HCO3 –(aq) + H2O(!$ \ell !$) !$ \rightleftharpoons !$ H2CO3(aq) + OH–(aq)
H2CO3(aq) !$ \rightleftharpoons !$ CO2(g) + H2O(!$ \ell !$)
A solução tampão formada nesse sistema envolve o par conjugado ácido-base, nessa ordem:
Provas
A reação do sódio metálico com etanol é uma forma mais segura de eliminação de resíduos do metal, quando comparada sua reação com a água, e pode ser representada pela equação não balanceada:
Na + CH3CH2OH → CH3CH2ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
Provas
Para a determinação da fórmula mínima de um hidrocarboneto foi realizada a análise por combustão de 0,580 g de substância, obtendo-se 1,75 g de CO2 e 0,920 g de H2O. Chegou-se à conclusão que a fórmula mínima desse hidrocarboneto é
Provas
Caderno Container