Foram encontradas 100 questões.
Escolha a única alternativa correta, dentre as opções apresentadas, que responde ou completa cada questão, assinalando-a, com caneta esferográfica de tinta azul ou preta, no Cartão de Respostas.
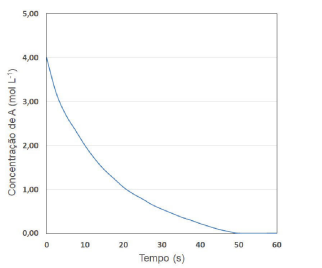
Os conceitos da cinética química são de grande importância para o desenvolvimento de produtos militares, particularmente explosivos e munições. Considere o gráfico a seguir, que representa a variação da concentração da espécie A em função do tempo na reação genérica representada pela equação A → 2 B. A velocidade de formação da substância B, em mol L-1s -1, nos primeiros 10 segundos de reação, é de aproximadamente
Provas
Escolha a única alternativa correta, dentre as opções apresentadas, que responde ou completa cada questão, assinalando-a, com caneta esferográfica de tinta azul ou preta, no Cartão de Respostas.
Nas Olimpíadas de Paris 2024, os atletas tiveram que se prevenir com relação ao uso de determinados medicamentos. O tramadol, um analgésico opioide, é indicado no tratamento de dores moderadas ou intensas. Seu uso foi proibido pela Agência Mundial Antidoping durante os Jogos Olímpicos e outras competições. A substância tramadol, na verdade, corresponde a uma mistura de compostos com estruturas parecidas, todavia com características assimétricas. Considere as estruturas do (1R,2R)-tramadol e do (18,2S)-tramadol, representadas a seguir.
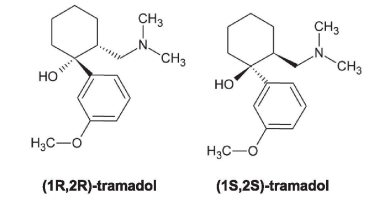
Sobre a fórmula e estrutura do tramadol, são feitas as seguintes afirmativas:
|- A fórmula molecular do (1R,2R)-tramadol é C16H25NO2.
II- O (18,2S)-tramadol apresenta em sua estrutura 6 (seis) carbonos com hibridização sp2.
Il- O (1R,2R)-tramadol apresenta grupos funcionais representativos das funções orgânicas ácido carboxílico e amida.
IV- Os dois compostos representados são isômeros ópticos.
Das afirmativas feitas, estão corretas apenas
Provas
O filme Oppenheimer reavivou o assunto sobre as bombas nucleares lançadas no Japão no final da Segunda Guerra Mundial. As bombas, nomeadas de Little Boy e Fat Man, eram baseadas no processo de fissão nuclear dos elementos urânio-235 e plutônio-239, respectivamente. Algumas das equações das reações nucleares envolvidas nesses processos são apresentadas abaixo, onde as incógnitas x e y representam a quantidade de nêutrons (n).
\( \begin{smallmatrix} 135\\ 92 \end{smallmatrix}U + n → \begin{smallmatrix} 142\\ 56 \end{smallmatrix}Ba + \begin{smallmatrix} 91\\ 36 \end{smallmatrix}Kr + x n \)
\( \begin{smallmatrix} 239\\ 94 \end{smallmatrix}Pu + n → \begin{smallmatrix} 97\\ 39 \end{smallmatrix} + \begin{smallmatrix}Y 138\\ 55 \end{smallmatrix}Cs + yn \)
Sobre os assuntos tratados no texto acima, são feitas as seguintes afirmativas:
I - Os valores das incógnitas x e y são, respectivamente, 3 e 5.
II - O processo de fissão nuclear é a junção de dois núcleos instáveis gerando um núcleo mais estável, liberando grande quantidade de energia.
III - A massa crítica ou massa físsil é a maior quantidade de matéria necessária para que ocorra a reação em cadeia.
IV - O número 239 no elemento plutônio significa que o átomo apresenta 239 nêutrons.
V - O número 92 no elemento urânio significa que o átomo apresenta 92 prótons.
Das afirmativas feitas, estão corretas apenas
Provas
Em química orgânica, compostos que possuem o grupo funcional nitro (N02) têm grande potencial para serem utilizados como explosivos. Um explosivo é um composto, ou mistura de compostos, que, sob ação de uma causa térmica ou mecânica, se transforma muito rapidamente, total ou parcialmente, em um grande volume de gases com liberação de calor. A expansão desses gases é responsável pelo trabalho de destruição, pois gera pressões muito altas. Teoricamente, os gases produzidos na explosão de compostos nitrados são CO2, H2O e N2, no entanto, empiricamente, também se formam outros gases.
O hexogênio (RDX), explosivo muito utilizado para fins militares, se decompõe de acordo com a equação:
C3H6N3(NO2)3 → 2 CO2(g) + CO(g) + H2O (g) + 3 N2 (g)
Considerando um comportamento ideal dos gases e que, à temperatura de 727 ºC, a detonação de 2,22 g de RDX libera um volume total de 14,76 L de gases formados, a pressão total atingida será de
Dados: Constante dos gases ideais: R = 0,082 atm L mor1 K-1
Relação de temperatura: T Kelvin (K) = T celsius (ºC) + 273
Provas
Escolha a única alternativa correta, dentre as opções apresentadas, que responde ou completa cada questão, assinalando-a, com caneta esferográfica de tinta azul ou preta, no Cartão de Respostas.
Para proteger um metal I da corrosão, pode-se utilizar outro metal II que apresenta uma tendência maior de perder elétrons (menor potencial de redução). Esse metal II se oxida e evita a corrosão do metal I, sendo, por isso, chamado de metal de sacrifício ou ânodo de sacrifício.
(Modificado de USBERCO, João; SALVADOR, Edgard. Química. 12. ed. São Paulo: Editora Saraiva, 2009, Vol.2, p. 295.)


Baseado na proteção contra a corrosão da tubulação e considerando o esquema e os processos eletroquímicos envolvidos, são feitas as seguintes afirmativas:
| - O metal níquel pode ser utilizado como ânodo de sacrifício (metal II) caso a tubulação (metal I) seja de cobre.
II - O ânodo de sacrifício (metal II) sofre uma reação de redução, aumentando sua massa ao longo do tempo.
III - O metal cobre pode ser utilizado como ânodo de sacrifício (metal II) caso a tubulação (metal I) seja de ferro.
IV - O metal usado no eletrodo de sacrifício (metal II) será o agente oxidante na reação eletroquímica.
V - Caso a tubulação (metal 1) seja de ouro, o ânodo de sacrifício (metal II) pode ser constituído por qualquer um dos outros metais apresentados na lista acima.
Das afirmativas feitas, estão corretas apenas
Provas
O diborano (B2H6) é um hidreto de boro altamente reativo, sendo considerado um possível
combustível e propelente de foguetes em programas espaciais. O cálculo da energia envolvida na
síntese de um mol de diborano pode ser feito utilizando-se a lei de Hess. Considere as equações
das seguintes reações:
(1) 2 B (s) + 3/2 02 (g) - B2O3 (s) + 1273 kJ
(2) B2Hs (g) + 3 02 (g) - 2035 kJ - B2O3 (s) + 3 H2O (g)
(3) H2 (g) + 1/2 02 (g) - H2O (g) + 242 kJ
Com base nessas reações e nos calores envolvidos nos processos, são feitas as seguintes afirmações:
I - A reação número dois é exotérmica e o AH = - 2035 kJ.
II - As três reações são exotérmicas.
III - A entalpia de formação do diborano é +36 kJ mor1.
Das afirmativas feitas, está(ão) correta(s) apenas
Provas
Escolha a única alternativa correta, dentre as opções apresentadas, que responde ou completa cada questão, assinalando-a, com caneta esferográfica de tinta azul ou preta, no Cartão de Respostas.
Os lenços umedecidos são um produto criado na década de 1950 nos EUA e que, de certa forma, revolucionaram os cuidados de higiene pessoal, especialmente em relação aos bebês e às crianças pequenas. Na composição destes produtos, a água é o componente majoritário, mas também são encontradas diversas outras substâncias como o etilenoglicol, o propilenoglicol e o 3-(4-tercbutilfenil)-2-metilpropanal, representadas abaixo:
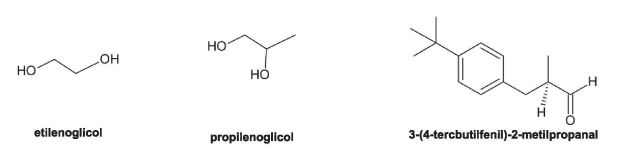
Em relação às substâncias citadas, são feitas as seguintes afirmações:
I- A adição dessas substâncias à água deixa a temperatura de congelamento da mistura menor do que a temperatura de congelamento da água pura.
II- O 3-4-tercbutilfenil)-2-metilpropanal possui a menor solubilidade em água em comparação ao etilenoglicol e ao propilenoglicol.
III- Devido à presença de grupos hidroxila em sua estrutura, a molécula de etilenoglicol não é capaz de estabelecer interações intermoleculares do tipo ligações de hidrogênio.
IV-Considerando-se uma mesma quantidade de massa, a substância que apresentará a maior quantidade de átomos de oxigênio será o propilenoglicol.
V- A substância 3-(4-tercbutilfenil)-2-metilpropanal possui 2 (dois) isômeros ópticos.
Das afirmativas feitas, estão corretas apenas
Provas
Uma das possibilidades químicas de obtenção de fogo é a reação entre permanganato de potássio (KMnO4) e propan-1,2,3-triol, que libera energia térmica suficiente para gerar uma chama, cuja reação pode ser descrita da seguinte forma:
14 KMnO4 + 4 propan-1,2,3-triol → 7 K2CO3 + 7 Mn2O3 + 16 H2O
Sobre os assuntos tratados no texto acima, são feitas as seguintes afirmativas:
I - O propan-1,2,3-triol possui a fórmula molecular C3H8O3.
II - A reação entre permanganato de potássio e propan-1,2,3-triol é endotérmica.
III - O permanganato de potássio é o agente oxidante da reação.
IV - De acordo com a teoria da repulsão dos pares eletrônicos da camada de valência, a geometria molecular do dióxido de carbono é linear.
V - O número de oxidação do átomo de manganês no KMnO4 é +7.
Das afirmativas feitas, estão corretas apenas
Provas
Em 1912, o químico alemão Fritz Haber (1868-1934) desenvolveu um processo para sintetizar amônia (NH3) diretamente a partir de nitrogênio (N2) e hidrogênio (H2). O processo é algumas vezes chamado de Haber-Bosch também para homenagear Karl Bosch, engenheiro que desenvolveu o equipamento para a produção industrial de amônia. Na Primeira Guerra Mundial, para a produção de explosivos, a Alemanha dependia de insumos à base de nitrogênio de outros países. Bloqueios navais cortaram esse suprimento. Entretanto, pela fixação de nitrogênio do ar, a Alemanha foi capaz de continuar a produzir explosivos. Especialistas estimaram que a Primeira Guerra Mundial teria terminado antes de 1918 se não fosse o processo de Haber. (Adaptado de: BROWN, T.L.; LEMAY, H.E.; BURSTEN, BE. Química, a ciência Central. São Paulo: Prentíce Hall, 2005, 9 ed, p . 534.)
O processo de Haber, ou processo de Haber-Bosch, promove a formação de amônia a partir da reação elementar entre nitrogênio e hidrogênio gasosos. Esta reação pode se apresentar na forma de um equilíbrio químico, conforme a equação: 1 N2 (g) + 3 H2 (g) ~ 2 NH3 (g). Sobre esse equilíbrio, analise as afirmativas abaixo.
I - O aumento da pressão parcial de N2 desloca o equilíbrio no sentido de formar mais H2.
II - Em determinada condição, se a concentração de N2 for de 10 mol L-1, de H2 for de 1 mol L-1 e de NH3 for de 2 mol L-1, o quociente da reação (Qc) será de 0,0125.
III - O aumento da pressão total aumenta a formação de NH3.
IV - A adição de gás H2, a volume constante, desloca o equilíbrio químico no sentido de formar mais NH3.
Das afirmativas feitas, estão corretas apenas
Provas
Escolha a única alternativa correta, dentre as opções apresentadas, que responde ou completa cada questão, assinalando-a, com caneta esferográfica de tinta azul ou preta, no Cartão de Respostas.
Em atividades militares de campo, podem ser usados aquecedores químicos sem chama para o aquecimento de rações operacionais. O óxido de cálcio — CaO — é um dos principais produtos químicos aproveitados nesses aquecedores. Esse composto químico reage com a água, gerando como produto o hidróxido de cálcio — Ca(OH)2, — além de grande quantidade de calor. Por ser extremamente exotérmico, esse processo pode ser empregado como aquecedor químico para esquentar rações operacionais em atividades militares.
Para o preparo do aquecedor químico sem chamas, cada um dos 50 soldados de um pelotão levou consigo um pote contendo 140 g de óxido de cálcio, com 80 % de pureza. Considerando-se o consumo total do reagente de todos os soldados do pelotão e a reação completa do óxido de cálcio com a água, a massa de produto gerada nessa reação foi de
Provas
Caderno Container