Foram encontradas 3.020 questões.
De acordo com a RDC Nº 512/21, sobre o item apresentação dos resultados analíticos, avalie se são verdadeiras (V) ou falsas (F) as afirmativas abaixo, no que se
refere ao que deve ser incluído no documento emitido pelo
laboratório:
I. Identificação do método usado.
II. Dados referentes aos desvios ocorridos apenas durante a execução da análise, quando aplicável.
III. Dados de calibração/qualificação dos equipamentos utilizados nos testes executados.
As afirmativas I, II e III são respectivamente:
I. Identificação do método usado.
II. Dados referentes aos desvios ocorridos apenas durante a execução da análise, quando aplicável.
III. Dados de calibração/qualificação dos equipamentos utilizados nos testes executados.
As afirmativas I, II e III são respectivamente:
Provas
Questão presente nas seguintes provas
De acordo com a norma ABNT NBR ISO/IEC
17025:2017, certificados de calibração devem incluir as
informações a seguir, a menos que algo diferente tenha
sido acordado com o cliente:
Provas
Questão presente nas seguintes provas
Baseado na norma ABNT NBR ISO/IEC 17025:2017,
no que se refere à rastreabilidade metrológica, observe as
afirmativas abaixo:
I. O laboratório deve assegurar que seus resultados de medição sejam rastreáveis ao Sistema Internacional de Unidades (SI).
II. O laboratório deve manter os dados de rastreabilidade metrológica por no mínimo 3 anos.
III. A tendência de um equipamento calibrado não precisa ser considerada para difundir a rastreabilidade metrológica aos resultados de medição.
IV. Laboratórios que realizam alguma etapa da cadeia de rastreabilidade precisam fornecer evidência de sua competência técnica.
V. BIPM, OIML, ILAC e INMETRO emitem a Declaração Conjunta sobre Rastreabilidade Metrológica que traz orientações específicas sobre quando há necessidade de se demonstrar a aceitabilidade internacional da cadeia de rastreabilidade metrológica.
Sobre as afirmativas acima, pode-se dizer que:
I. O laboratório deve assegurar que seus resultados de medição sejam rastreáveis ao Sistema Internacional de Unidades (SI).
II. O laboratório deve manter os dados de rastreabilidade metrológica por no mínimo 3 anos.
III. A tendência de um equipamento calibrado não precisa ser considerada para difundir a rastreabilidade metrológica aos resultados de medição.
IV. Laboratórios que realizam alguma etapa da cadeia de rastreabilidade precisam fornecer evidência de sua competência técnica.
V. BIPM, OIML, ILAC e INMETRO emitem a Declaração Conjunta sobre Rastreabilidade Metrológica que traz orientações específicas sobre quando há necessidade de se demonstrar a aceitabilidade internacional da cadeia de rastreabilidade metrológica.
Sobre as afirmativas acima, pode-se dizer que:
Provas
Questão presente nas seguintes provas
Nos estudos farmacocinéticos pré-clínicos do 25a, um promissor novo diurético, da classe dos inibidores de transportadores de ureia, a proporção de ligação da substância a proteínas plasmáticas de ratos Sprague-Dawley (SD) e de
humanos foi avaliada por microdiálise. 400 µL de plasma contendo 50, 500 e 2500 ng mL-1 de 25a foram depositados
nas bolsas de diálise (lado do plasma) e as bolsas foram colocadas em tubos contendo 4 mL de tampão de diálise (lado
do tampão). Após agitação e incubação a 37±1°C por 5 h, alíquotas de 50 µL foram tomadas de ambos os lados (lado
do plasma e lado do tampão), diluídas a 100 µL e acrescidas de 600µL de acetonitrila (contendo 10 ng mL-1 de padrão
interno) para precipitação das proteínas e subsequente análise por cromatografia líquida acoplada à espectrometria de
massas sequencial (LC–MS/MS).
A proporção de ligação da substância a proteínas plasmáticas (%) foi calculada como 100% x (1- Concentração(lado do tampão)/Concentração(lado do plasma) ) e os resultados encontram-se na tabela abaixo.

Observe as afirmativas a seguir, em relação à determinação in vitro da ligação do 25a a proteínas plasmáticas:
I – O valor médio de ligação a proteínas plasmáticas do 25a no plasma humano e de rato foi de 38,8% – 44,1% e 61,4% – 64,5%, respectivamente, indicando uma ligeira diferença entre as espécies, enquanto a ligação a proteínas plasmáticas do 25a em ambas as matrizes de plasma foi relativamente baixa a moderada em comparação com a substância utilizada como composto de referência (varfarina) (98,5%).
II – Considerando que a ligação a proteínas plasmáticas do 25a em plasma humano foi relativamente baixa, esse resultado indica que a droga é pouco eficiente em atravessar as membranas celulares ou se difundir.
III – A ligação a proteínas plasmáticas em cada nível de concentração não mostrou diferenças significativas (p > 0,05, teste t de Student), indicando que a ligação do 25a com as proteínas plasmáticas independe da concentração.
Das afirmativas acima, apenas:
A proporção de ligação da substância a proteínas plasmáticas (%) foi calculada como 100% x (1- Concentração(lado do tampão)/Concentração(lado do plasma) ) e os resultados encontram-se na tabela abaixo.

Observe as afirmativas a seguir, em relação à determinação in vitro da ligação do 25a a proteínas plasmáticas:
I – O valor médio de ligação a proteínas plasmáticas do 25a no plasma humano e de rato foi de 38,8% – 44,1% e 61,4% – 64,5%, respectivamente, indicando uma ligeira diferença entre as espécies, enquanto a ligação a proteínas plasmáticas do 25a em ambas as matrizes de plasma foi relativamente baixa a moderada em comparação com a substância utilizada como composto de referência (varfarina) (98,5%).
II – Considerando que a ligação a proteínas plasmáticas do 25a em plasma humano foi relativamente baixa, esse resultado indica que a droga é pouco eficiente em atravessar as membranas celulares ou se difundir.
III – A ligação a proteínas plasmáticas em cada nível de concentração não mostrou diferenças significativas (p > 0,05, teste t de Student), indicando que a ligação do 25a com as proteínas plasmáticas independe da concentração.
Das afirmativas acima, apenas:
Provas
Questão presente nas seguintes provas
A avaliação da ligação à proteína plasmática de uma
substância candidata ao tratamento do mieloma múltiplo
foi realizada pelo método RED (Rapid Equilibium Dyalisis).
Foram utilizados plasma de rato, do cão e humano, preparando-se amostras nas concentrações de 20, 60 e 200ng/mL. A determinação do composto de interesse no plasma
e tampão, após 4h de equilíbrio, foi feita com um método
de cromatografia a líquido de ultra eficiência acoplada a
espectrometria de massa Triplo Quadrupolo (TQP), com o
limite inferior de quantificação (LIQ) de 0,2 ng/mL. Em todas
as condições testadas a concentração no tampão foi menor
que LIQ. A partir desses resultados pode-se concluir que:
Provas
Questão presente nas seguintes provas
A determinação do log P é um ensaio fundamental na
predição de propriedades farmacocinéticas de substâncias
candidatas a fármacos. Existem vários procedimentos
experimentais para essa determinação, sendo que a organização para cooperação e desenvolvimento econômico
(OCDE) estabeleceu parâmetros para determinação do log
P por cromatografia a líquido. Leia as afirmativas abaixo
sobre esses parâmetros:
I. Devem-se utilizar colunas de troca catiônica para a determinação do valor de log P.
II. Deve ser feita uma calibração com substâncias com valor de log P conhecido, utilizando-se valores de retenção na coluna cromatográfica para a determinação do log P.
III. O coeficiente de correlação entre os valores de log P de substâncias conhecidas e a retenção deve ser no mínimo 0,99 para considerar o ensaio valido.
IV. O ideal é a determinação do valor de log P por interpolação aos valores dos padrões.
Das afirmativas acima, estão corretas apenas:
I. Devem-se utilizar colunas de troca catiônica para a determinação do valor de log P.
II. Deve ser feita uma calibração com substâncias com valor de log P conhecido, utilizando-se valores de retenção na coluna cromatográfica para a determinação do log P.
III. O coeficiente de correlação entre os valores de log P de substâncias conhecidas e a retenção deve ser no mínimo 0,99 para considerar o ensaio valido.
IV. O ideal é a determinação do valor de log P por interpolação aos valores dos padrões.
Das afirmativas acima, estão corretas apenas:
Provas
Questão presente nas seguintes provas
A substância (1), mostrada abaixo, é um candidato a novo fármaco para o tratamento de alguns tipos de tumor.
No processo de desenvolvimento dessa droga foram estudados os produtos de biotransformação em hepatócitos de
diferentes espécies. A técnica utilizada foi a cromatografia a líquido de ultra eficiência acoplada a um espectrômetro de
massa Q-Tof. Não houve diferença no perfil dos metabolitos formados, independentemente do hepatócito utilizado. Na
tabela abaixo são mostrados os tempos de retenção (tR) de cada pico observado, as fórmulas moleculares obtidas para
cada um, com os erros associados.
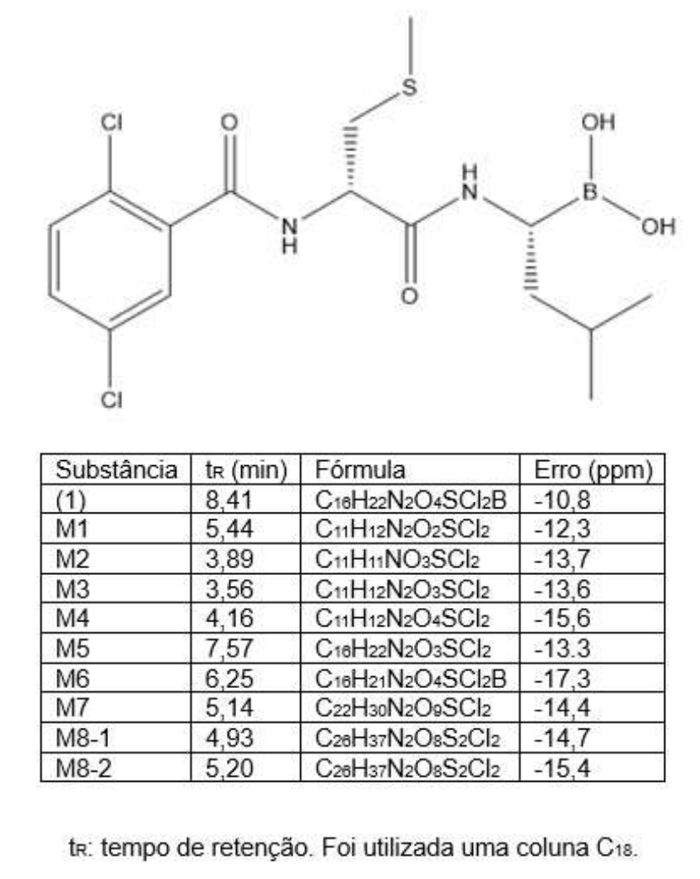
Analisando esses dados, a alternativa errada sobre os metabolitos formados é

Analisando esses dados, a alternativa errada sobre os metabolitos formados é
Provas
Questão presente nas seguintes provas
Produtos naturais são uma importante fonte para o desenvolvimento de novos fármacos; a avaliação da farmacocinética de compostos naturais em modelos animais de ajuda no desenvolvimento de análogos sintéticos com propriedades
superiores. Abaixo é mostrado o efeito sobre a biodisponibilidade de alguns marcadores, após a administração por 14
dias em ratos, de um composto natural.
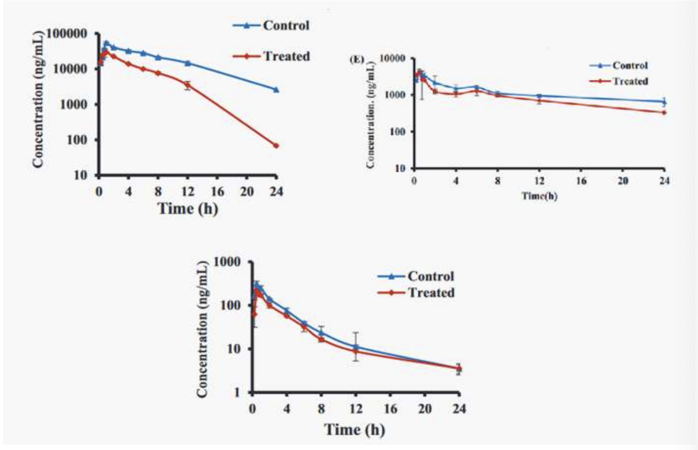
Superior à esquerda: efeito sobre a biodisponibilidade de um marcador para CYP1A2; superior à direita: efeito sobre a biodisponibilidade de marcador do CYP2E1; inferior: efeito sobre a biodisponibilidade de marcador da isoforma CYP3A1. Grupo controle identificado com triangulo e grupo tratado com o produto natural identificado com losango. Observando esses resultados pode-se concluir que:

Superior à esquerda: efeito sobre a biodisponibilidade de um marcador para CYP1A2; superior à direita: efeito sobre a biodisponibilidade de marcador do CYP2E1; inferior: efeito sobre a biodisponibilidade de marcador da isoforma CYP3A1. Grupo controle identificado com triangulo e grupo tratado com o produto natural identificado com losango. Observando esses resultados pode-se concluir que:
Provas
Questão presente nas seguintes provas
O estudo da biodisponibilidade por via oral é um parâmetro importante na farmacocinética não clínica. É importante que
sejam utilizadas as mesmas espécies/linhagens usadas em outros ensaios, como, por exemplo, no ensaio de potência.
Abaixo são mostradas as curvas de biodisponibilidade oral (PO) de um candidato a fármaco, em camundongos (superior)
e em cães (inferior). A biodisponibilidade por via endovenosa (IV) também foi determinada.
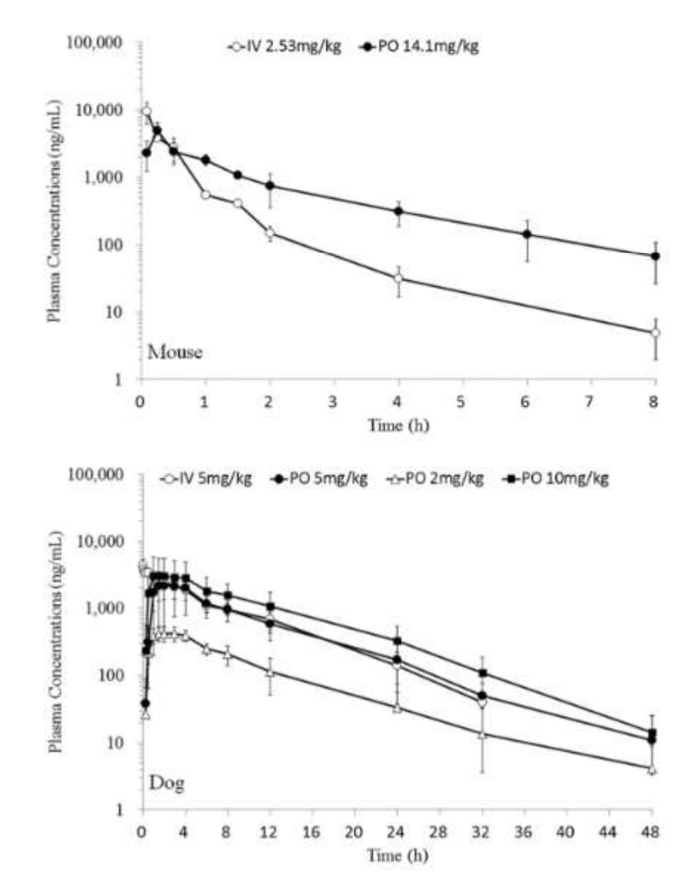
Observando esses resultados pode-se concluir que:

Observando esses resultados pode-se concluir que:
Provas
Questão presente nas seguintes provas
A estabilidade frente às frações microssomal e S9 é um ensaio que ajuda a estimar a estabilidade de substâncias
candidatas a fármaco a processos de biotransformação. Abaixo são mostrados resultados da estabilidade de um candidato
a fármaco, frente às frações microssomais e S9 de cinco diferentes espécies. Os valores apresentados são o tempo de
meia vida(t1/2) em minutos. Foi utilizado material de macacos cynomolgus.
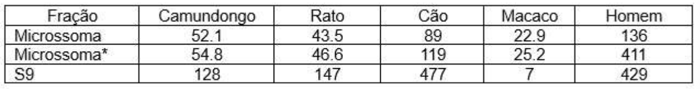
*Nessa condição a atividade flavina monoxigenase (fmo) foi inativada.
Avalie as afirmativas abaixo:
I. Pode-se observar claramente que a substância estudada é pouco biotransformada por enzimas fase 2 em todas as espécies.
II. A inativação da fmo afeta radicalmente a taxa de biotransformação em todas as espécies.
III. Esses resultados indicam uma maior estabilidade metabólica no homem em relação às demais espécies.
Das afirmativas acima:

*Nessa condição a atividade flavina monoxigenase (fmo) foi inativada.
Avalie as afirmativas abaixo:
I. Pode-se observar claramente que a substância estudada é pouco biotransformada por enzimas fase 2 em todas as espécies.
II. A inativação da fmo afeta radicalmente a taxa de biotransformação em todas as espécies.
III. Esses resultados indicam uma maior estabilidade metabólica no homem em relação às demais espécies.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container