Foram encontradas 1.245 questões.
Observe o sistema em que KC representa sua constante de equilíbrio em função da concentração:
A (aq) + B (aq) → AB (aq) KC = 4,0.
Foram preparadas cinco soluções em recipientes numerados, cujas concentrações iniciais de A, B e AB foram calculadas, como mostra a tabela a seguir:
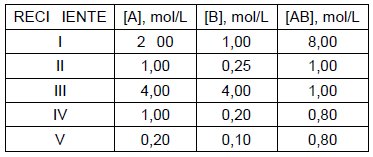
Dessa forma, a concentração inicial de AB irá aumentar no recipiente
Provas
Com a construção de aparelhos mais avançados para obter os espectros, foi possível perceber que eles apresentam uma estrutura fina, ou seja, algumas das linhas verificadas por Bohr são compostas de duas ou mais linhas muito próximas. Para explicar esta multiplicidade das raias espectrais verificadas experimentalmente, há exatos cem anos, o físico alemão Arnold Sommerfeld (1868-1951) deduziu algumas equações semelhantes às de Bohr. O enunciado que diz respeito a essa descoberta de Sommerfeld é
Provas
Considerando átomos que, no estado fundamental, têm elétrons distribuídos nos orbitais 1s, 2s, 2p, 3s e 3p, dos quais apenas dois desses elétrons são desemparelhados, eles podem apresentar os seguintes números atômicos:
Provas
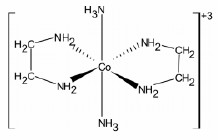
Para o íon complexo de fórmula abaixo, pode-se afirmar CORRETAMENTE que
Provas
As constantes de equilíbrio nos íons complexos [Ni(NH3)6]2+ e [Ni(en)3]2+ são, respectivamente, 4.108 e 2.1018, sendo “en” o ligante H2NCH2CH2NH2. Face a isso, é CORRETO afirmar que
Provas
Considere a equação que representa o calor de combustão do gás butano, C4H10:
1 C4H10(g) + 6,5 O2(g) → 4 CO2(g) + 5 H2O \( \Delta \)H = – 690 kcal
A massa de água, em gramas, que poderá ser aquecida de 25 °C até a ebulição, com o calor liberado a partir da queima de 11,6 gramas de gás butano, assumindo 75% de eficiência é
Dados: Calor específico da água = 1 cal/ºC . g
Provas
Considere as seguintes equações termoquímicas:
I. 2C(s) + 3 H2(g) + \( \dfrac 1 2 \) O2(g) → C2H5OH(\( \ell \)) \( \Delta \)H = – 66,0 kcal/mol
II. H2(g) + \( \dfrac 1 2 \) O2(g) → H2O(\( \ell \)) \( \Delta \)H = –68,0 kcal/mol
III. C(s) + O2(g) → CO2(g) \( \Delta \)H = –94,0 kcal/mol
A quantidade de calor liberada na queima completa de um tanque cheio com 57,5 litros de etanol é
Dados: detanol = 0,80 g/mL; massa molar do etanol = 46 g/mol.
Provas
Para a decomposição do carbonato de cálcio, CaCO3(s) → CaO(s) + CO2(g), sabe-se que, a 25°C e 1 atm, \( \Delta \)H = 42,37 kcal/mol e \( \Delta \)S = 37,73 cal/K . mol.
Uma indústria que produz cal virgem com seus fornos trabalhando a 1500 °C recebe a recomendação do departamento financeiro para que essa temperatura seja baixada para 800 ºC, por necessidade de redução em seu consumo de energia elétrica. Considerando apenas os aspectos termodinâmicos, o departamento técnico
Provas
O nome correto para cada um dos compostos abaixo, segundo as normas da IUPAC, é
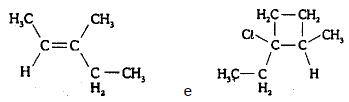
Provas
São conhecidos dois isômeros carbonilados, A e B, ambos cíclicos, com fórmula C6H10O, com um carbono primário, um terciário e o restante secundário. O isômero A reduz o reativo de Tolens, o B não. Reagindo-se o isômero B com cloreto de metil-magnésio, seguido de hidrólise ácida, obtém-se o composto
Provas
Caderno Container