Foram encontradas 35 questões.
Provas
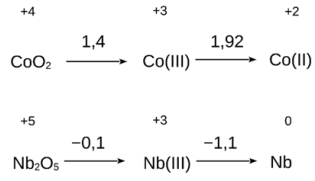
Admitindo-se que essas espécies possam estar participando do processo responsável pelo acendimento do LED, que opera entre 1,5 e 2,7 V, a possível pilha formada envolve:
Provas
A ordem crescente de pKaH é:
Provas
A variação de energia livre relacionada à reação de combustão do etanol, apresentada pela equação a seguir, é mais próxima do comportamento descrito pela seguinte letra (correspondente no gráfico):

C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(g)
Provas
Ventura, D. O lendário azul da Prússia, cor que pode salvar ou tirar vidas. Disponível em www.bbc.com. Adaptado.
A distribuição eletrônica na valência do par associado à conversão eletroquímica de oxidação mencionada no texto é descrita por:
Provas
- Química CinéticaTransformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Os cientistas usam a tabela periódica para acessar rapidamente informações sobre um elemento, como seu símbolo, número ou massa atômicos. A organização da tabela periódica também permite avaliar tendências nas propriedades atômicas, tais como energia de ionização (EI) e eletronegatividade de Pauling (χP), ou mesmo propriedades dos respectivos cátions bivalentes, como dureza absoluta de Pearson (η) e acidez (p\( K \)A). No grupo 12 da tabela temos, de cima para baixo, os elementos zinco, cádmio e mercúrio.\( K \)
Analisando as propriedades mencionadas no texto, para o grupo 12 e partindo do zinco em direção ao mercúrio, é possível prever tendência de:
Provas
A contaminação por mercúrio do ambiente e das populações ribeirinhas na região amazônica, causada pelo garimpo ilegal, tem se agravado e alcançado níveis alarmantes. Mais recentemente, esse problema tem sido noticiado paralelamente a outras denúncias de crimes contra povos indígenas que vivem nas reservas da região. O mercúrio metálico (Hg) usado na extração do ouro converte-se em outras espécies, comumente na forma de cloretos, como cloreto mercuroso (Hg2Cl2), cloreto mercúrico (HgCl2) e cloreto de metilmercúrio (CH3HgCl). O perigo e os riscos associados a essas espécies são descritos nas fichas de segurança, e algumas informações estão colocadas no quadro a seguir.1
| Hg | Hg2Cl2 | HgCl2 |
CH3HgCl |
|
|
Controles de exposição (Pele) mg m−3 (ACGIH)* |
0,025 |
0,025 |
0,025 |
0,01 |
|
Informação toxicológica |
Carcinogenicidade LD50 não disponível | Toxicidade aguda LD50 = 1500 mg kg | Toxicidade aguda LD50 = 41 mg kg−1 |
Toxicidade aguda fatal em contato com a pele |
Entre os compostos listados, verifica-se maior perigo associado à espécie:
Provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
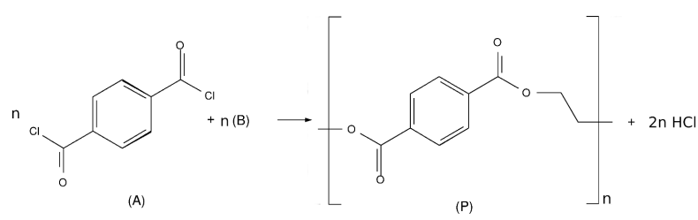
Para obtenção do produto (P), o derivado de cloreto de acila (A) deve reagir com o reagente (B), que é o:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Ao distribuir os elétrons de valência na molécula de N2O, é possível gerar mais de uma estrutura de Lewis. Considerando as cargas formais (CF) dos átomos, a estrutura mais estável é:
Dados: N (Z=7); O (Z=8)
Provas
O óxido nitroso é facilmente oxidado por ozônio para gerar o tetróxido de nitrogênio, conforme equação de equilíbrio a seguir:
N2O(g) + O3(g) ⇌ N2O4(g) K = 4,4 × 102
Num sistema em equilíbrio, as concentrações de O3 e N2O4 são, respectivamente, 6,4 x 10-3 mol L-1 e 0,25 mol L-1. Qual é o valor da concentração de N2O?
Provas
Caderno Container