Foram encontradas 4.578 questões.
A corrosão de objetos metálicos representa grande problema econômico no mundo atual, sendo seus efeitos acentuados pelo fenômeno da chuva ácida. A reação mais importante durante a corrosão de uma superfície de ferro, em presença de água e oxigênio, é a representada pela seguinte equação.
\(2\,\quad\,Fe_{(s)}\,+\,4\,\quad^+_{(aq)}\,+\,O_{2\,\mathrm\,(g)}\,\rightarrow\,2\,\quad\,Fe^{2+}_{aq}\,+\,2\,\quad\,H_2O_{\,(\,\ell)}\)
A seguir, são fornecidos os potenciais-padrão de eletrodo (Eº), a 25 ºC, para algumas reações de redução.
O2 + 4 H+ + 4 e- \(\rightarrow\) 2 H2O Eº = +1,23 VO potencial E de uma célula eletroquímica pode ser relacionado ao seu potencial-padrão pela equação de Nernst,
Fe3+ + e- \(\rightarrow\) Fe2+ Eº = +0,77 V
Cr3+ + 3 e- \(\rightarrow\) Cr Eº = +0,74 V
Fe2+ + 2 e- \(\rightarrow\) Fe Eº = -0,44 V
Cr2+ + 2 e- \(\rightarrow\) Cr Eº = -0,91 V
\(E = E^o - { 2,3 RT \over nF} \log \quad Q,\)
em que \(R\), \(T\), \(n\), \(F\) e \(Q\) representam, respectivamente, a constante universal dos gases, a temperatura da célula eletroquímica (em Kelvin), a quantidade de matéria de elétrons transferidos na reação de oxirredução, a constante de Faraday e o quociente reacional.
Considerando as informações acima e que \(pH\,=-\log a_{H+}\), em que \(a_{H+}\) representa a atividade dos íons \(H^+\) na solução, julgue o item que se segue.
Em uma peça de aço inoxidável, a proteção contra a corrosão ocorre porque o cromo apresenta menor tendência eletroquímica à oxidação que o ferro.
Provas
Os gráficos a seguir mostram resultados obtidos após a aplicação do método dos mínimos quadrados em estudos cinéticos a respeito da reação \(2\,N_2\,O_{5\,\mathrm\,(g)}\,\rightarrow\,4\,NO_{2\,\mathrm\,{(g)}}\,+\,O_{2\,\mathrm\,{(g)}}\).
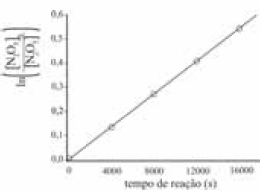
Gráfico 1. Gráfico do logaritmo natural da razão entre a concentração inicial do N2O5(g) − ([N2O5]0) − e sua concentração − [N2O5] − em função do tempo de reação a 25 ºC.
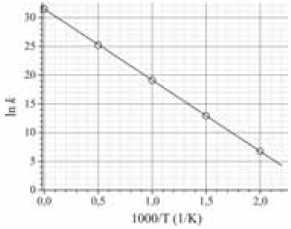
Gráfico 2. Gráfico do logaritmo natural da constante de velocidade, k, em função do inverso da temperatura absoluta, T, multiplicado por 1.000.
Considerando as informações fornecidas e que a constante dos gases ideais seja igual a 8,3 J.mol-1.K-1, julgue o próximo item.
A reação em questão apresenta cinética de segunda ordem.
Provas
Os gráficos a seguir mostram resultados obtidos após a aplicação do método dos mínimos quadrados em estudos cinéticos a respeito da reação \(2\,N_2\,O_{5\,\mathrm\,(g)}\,\rightarrow\,4\,NO_{2\,\mathrm\,{(g)}}\,+\,O_{2\,\mathrm\,{(g)}}\).

Gráfico 1. Gráfico do logaritmo natural da razão entre a concentração inicial do N2O5 (g) − ([N2O5]0) − e sua concentração − [N2O5] − em função do tempo de reação a 25 ºC.

Gráfico 2. Gráfico do logaritmo natural da constante de velocidade, k, em função do inverso da temperatura absoluta, T, multiplicado por 1.000.
Considerando as informações fornecidas e que a constante dos gases ideais seja igual a 8,3 J.mol-1.K-1, julgue o próximo item.
A energia de ativação da reação em questão é maior que 80 kJ/mol.
Provas
A figura a seguir apresenta o diagrama de fases de uma substância. Nesse diagrama, o ponto triplo e o ponto crítico correspondem, respectivamente, às coordenadas (216,8 K, 5,11 atm) e (340,2 K, 72,9 atm).
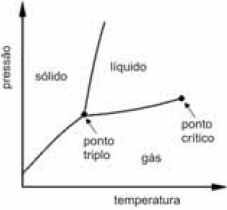
As curvas que representam os pontos de equilíbrio entre as fases podem ser descritas pela equação de Clapeyron, \({dp \over dT} = { \Delta H_{tr} \over T. \Delta V_{tr}},\) em que \(p\), \(T\), \(\Delta H_{tr}\) e \(\Delta V_{tr}\) representam a pressão, a temperatura e as variações de entalpia e de volume durante a transição de fase, respectivamente.
à temperatura de 280 K, a pressão de vapor dessa substância é maior que 72,9 atm.
Provas
A figura a seguir apresenta o diagrama de fases de uma substância. Nesse diagrama, o ponto triplo e o ponto crítico correspondem, respectivamente, às coordenadas (216,8 K, 5,11 atm) e (340,2 K, 72,9 atm).

As curvas que representam os pontos de equilíbrio entre as fases podem ser descritas pela equação de Clapeyron, \({dp \over dT} = { \Delta H_{tr} \over T. \Delta V_{tr}},\) em que \(p\), \(T\), \(\Delta H_{tr}\) e \(\Delta V_{tr}\) representam a pressão, a temperatura e as variações de entalpia e de volume durante a transição de fase, respectivamente.
A partir do diagrama apresentado e com base na equação de Clapeyron, é correto inferir que
à pressão de 1 atm, a referida substância pode sofrer sublimação.
Provas
A figura a seguir apresenta o diagrama de fases de uma substância. Nesse diagrama, o ponto triplo e o ponto crítico correspondem, respectivamente, às coordenadas (216,8 K, 5,11 atm) e (340,2 K, 72,9 atm).

As curvas que representam os pontos de equilíbrio entre as fases podem ser descritas pela equação de Clapeyron, \({dp \over dT} = { \Delta H_{tr} \over T. \Delta V_{tr}},\) em que \(p\), \(T\), \(\Delta H_{tr}\) e \(\Delta V_{tr}\) representam a pressão, a temperatura e as variações de entalpia e de volume durante a transição de fase, respectivamente.
A partir do diagrama apresentado e com base na equação de Clapeyron, é correto inferir que
na temperatura de fusão, a fase sólida da substância em apreço apresenta densidade maior que a do respectivo estado líquido.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\)![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com
base nessa informação e considerando que os logaritmos naturais de 5 e 2
sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Na temperatura T, a energia livre padrão da reação apresentada é negativa, e o valor de seu módulo é superior a 5RT.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\)![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com
base nessa informação e considerando que os logaritmos naturais de 5 e 2
sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Se 10,0 mol de \(BrC\,\ell_{\,\mathrm\,(g)}\) forem colocados em uma câmara inicialmente evacuada, quando o equilíbrio químico for atingido, à temperatura T, a quantidade de matéria de \(Br_2\) será inferior a 6,0 mol.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\)![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com
base nessa informação e considerando que os logaritmos naturais de 5 e 2
sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Considerando que a reação seja endotérmica em toda a faixa compreendida entre as temperaturas T e T' e que T' seja maior que T, é correto concluir que a constante de equilíbrio da reação na temperatura T' é superior a 400.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\) ![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com base nessa informação e considerando que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Para a reação em questão, o volume da câmara não influencia a velocidade com que o equilíbrio é atingido.
Provas
Caderno Container