Foram encontradas 428 questões.
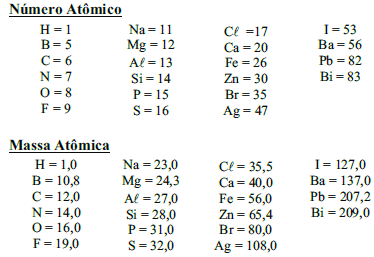
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Considerando os elementos: gálio, alumínio, cloro e oxigênio, as fórmulas corretas dos compostos iônicos formados entre eles são:
Provas
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Um elemento X apresenta propriedades químicas semelhantes às do sódio (Z = 11). X pode ter a seguinte configuração em seu estado fundamental:
Provas
- Química InorgânicaSubstância e mistura: substância simples, substância composta e mistura. Alotropia
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Há distinção entre substância e mistura. Por exemplo: álcool etílico é uma substância, enquanto a gasolina é uma mistura. Assinale a alternativa em que só há misturas:
Provas
Constante Universal dos Gases Ideais: !$ R = 0,082 { \Large { atm.L \over mol.K}} !$
log10 1,111 = 0,0457
log10 2,08 = 0,318
ln 2,329 = 0,845
1 atm = 1,013 x 106 g.cm-1.s-1
1 atm = 760mmHg
Uma pilha foi montada utilizando uma barra de chumbo em solução 0,025M de Pb2+ e uma barra de prata em solução 0,0015M de Ag+ . Sabendo-se os potenciais de redução no estado padrão:
!$ Pb^{2+} + 2e \rightarrow Pb\,\,\,\,E^{ \circ} = -0,13\,volts\\Ag^+ le \rightarrow\,\,\,\,E^{ \circ} =+0,80\,volts !$
podemos afirmar, corretamente, que a carga em ampère- hora (AH) que essa pilha pode fornecer e a d.d.p. (em volts) são, respectiva e aproximadamente:
Provas
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Nem todas as moléculas dos compostos químicos seguem a regra do octeto. Aponte aquela que é exceção à regra.
Provas

Constante Universal dos Gases Ideais: !$ R = 0,082 { \Large { atm.L \over mol.K}} !$
log10 1,111 = 0,0457
log10 2,08 = 0,318
ln 2,329 = 0,845
1 atm = 1,013 x 106 g.cm-1.s-1
1 atm = 760mmHg
Indique a melhor forma possível de identificação entre os ânions !$ PO^{3-}_4\,e\,SO^{2-}_4 !$.
Provas
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Uma dona de casa tempera uma salada com vinagre e sal. Sabendo-se que o vinagre é uma mistura de ácido acético e água, o conjunto de procedimentos que permite separar sal, ácido acético e água é:
Provas
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Na fórmula porcentual ou centesimal do bicarbonato de sódio, NaHCO3, existem, aproximadamente:
Provas
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
Considere os seguintes processos que ocorrem em nosso dia-a-dia:
I - Aquecimento de água para fazer café.
II - Aplicação de éter sobre a lesão de um atleta para resfriar o músculo.
III - Em dia úmido o sal entope o saleiro.
IV - Remoção de manchas em um prato de porcelana com adição de vinagre.
V - Fermentação do lixo orgânico.
VI - Incêndio nas florestas.
NÃO são fenômenos químicos:
Provas
Número Atômico
H = 1 F = !$ C\ell = 17 !$
C= 6 Na = 11 Ca = 20
N = 7 !$ A \ell =13 !$ Ga 31
O = 8 S =16
Massa Atômica
H = 1 !$ A \ell = 27 !$
C= 12 S = 32
O= 16 Ca = 40
Na=23
O álcool etílico, C2H5OH, quando ingerido, provoca alterações no organismo humano. Em algumas pessoas, acima de uma concentração de 0,30g de álcool por litro de sangue, o risco de acidentes automobilísticos aumenta. Um adulto tem, em média, 7 litros de sangue. Para que essas pessoas possam tomar uma bebida alcóolica sem cair na faixa de risco podem ingerir uma quantidade de álcool etílico, no máximo, igual a:
Provas
Caderno Container