Foram encontradas 3.478 questões.
A cromatografia é um método de separação de espécies químicas muito semelhantes. São tipos de cromatografia líquida, EXCETO a de
Provas
O aço em contato com o meio ambiente tende a se oxidar pela presença de O2 e H2O, começando pela superfície do metal até a sua total deterioração. Dentre as soluções que reduzem a velocidade da corrosão, uma delas é a utilização de aços resistentes à corrosão atmosférica como o aço inoxidável. No aço inoxidável estão presentes os metais
Provas
A respeito de corrosão, analise as afirmativas abaixo.
I - A resistência à corrosão dos aços inoxidáveis depende basicamente da composição química e da microestrutura, sendo os aços inoxidáveis martensíticos os menos resistentes e os austeníticos, os mais resistentes à corrosão.
II - Os aços resistentes à corrosão atmosférica são os aços inoxidáveis e os aços patináveis ou aclimáveis.
III - O aço inoxidável é um material que não se destrói mesmo quando submetido aos mais violentos abusos.
IV - Existe uma família inteira de ligas denominadas gusa, com diferentes propriedades, bastando variar a quantidade de carbono e os aços especiais são conseguidos adicionando-se outros metais à liga.
Estão corretas as afirmativas
Provas
A corrosão é a deterioração de um material devido à reação química ou eletroquímica com seu meio. São considerados tipos ou formas de corrosão, EXCETO corrosão
Provas
A cromatografia é um método de separação de espécies químicas muito semelhantes. São tipos de cromatografia líquida, EXCETO a de
Provas
O Ferro, em contato com o oxigênio presente na água e no ar, oxida-se surgindo um precipitado marrom conhecido como ferrugem. O ferro enferrujado é um exemplo de corrosão. Qual o metal que pode ser usado como metal de sacrifício para evitar a ferrugem?
Provas
Considere as semirreações e os potenciais-padrão de redução dos elementos abaixo.
Zn2+ + 2e− !$
ightleftarrows !$ Zn E0 redução = − 0,76 V
Cu2+ + 2e− !$
ightleftarrows !$ Cu E0 redução = + 0,34 V
Ag+ + e− !$
ightleftarrows !$ Ag0 E0 redução = + 0,80 V
Al3+ + 3e− !$
ightleftarrows !$ Al0 E0 redução = − 1,66 V
Fe2+ + 2e− !$
ightleftarrows !$ Fe0 E0 redução = − 0,44 V
2H+ + 2e− !$
ightleftarrows !$ H2 E0 redução = 0,00 V
O composto químico que, em solução, pode ser armazenado em um tanque revestido internamente com zinco metálico, sem que haja alteração de suas características, é
Provas
Os ácidos carboxílicos apresentados abaixo estão dispostos em ordem decrescente de acidez.
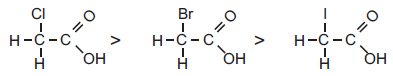
A força ácida desses compostos é influenciada pelo efeito provocado pela presença do halogênio em sua estrutura química, em que o aumento da acidez está relacionado ao aumento de uma das propriedades periódicas desses elementos, que é o (a)
Provas
A proteção catódica por corrente galvânica é um procedimento eletroquímico que atenua as reações de oxidação em uma estrutura metálica, por meio da conexão de outro metal à estrutura que possui um maior potencial de oxidação, formando um anodo de sacrifício. Assim, levando-se em conta apenas as semirreações dos metais e seus respectivos potenciais-padrão de redução, o metal mais apropriado para ser usado como anodo de sacrifício em um sistema de proteção catódica de uma estrutura metálica de ferro é (Dado: Fe2+ + 2 e− !$ ightleftarrows !$ Fe (s) E0 redução = − 0,44 V)
Provas
A hidrazina (N2H4) é utilizada para a remoção do oxigênio dissolvido em águas de alimentação de caldeiras. No entanto, se o seu teor na água não for controlado, a hidrazina transforma o Fe2O3 da parede da caldeira em Fe3O4 , por meio da seguinte reação:
6 Fe2O3 + N2H4 → N2 + 2 H2O + 4 Fe3O4
Nessa reação, oxidante e redutor são, respectivamente,
Provas
Caderno Container