Foram encontradas 2.276 questões.
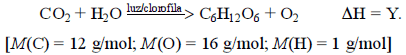
Provas

A revista Superinteressante de julho de 1996 trazia, com certa melancolia, uma reportagem sobre o fim do programa PROÁLCOOL. Afirmavam os autores que “a mólecula de etanol, o álcool hidratado que livrou o país do pesadelo da importação do petróleo, partiu-se. O PROÁLCOOL criou gastos insustentáveis e será extinto em 1997. O Brasil tem alguns meses para decidir o que fazer com a agroindústria que diminuiu a dependência externa de energia e criou um combustível renovável e menos poluente”. A ilustração acima mostra as etapas de produção desse combustível. Acerca desse assunto, de Microbiologia e de processos bioquímicos, julgue o item a seguir.
A etapa de destilação é necessária porque a fermentação rende uma solução que contém apenas entre 12% e 15% de álcool. A destilação eleva o conteúdo de etanol para até 95%.
Provas
Entre os primeiros a explorar o fundo do oceano em busca do ouro negro, o Brasil foi forçado a desenvolver tecnologia própria de prospecção e extração. Hoje, é referência mundial no assunto, trabalhando para atingir reservas em lâminas d’água de 3 mil metros. Vários obstáculos devem ser superados para se alcançar esse objetivo e um dos principais é a corrosão, que degrada os equipamentos empregados nessa atividade e é acelerada pela salinidade do mar.
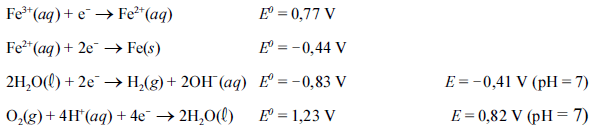
Scientific American Brasil, ed. especial n.º 3, dez./2003 (com adaptações).
Abaixo são representadas algumas reações de redução importantes para a análise da corrosão do ferro metálico, com os seus respectivos potenciais padrão de redução (E0) e alguns potenciais de redução (E), a 25 ºC.
Com relação às informações acima apresentadas, julgue o item que se segue, acerca da corrosão e de assuntos a ela relacionados.
A fosfatização aumenta consideravelmente a eficiência de outros meios convencionais de proteção metálica.
Provas

Sobre uma fila de caminhões e carros paira uma nuvem de fuligem — resultado da queima parcial do óleo dísel, liberando partículas de carbono finamente divididas na atmosfera — e gases tóxicos que ameaça a saúde humana e a do planeta. Essa é uma cena comum nas metrópoles do Brasil e do mundo, produto de uma sociedade dependente dos combustíveis fósseis. Porém, esse quadro funesto pode mudar com a utilização em larga escala do biodísel. Obtido a partir de matérias-primas oleaginosas — como grãos, gorduras vegetais e até óleo de fritura usado, além de outras, que vão de canola e pequi a óleo de peixe e sebo bovino, sendo possível utilizar, também, graxa de esgotos e da indústria —, esse combustível polui muito pouco. Pode ser utilizado como um aditivo do dísel de petróleo, sem grandes adaptações nos veículos, ou isoladamente — nesse caso, pede a substituição de algumas peças de borracha no motor. Trata-se de uma tecnologia que existe no país desde 1970. Na época, foi concedida a primeira patente de biodísel — hoje expirada — a um brasileiro, o cearense Expedito Parente, que desenvolveu a técnica. Mas quem comprou a idéia de fato foram os estrangeiros: os europeus aderiram ao biodísel, assim como os americanos e os japoneses. Há no Brasil iniciativas isoladas, muitas em caráter experimental, como forma de recuperar o tempo perdido.
O biodísel é conhecido desde 1895, quando o engenheiro francês Rudolf Diesel (1858-1913), o criador do motor com ignição a compressão que leva o seu nome, iniciou as pesquisas para utilização de subprodutos do petróleo como combustível para sua invenção. Em 1900, durante a Feira Mundial de Paris, ele utilizou óleo de amendoim para movimentar seu invento. “O motor a dísel pode ser alimentado com óleos vegetais e ajudar o desenvolvimento dos países que o utilizam”, disse na época o engenheiro.
Após um século de dominação mundial do petróleo, o biodísel finalmente encontra um lugar sob os holofotes. Ele é uma mistura de ésteres.
É o que tem sido pesquisado pelo Laboratório de Desenvolvimento de Tecnologias Limpas (LADETEL), do Departamento de Química da USP, em Ribeirão Preto. A equipe desenvolveu o primeiro biodísel de origem 100% vegetal, ao usar álcool de cana no lugar de metanol, um derivado do petróleo, como reagente na queima do óleo vegetal.
É principalmente a vantagem ambiental que tem feito os países europeus, mais comprometidos com a redução de gases-estufa na atmosfera, investirem pesado no biodísel. Isso porque a queima do biodísel gera menos gases poluentes, sem perda de rendimento do motor. Foi constatada uma redução de 48% de monóxido de carbono em comparação com a emissão resultante da queima do dísel. O mesmo vale para o material particulado, a boa e velha fuligem — 26% a menos. A emissão de enxofre, um dos ingredientes da chuva ácida, é nula.
Idem, 5/3/2004 (com adaptações).
A partir do texto ao lado, julgue o item que se segue.
A obtenção do óleo vegetal a partir de grãos corresponde a uma transformação química.
Provas
Provas
Entre os primeiros a explorar o fundo do oceano em busca do ouro negro, o Brasil foi forçado a desenvolver tecnologia própria de prospecção e extração. Hoje, é referência mundial no assunto, trabalhando para atingir reservas em lâminas d’água de 3 mil metros. Vários obstáculos devem ser superados para se alcançar esse objetivo e um dos principais é a corrosão, que degrada os equipamentos empregados nessa atividade e é acelerada pela salinidade do mar.
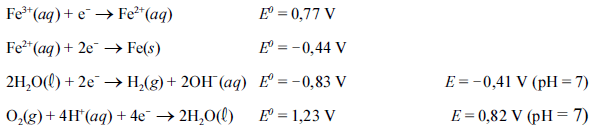
Scientific American Brasil, ed. especial n.º 3, dez./2003 (com adaptações).
Abaixo são representadas algumas reações de redução importantes para a análise da corrosão do ferro metálico, com os seus respectivos potenciais padrão de redução (E0) e alguns potenciais de redução (E), a 25 ºC.
Com relação às informações acima apresentadas, julgue o item que se segue, acerca da corrosão e de assuntos a ela relacionados.
O aumento do pH diminui a corrosão do ferro pelo oxigênio dissolvido na água.
Provas
Provas
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
Considere os potenciais-padrão de redução abaixo.
!$ S(s)2e^- \rightarrow S^{2-} \,\,\,\, Eº=0,407V !$
!$ Cr_2O^{2-}_7+14H^++6e^- \rightarrow 2Cr^{3+}+7H_2O\,\,\,\, Eº+1,36V !$
Com base nesses dados, é correto concluir que o enxofre poderia ser determinado por dicromatometria, ou seja, por volumetria de oxirredução, usando-se o dicromato de potássio como titulante. No entanto, para isso, o enxofre teria de ser convertido antes em íon sulfeto (S2-) por meio de um agente redutor adequado, cujo excesso pudesse ser eliminado previamente à titulação.
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
Sabendo-se que o pKa do alaranjado de metila é igual a 3,7, o do azul de bromotimol é igual a 7,1 e o da fenolftaleína é igual a 9,6, então, o melhor indicador para o primeiro ponto de equivalência dessa titulação, entre os citados, é a fenolftaleína.
Provas
Caderno Container