Foram encontradas 2.276 questões.
O modelo de obtenção de energia a partir da queima de combustíveis fósseis, adotado no início do desenvolvimento econômico industrial e cuja equação química geral é !$ \alpha !$CxH2x + 2 + !$ \beta !$O2 → !$ \gamma !$CO2 + !$ \eta !$H2O, tem apresentado várias conseqüências danosas para o atual estágio socioeconômico mundial. Uma delas é o aumento da concentração de óxidos no ar, tais como CO2, SO2, SO3, NO e NO2, que poluem a atmosfera. Esses óxidos reagem com a água da chuva, formando ácidos. Abaixo são representados alguns exemplos dessas reações.
I – CO2 + H2O → H2CO3
II – SO2 + ½ O2 + H2O → H2SO4
III – 2NO + O2 + H2O → HNO3 + HNO2
Os ácidos formados precipitam-se com a chuva, o que traz prejuízos para a agricultura, a vida aquática, a construção civil etc. Questões como essas, associadas à incerteza da quantidade de petróleo disponível no mundo, tornaram a pesquisa de outras fontes de energia uma prioridade na busca do bem-estar da humanidade e de um desenvolvimento economicamente sustentável. Diante dessa tarefa, a PETROBRAS já vem realizando pesquisas e decidiu que, até 2010, será uma companhia de energia e não mais uma empresa somente de petróleo e gás, o que justifica o seu slogan: DESAFIO, ESSA É A NOSSA ENERGIA!
Considerando o texto acima e sabendo que M(E) = 12 g/mol, M(O) = 16 g/mol e M(H) = 1 g/mol, julgue o item a seguir.
Os óxidos CO2, SO2 e NO reagem com ácido, produzindo sal e água. Por conseguinte, não reagem com base.
Provas
Julgue o item a seguir, acerca de alguns aspectos da química de fármacos, produtos de limpeza e saponificação.
O fator polaridade é determinante na ação de sabões e detergentes, mas não tem importância significativa para o desenvolvimento de fármacos.
Provas
O modelo de obtenção de energia a partir da queima de combustíveis fósseis, adotado no início do desenvolvimento econômico industrial e cuja equação química geral é !$ \alpha !$CxH2x + 2 + !$ \beta !$O2 → !$ \gamma !$CO2 + !$ \eta !$H2O, tem apresentado várias conseqüências danosas para o atual estágio socioeconômico mundial. Uma delas é o aumento da concentração de óxidos no ar, tais como CO2, SO2, SO3, NO e NO2, que poluem a atmosfera. Esses óxidos reagem com a água da chuva, formando ácidos. Abaixo são representados alguns exemplos dessas reações.
I – CO2 + H2O → H2CO3
II – SO2 + ½ O2 + H2O → H2SO4
III – 2NO + O2 + H2O → HNO3 + HNO2
Os ácidos formados precipitam-se com a chuva, o que traz prejuízos para a agricultura, a vida aquática, a construção civil etc. Questões como essas, associadas à incerteza da quantidade de petróleo disponível no mundo, tornaram a pesquisa de outras fontes de energia uma prioridade na busca do bem-estar da humanidade e de um desenvolvimento economicamente sustentável. Diante dessa tarefa, a PETROBRAS já vem realizando pesquisas e decidiu que, até 2010, será uma companhia de energia e não mais uma empresa somente de petróleo e gás, o que justifica o seu slogan: DESAFIO, ESSA É A NOSSA ENERGIA!
Considerando o texto acima e sabendo que M(C) = 12 g/mol, M(O) = 16 g/mol e M(H) = 1 g/mol, julgue o item a seguir.
As substâncias elementares dos átomos representados nas equações I, II e III apresentam altas condutividades térmica e elétrica.
Provas

Sobre uma fila de caminhões e carros paira uma nuvem de fuligem — resultado da queima parcial do óleo dísel, liberando partículas de carbono finamente divididas na atmosfera — e gases tóxicos que ameaça a saúde humana e a do planeta. Essa é uma cena comum nas metrópoles do Brasil e do mundo, produto de uma sociedade dependente dos combustíveis fósseis. Porém, esse quadro funesto pode mudar com a utilização em larga escala do biodísel. Obtido a partir de matérias-primas oleaginosas — como grãos, gorduras vegetais e até óleo de fritura usado, além de outras, que vão de canola e pequi a óleo de peixe e sebo bovino, sendo possível utilizar, também, graxa de esgotos e da indústria —, esse combustível polui muito pouco. Pode ser utilizado como um aditivo do dísel de petróleo, sem grandes adaptações nos veículos, ou isoladamente — nesse caso, pede a substituição de algumas peças de borracha no motor. Trata-se de uma tecnologia que existe no país desde 1970. Na época, foi concedida a primeira patente de biodísel — hoje expirada — a um brasileiro, o cearense Expedito Parente, que desenvolveu a técnica. Mas quem comprou a idéia de fato foram os estrangeiros: os europeus aderiram ao biodísel, assim como os americanos e os japoneses. Há no Brasil iniciativas isoladas, muitas em caráter experimental, como forma de recuperar o tempo perdido.
O biodísel é conhecido desde 1895, quando o engenheiro francês Rudolf Diesel (1858-1913), o criador do motor com ignição a compressão que leva o seu nome, iniciou as pesquisas para utilização de subprodutos do petróleo como combustível para sua invenção. Em 1900, durante a Feira Mundial de Paris, ele utilizou óleo de amendoim para movimentar seu invento. “O motor a dísel pode ser alimentado com óleos vegetais e ajudar o desenvolvimento dos países que o utilizam”, disse na época o engenheiro.
Após um século de dominação mundial do petróleo, o biodísel finalmente encontra um lugar sob os holofotes. Ele é uma mistura de ésteres.
É o que tem sido pesquisado pelo Laboratório de Desenvolvimento de Tecnologias Limpas (LADETEL), do Departamento de Química da USP, em Ribeirão Preto. A equipe desenvolveu o primeiro biodísel de origem 100% vegetal, ao usar álcool de cana no lugar de metanol, um derivado do petróleo, como reagente na queima do óleo vegetal.
É principalmente a vantagem ambiental que tem feito os países europeus, mais comprometidos com a redução de gases-estufa na atmosfera, investirem pesado no biodísel. Isso porque a queima do biodísel gera menos gases poluentes, sem perda de rendimento do motor. Foi constatada uma redução de 48% de monóxido de carbono em comparação com a emissão resultante da queima do dísel. O mesmo vale para o material particulado, a boa e velha fuligem — 26% a menos. A emissão de enxofre, um dos ingredientes da chuva ácida, é nula.
Idem, 5/3/2004 (com adaptações).
A partir do texto ao lado, julgue o item que se segue.
Uma molécula de etanol é formada por íons de carbono, hidrogênio e oxigênio.
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
O ácido sulfúrico é considerado um ácido forte com relação ao 1.º hidrogênio dissociado.
Provas
Julgue o item a seguir, acerca de alguns aspectos da química de fármacos, produtos de limpeza e saponificação.
A produção de sabão é feita pela hidrólise alcalina de ésteres de ácidos graxos. Os sais obtidos são de difícil biodegradação, o que tem sido alvo de muitos estudos, devido aos problemas causados ao meio ambiente.
Provas
Provas
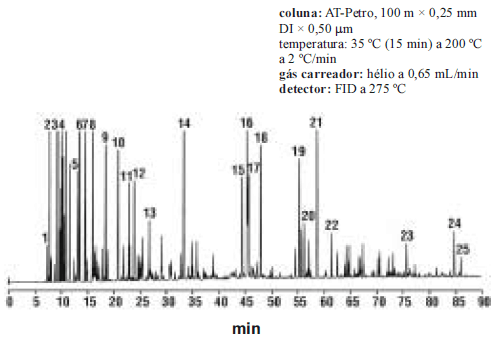
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
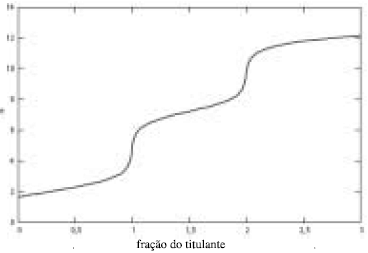
A curva de titulação do H2SO4 pelo NaOH pode ser corretamente representada pela figura abaixo.
Provas
Na luta contra a poluição do ar nos centros urbanos, a contribuição da Química é essencial. A Catálise é uma área da Química que permite compreender o funcionamento dos conversores catalíticos. Mais especificamente, em relação ao uso de combustíveis automotivos, o estudo das reações químicas envolvidas é de fundamental importância. Uma das reações relaciona-se à queima de metano, cuja equação representativa não-balanceada é:
CH4 + O2 → CO2 + H2O
[M(C) = 12 g/mol; M(H) = 1 g/mol; M(O) = 16 g/mol].
Acerca desse assunto, julgue o item subseqüente.
Considerando a energia de ativação envolvida, os postos de combustíveis devem possuir recipientes que impeçam o contato da gasolina com o oxigênio do ar.
Provas

Sobre uma fila de caminhões e carros paira uma nuvem de fuligem — resultado da queima parcial do óleo dísel, liberando partículas de carbono finamente divididas na atmosfera — e gases tóxicos que ameaça a saúde humana e a do planeta. Essa é uma cena comum nas metrópoles do Brasil e do mundo, produto de uma sociedade dependente dos combustíveis fósseis. Porém, esse quadro funesto pode mudar com a utilização em larga escala do biodísel. Obtido a partir de matérias-primas oleaginosas — como grãos, gorduras vegetais e até óleo de fritura usado, além de outras, que vão de canola e pequi a óleo de peixe e sebo bovino, sendo possível utilizar, também, graxa de esgotos e da indústria —, esse combustível polui muito pouco. Pode ser utilizado como um aditivo do dísel de petróleo, sem grandes adaptações nos veículos, ou isoladamente — nesse caso, pede a substituição de algumas peças de borracha no motor. Trata-se de uma tecnologia que existe no país desde 1970. Na época, foi concedida a primeira patente de biodísel — hoje expirada — a um brasileiro, o cearense Expedito Parente, que desenvolveu a técnica. Mas quem comprou a idéia de fato foram os estrangeiros: os europeus aderiram ao biodísel, assim como os americanos e os japoneses. Há no Brasil iniciativas isoladas, muitas em caráter experimental, como forma de recuperar o tempo perdido.
O biodísel é conhecido desde 1895, quando o engenheiro francês Rudolf Diesel (1858-1913), o criador do motor com ignição a compressão que leva o seu nome, iniciou as pesquisas para utilização de subprodutos do petróleo como combustível para sua invenção. Em 1900, durante a Feira Mundial de Paris, ele utilizou óleo de amendoim para movimentar seu invento. “O motor a dísel pode ser alimentado com óleos vegetais e ajudar o desenvolvimento dos países que o utilizam”, disse na época o engenheiro.
Após um século de dominação mundial do petróleo, o biodísel finalmente encontra um lugar sob os holofotes. Ele é uma mistura de ésteres.
É o que tem sido pesquisado pelo Laboratório de Desenvolvimento de Tecnologias Limpas (LADETEL), do Departamento de Química da USP, em Ribeirão Preto. A equipe desenvolveu o primeiro biodísel de origem 100% vegetal, ao usar álcool de cana no lugar de metanol, um derivado do petróleo, como reagente na queima do óleo vegetal.
É principalmente a vantagem ambiental que tem feito os países europeus, mais comprometidos com a redução de gases-estufa na atmosfera, investirem pesado no biodísel. Isso porque a queima do biodísel gera menos gases poluentes, sem perda de rendimento do motor. Foi constatada uma redução de 48% de monóxido de carbono em comparação com a emissão resultante da queima do dísel. O mesmo vale para o material particulado, a boa e velha fuligem — 26% a menos. A emissão de enxofre, um dos ingredientes da chuva ácida, é nula.
Idem, 5/3/2004 (com adaptações).
A partir do texto ao lado, julgue o item que se segue.
Com a utilização do biodísel, elimina-se a emissão de chuva com pH superior a 7.
Provas
Caderno Container