Foram encontradas 2.276 questões.
Provas

A simples lavagem de um carro em equipamentos automáticos de postos de gasolina gasta, em média, cerca de 100 litros de água. Diante da perspectiva de um futuro de escassez desse recurso, diminuir seu desperdício foi a meta de uma técnica desenvolvida por uma engenheira civil em seu mestrado, realizado na Universidade Estadual de Campinas (Unicamp). Na pesquisa, foi elaborado um processo de reciclagem que reduz a quantidade de poluentes que se incorporam à água após ela ser usada nos equipamentos de lavagem, o que permite a sua reutilização pelos postos de gasolina.
O processo de reciclagem que a pesquisadora utilizou e aperfeiçoou foi o da flotação por ar dissolvido: a água usada na lavagem é armazenada em um recipiente e recebe substâncias químicas (cloreto de ferro, sulfato de alumínio etc.), que fazem com que as partículas de sujeira se aglomerem e formem flocos. Em seguida são liberadas microbolhas de ar que aderem aos flocos de sujeira. O aglomerado partícula-bolha é menos denso que a água, o que permite a remoção manual ou mecânica de grande parte dos poluentes presentes no líquido.
De 70% a 80% da água utilizada em uma lavagem pode ser recuperada, mas a taxa pode ser ainda maior com o acréscimo de água da chuva, que serve para minimizar as perdas com a evaporação e diminuir o índice de poluentes que se concentram após vários processos de reciclagem. “Uma certa quantidade de sais, por exemplo, pode provocar a corrosão da carroceria do veículo”, explica a pesquisadora.
Os poluentes produzidos em uma lavagem de carro são uma mixórdia: óleos, graxa, partículas de poeira, carbono, asfalto, metais pesados, detergentes etc. “Uma remoção grosseira dos poluentes pode ocasionar o crescimento de microrganismos, como a bactéria Legionella pneumophila, que podem provocar danos à saúde das pessoas que entram em contato com o líquido armazenado”, pondera a pesquisadora. “Além disso, a água pode ficar com um odor desagradável”. A reciclagem da água usada na lavagem de carros ainda é incipiente no Brasil, pois a maioria dos métodos não atinge resultados satisfatórios. “No exterior existem tratamentos eficientes, mas muito caros”, esclarece a pesquisadora. Os testes em escala experimental realizados conseguiram remover cerca de 90% dos poluentes suspensos e de 60% a 80% dos dissolvidos. “Esse é um índice de qualidade ótimo para se reciclar a água”, ressalta.
Ciência Hoje on-line. 4/7/2003 (com adaptações).
Tendo por referência o texto ao lado, julgue o item a seguir.
O “aglomerado partícula-bolha”, obtido no processo de reciclagem descrito, tende a flutuar na água que está sendo tratada.
Provas
Um químico recebeu uma amostra sólida contendo uma mistura de substâncias orgânicas. Após separação dos componentes da mistura (total de três) e purificação das substâncias, foram realizados testes em laboratório e obtidos diferentes espectros dos compostos. Os resultados foram registrados, alguns dos quais são descritos a seguir.
Substância 1: é insolúvel em água, solúvel em solução aquosa de NaOH a 5%, mas insolúvel em solução aquosa de NaHCO3 a 5%.
Substância 2: o espectro de infravermelho apresenta banda larga em torno de 3.000 cm-1.
Substância 3: o espectro de hidrogênio de ressonância magnética nuclear apresenta dois sinais: um quarteto e um tripleto.
Acerca das substâncias acima descritas e de possíveis testes a serem realizados, julgue o seguinte item.
Para se saber o número de componentes da mistura, pode-se proceder à sua destilação.
Provas
Um químico recebeu uma amostra sólida contendo uma mistura de substâncias orgânicas. Após separação dos componentes da mistura (total de três) e purificação das substâncias, foram realizados testes em laboratório e obtidos diferentes espectros dos compostos. Os resultados foram registrados, alguns dos quais são descritos a seguir.
Substância 1: é insolúvel em água, solúvel em solução aquosa de NaOH a 5%, mas insolúvel em solução aquosa de NaHCO3 a 5%.
Substância 2: o espectro de infravermelho apresenta banda larga em torno de 3.000 cm-1.
Substância 3: o espectro de hidrogênio de ressonância magnética nuclear apresenta dois sinais: um quarteto e um tripleto.
Acerca das substâncias acima descritas e de possíveis testes a serem realizados, julgue o seguinte item.
O registro dos resultados deve conter todas as constantes físicas obtidas, os testes realizados, os dados espectroscópicos, entre outros. O nome do químico analista deve ser ocultado, por motivo de segurança, sendo de conhecimento apenas do gerente do laboratório.
Provas
Provas
Provas
Julgue o item que se segue.
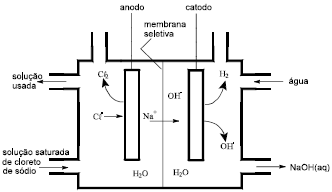
Sabendo-se que a produção industrial de cloro e soda cáustica é feita por meio da eletrólise do cloreto de sódio, representada pela equação
2 NaCl(aq) + 2 H2O(R) → 2 NaOH(aq) + H2(g) + Cl2(g),
é correto afirmar que o respectivo esquema é o abaixo representado.
Provas
Um químico recebeu uma amostra sólida contendo uma mistura de substâncias orgânicas. Após separação dos componentes da mistura (total de três) e purificação das substâncias, foram realizados testes em laboratório e obtidos diferentes espectros dos compostos. Os resultados foram registrados, alguns dos quais são descritos a seguir.
Substância 1: é insolúvel em água, solúvel em solução aquosa de NaOH a 5%, mas insolúvel em solução aquosa de NaHCO3 a 5%.
Substância 2: o espectro de infravermelho apresenta banda larga em torno de 3.000 cm-1.
Substância 3: o espectro de hidrogênio de ressonância magnética nuclear apresenta dois sinais: um quarteto e um tripleto.
Acerca das substâncias acima descritas e de possíveis testes a serem realizados, julgue o seguinte item.
A cromatografia em camada delgada pode ser utilizada para a purificação das substâncias isoladas.
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
Uma forma alternativa de titular o enxofre contido em um combustível é por volumetria de complexação, pois o enxofre forma um complexo estável com o ácido etilenodiaminotetracético (EDTA).
Provas
Provas
Caderno Container