Foram encontradas 45 questões.
Analise e responda a questão, de acordo com Lei nº 8.112, de 11/12/1990 e suas alterações.
Assinale a alternativa INCORRETA.
Provas
Questão presente nas seguintes provas
A quantidade de mercúrio encontrada em amostras de 5 (cinco) espécimes diferentes de peixes de um lago foi determinada por métodos baseados na técnica de absorção atômica. Os resultados
dessas análises estão apresentados na Tabela 1 abaixo. Tabela 1: Concentração (em parte por milhão, ppm) de mercúrio presente em cinco diferentes espécimes de peixes lacustres.
| Espécime |
Número de
amostras
medidas
|
Concentração de
mercúrio
(em ppm)
|
Média
(em ppm)
|
Desvio
padrão
(em ppm)
|
| 1 | 3 | 1,80; 1,58; 1,64 | 1,67 | 0,11 |
| 2 | 4 | 0,96; 0,98; 1,02; 1,1 | 1,02 | 0,06 |
| 3 | 6 | 2,06; 1,93; 2,12; 2,16; 1,89; 1,95 | 2,02 | 0,11 |
| 4 | 5 | 2,35; 2,44; 2,7; 2,48; 2,44 | 2,48 | 0,13 |
| 5 | 4 | 1,11; 1,15; 1,22; 1,04 | 1,13 | 0,08 |
Uma inspeção simples nessa tabela mostra que:
Provas
Questão presente nas seguintes provas
Em diversas áreas da ciência, unidades de quantidades físicas são criadas a partir de definições ou convenções próprias. Como dois exemplos, na criação e desenvolvimento da termodinâmica foi empregado a “caloria” como unidade de energia e na área da física atômica e molecular a unidade “eletron-Volt” é mais adequada para uso cotidiano.
A unidade de energia “caloria”, cujo símbolo é o “cal”, tem a correspondência de 1 cal = 4,184 J, sendo o Joule a unidade de energia no sistema internacional (SI) de medidas. Por outro lado, o eletron-Volt, símbolo “eV”, tem a correspondência 1 eV = 1,602×10−19 J. Por definição, 1 eV é a energia cinética ganha por um elétron, inicialmente em repouso, acelerado por uma diferença de potencial de 1 V no vácuo.
A energia de dissociação C-H em hidrocarbonetos é da ordem de 100 cal mol−1. O valor dessa energia em Joules por molécula e eletron-Volts por molécula é estimado ser, respectivamente:
Provas
Questão presente nas seguintes provas
O alumínio é o elemento metálico mais abundante da crosta terrestre.
Seu peso específico, condutividade elétrica, resistência à corrosão após passivação e baixo ponto de fusão lhe conferem inúmeras aplicações. No entanto, suas aplicações práticas apresentam-se limitadas sobremaneira devido aos seguintes problemas listados abaixo. EXCETO:
Provas
Questão presente nas seguintes provas
A equação de Clapeyron estabelece que o produto da pressão p e o volume V ocupado por um gás é igual ao produto da quantidade de matéria n do gás por sua temperatura T (em graus absoluto) e uma constante R, a denominada constante dos gases ideias:
pV = nRT [Equação de Clapeyron]
Gases que seguem exatamente o comportamento descrito pela equação de Clapeyron são denominados gases ideais.
Para qualquer gás, ideal ou não ideal, pode-se formar uma função termodinâmica chamada fator de compressibilidade, Z(p), e definida pela razão
!$ Z(p) = \dfrac {pV} {nRT} !$ Fator de compressabilidade de um gás]
Na figura abaixo, é apresentado o comportamento da função Z(p) em função da pressão p para 1 (um) mol dos gases nitrogênio (N2), metano (CH4), hidrogênio (H2) e dióxido de carbono (CO2), todos obtidos à temperatura ambiente.
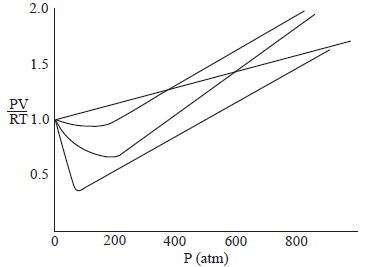
Variação da função fator de compressibilidade
Z(p) = pV / nRT em função da pressão para os gases
nitrogênio, metano, hidrogênio e dióxido de carbono
obtido a 25º.
Com as informações apresentadas, conclui-se que, à temperatura de 25º C:
Provas
Questão presente nas seguintes provas
De acordo com a Teoria de Repulsão dos Pares Eletrônicos da Camada de Valência (VSEPR, sigla inglesa), a geometria em torno de um átomo central na estrutura molecular de um composto é definida pela repulsão dos pares de elétrons de sua camada de valência (elétrons que participam de uma ligação química e os não ligantes) e pelos átomos ligados a ele.
Por outro lado, a polaridade total de uma molécula pode ser determinada pela soma vetorial das polaridades ao longo de cada ligação química presente na sua estrutura.
Baseado nessas informações, marque a alternativa que apresenta a associação de uma substância química com sua geometria e polaridade molecular mais provável.
| Substância | Geometria | Polaridade |
Provas
Questão presente nas seguintes provas
A cromatografia é uma técnica de análise que se presta à separação, identificação, purificação e doseamento de substâncias orgânicas e inorgânicas.
A cromatografia baseia-se na diferença de velocidade com que as substâncias se movem em um meio poroso, a fase estacionária, quando arrastadas por um solvente, o eluente, em movimento. Na cromatografia em camada delgada, uma placa de vidro é revestida com uma camada de um material adsorvente, normalmente sílica finamente pulverizada, formando, assim, a denominada cromatoplaca.
Em relação à cromatografia em camada delgada, é CORRETO afirmar que:
Provas
Questão presente nas seguintes provas
Considere as fórmulas moleculares estendidas das substâncias I a V apresentadas a seguir, substâncias que mostram diferentes grupos funcionais orgânicos:
|
CH3CH2CH2CH2C(O)CH2CH3
I
|
CH3CH2CH2CH2CO2H
II
|
|
|
CH3CH2CH2CH2CONH2
III
|
||
|
CH3CH2CH2CH2CH2O CH2CH3
IV
|
CH3CH2CH2CH2CH(OH)CH2CH3
V
|
Para essas substâncias, pode-se afirmar que:
Provas
Questão presente nas seguintes provas
SORRIA
A substituição do homem pela máquina segue em ritmo acelerado. São máquinas que atendem ao telefone de muitas empresas. Isto é melhor para o cliente? Nem sempre. É mais barato para a empresa? Provavelmente sim. O que é certo é que elimina empregos de atendentes ao mesmo tempo em que gera empregos técnicos. Produz as adoradas estatísticas, que regem o mundo corporativo, sejam sensatas ou não.
Hoje ouvimos uma frase onipresente: “Para sua segurança esta ligação poderá ser gravada”. É uma versão rústica de outra mensagem frequente nos EUA: “Para controle de qualidade do nosso atendimento esta ligação poderá ser monitorada”.
Por que gravam nossas ligações? De que segurança estão falando? Estão querendo nos proteger ou proteger a eles mesmos? Se é para nos proteger, por que não facilitam o nosso acesso a tais gravações?
O paralelo mais óbvio às gravações de voz são as câmeras de segurança. No mundo da espionagem institucionalizada, a comunicação evoluiu para algo mais simpático e menos ameaçador. “Sorria. Você está sendo filmado.”
As câmeras são instaladas para flagrar furtos, roubos e outros crimes. Mas, ao ler essa frase, o cidadão pode se sentir um ator de cinema e realmente sorrir, esquecendo um instante que o motivo da filmagem é desconfiança e repressão.
Nas últimas semanas, um colégio tradicional paulistano instalou câmeras dentro de salas de aula. Não, não eram berçários dos quais pais aflitos, desconfiados ou culpados vigiam bebês e profissionais à distância. Era uma escola de elite que num só dia suspendeu 107 alunos do ensino médio que resolveram protestar quando descobriram as câmeras.
Questionada, a direção da escola alegou razões de segurança e disciplina. O fato de já haver câmeras em laboratórios [...] fez com que a escola não se preocupasse em discutir o tema com pais e alunos antes de instalar os olhos de vidro em todas as salas de aula.
Parte dos pais aprovou a medida, mas especialistas levantaram a voz para questionar que tipo de educação se desenvolve com base em desconfiança mútua. Outros questionaram o direito de uma escola filmar menores sem aval dos pais.
A ideia é do final do século 18 e foi concebida pelo filósofo e jurista inglês Jeremy Bentham. Ganhou o nome de poder panóptico: a consciência da permanente visibilidade asseguraria o funcionamento de um poder autoritário, como uma prisão, um manicômio, uma empresa ou uma escola. A única novidade é a banalização do instrumento.
Panopticon é o nome de uma estrutura arquitetônica concebida para permitir a observação de tudo o que se passa num edifício sem que as pessoas a serem observadas saibam se estão sendo vigiadas. A simples possibilidade de estarem sendo vigiadas regularia o comportamento delas. O desenho consiste numa estrutura circular com uma torre de inspeção no centro, de onde o inspetor oculto poderia avistar todos os que estiverem no perímetro do edifício. Ele descreveu o projeto como um novo modo de obter poder da mente sobre a mente, numa quantidade até então sem paralelo.
STRECKER, Marion. Folha de S.Paulo. São Paulo, 15 out.2012. TEC, F8.[Fragmento]
Assinale a alternativa que ULTRAPASSA as informações do texto.
Provas
Questão presente nas seguintes provas
Na combustão completa de uma substância contendo apenas um grupo éster como função orgânica, foram produzidos 2,64 g de CO2 e 1,08 g de H2O. Sabendo que as massas molares do oxigênio, carbono e hidrogênio são, respectivamente, 16,0 g mol−1, 12,0 g mol−1 e 1,0 g mol−1, pode-se propor que a fórmula molecular desse éster é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container