Foram encontradas 45 questões.
Provas
Provas
Provas
Provas
O aço é uma liga metálica formada essencialmente por ferro e carbono, com percentagens desse último elemento variando entre 0,008 e 2,11 %. Além dos componentes principais indicados, o aço incorpora outros elementos químicos provenientes da sucata, do mineral ou do processo de fabricação empregado. Outros são adicionados intencionalmente para melhorar algumas propriedades, tais como magnéticas, mecânicas e resistência à corrosão.
Uma análise química para a determinação do teor de Ni em amostras de um lote de aço inox foi realizada segundo o seguinte procedimento:
A uma alíquota de aço pesando 0,5000 g foram adicionados 50 mL de HCl diluído e a mistura foi aquecida até a completa dissolução da amostra. Após resfriamento, a solução foi transferida para um balão volumétrico com capacidade igual a 100,00 mL e o volume completado com água destilada. Para a determinação do níquel (59 g !$ mol^{−1} !$), uma alíquota de 25,00 mL do balão volumétrico foi transferida para um béquer de 500 mL. Após aquecimento dessa alíquota, foram adicionados 25 mL de solução alcóolica de dimetilglioxima 1% m/m e solução de !$ NH_3 !$. A mistura resultante contendo dimetilglioximato de níquel (289 g !$ mol^{−1} !$) foi aquecida por 30 minutos e filtrada. Após a filtração, o papel de filtro que inicialmente pesava 0,2000 g foi transferido para uma estufa a 100oC por 50 minutos. Após resfriamento o papel de filtro com a amostra retida foi pesado, obtendo-se uma massa de 0, 2012 g.
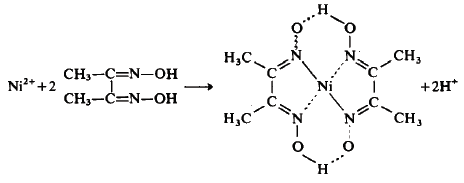
Conhecendo-se a reação entre o níquel e a dimetilglioxima, é CORRETO afirmar que a concentração de níquel é
Provas
Como cuidados básicos de limpeza e conservação de vidrarias e equipamentos de uso em laboratórios de química, após lavagem com detergente e água corrente, NÃO se deve secar em estufas as vidrarias:
Provas
.
Um método colorimétrico foi planejado para a determinação da concentração das soluções do azul de metileno obtidas após o processo de adsorção pelo carvão ativado. Um colorímetro com as especificações técnicas mostradas na tabela abaixo foi escolhido.

Provas
Provas
Provas
Provas
Caderno Container