Foram encontradas 45 questões.
Como funciona a Estação Espacial Internacional
Com cabines para dormir, banheiros e espaço para fazer exercícios, a Estação Espacial Internacional lembra um hotel. O hotel mais veloz do mundo: viaja pelo espaço a 27 mil km/h. Além disso, se fosse um hotel, estaria constantemente em baixa temporada: recebeu apenas 98 visitantes em 12 anos de atividade. E conta com turistas que estão longe do lazer das férias. Eles passam o tempo todo pesquisando nos laboratórios científicos dentro da estação e trabalhando duro para instalar as pesadas peças que trouxeram da Terra. A construção desse complexo de 420 toneladas começou em 1998, depois de mais de uma década de estudos. Como seria impossível montá-lo na Terra e enviálo ao espaço, a solução foi fazer peças que pudessem ser lançadas por foguetes, uma por uma. A ISS (International Space Station) foi construída como um quebra-cabeça, com investimentos de EUA, Japão, Rússia e alguns países da Europa - mas com ajuda de astronautas do mundo inteiro. Inclusive o brasileiro Marcos Pontes, engenheiro de sistemas que participou de testes das peças e depois da construção. Depois de 40 voos para montagem, a estação ainda não está concluída. E, em dezembro deste ano, a ISS ganhará um novo cômodo: um laboratório equipado com um braço robótico.
Fonte: http://super.abril.com.br/universo/como-funciona-estacao-espacial-internacional-743106.shtml, acesso em 15 fev. 2015.
Assinale a passagem transcrita do texto em que há ocorrência de linguagem informal.
Provas
Questão presente nas seguintes provas
A mistura de 1 litro de solução 0,50 mol !$ L^{−1} !$ de cloreto de bário com 1 litro de solução 0,20 mol !$ L^{−1} !$ de cromato de potássio leva à formação de um sal pouco solúvel. Considerando-se que o cromato de bário tem solubilidade desprezível, as concentrações de ions bário, cloreto e potássio em solução, após o término da precipitação são, respectivamente:
Provas
Questão presente nas seguintes provas
O mol é uma ferramenta fundamental para os químicos, que torna possível, com a ajuda da tabela periódica e uma balança, determinar o número de átomos, íons ou moléculas em uma amostra. A fórmula empírica da aspirina que possui 60,0 % de carbono, 4,5 % de hidrogênio e 35,5 % de oxigênio em massa é
Provas
Questão presente nas seguintes provas
Para padronizar uma solução de permanganato de potássio, KMnO4, três massas iguais a 0,3350 g do padrão primário oxalato de sódio anidro, Na2C2O4, foram pesadas e transferidas para um erlenmeyer de 250 mL. O padrão foi titulado em meio ácido, em triplicata, com a solução de KMnO4 até o aparecimento da coloração rósea, consumindo o volume médio igual a 10,00 mL deste titulante. Considerando a reação da titulação,
!$ 2MnO_4^- !$ !$ + !$ !$ 5 !$ !$ C_2O_4^{2−} !$ !$ + !$ !$ 8 !$ !$ H^+ !$ !$ ⇌ !$ !$ 2 !$ !$ Mn^{2+} !$ !$ + !$ !$ 10 !$ !$ CO_2 !$ !$ + !$ !$ 4 !$ !$ H_2O !$
É CORRETO que a concentração do permanganato de potássio determinada é:
Provas
Questão presente nas seguintes provas
A reação de decomposição do peróxido de hidrogênio, !$ H_2O_2 !$, catalisado com o cloreto férrico, !$ FeCl_3 !$, segue uma lei de velocidade simples de reação de primeira ordem.
A cinética dessa reação foi acompanhada para uma amostra de água oxigenada com uma concentração inicial de 1 mol !$ L^{-1} !$ e a uma temperatura constante de 25 ºC. Água oxigenada é uma solução aquosa de peróxido de hidrogênio. Nesse experimento, a quantidade de peróxido de hidrogênio presente em um tempo escolhido t foi determinada através de titulações com permanganato de potássio, !$ KMnO_4 !$, de alíquotas de 5 mL de solução acidificada de água oxigenada. Os resultados obtidos são mostrados na tabela abaixo.
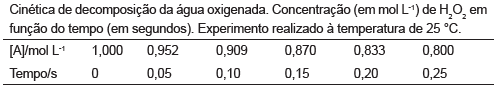
Com os dados apresentados acima e seus conhecimentos básicos de processos cinéticos, podemos afirmar que:
1. A velocidade média desta reação no intervalo de 0,10 s a 0,15 s é -0,78 mol !$ L^{-1} !$ !$ S^{-1} !$ .
2. A velocidade da reação de decomposição da água oxigenada diminui a medida que o tempo aumenta.
3. Utilizando-se as mesmas condições iniciais para a concentração da água oxigenada, a velocidade de reação de decomposição catalisada com !$ FeCl_3 !$ seria idêntica para um experimento conduzido à tempertura de 42º C.
4. A velocidade dessa reação química não deve alterar-se se ions iodeto !$ I^- !$ são utilizados como catalisador em lugar do !$ FeCl_3 !$.
Dessas, são VERDADEIRAS as afirmativas:
Provas
Questão presente nas seguintes provas
Readaptação é
Provas
Questão presente nas seguintes provas
A fixação do !$ CO_2 !$ pelos oceanos se dá através da dissolução do gás na água e por fotossíntese. A dissolução desse gás em água pode ser expressa pelas seguintes reações químicas:
!$ CO_2(g) !$ !$ \rightleftarrows !$ !$ CO_2(aq) !$ !$ K_{eq} !$ !$ = 3,4x10^{-2} !$
!$ CO_2(aq) !$ !$ + !$ !$ H_2O(l) !$ !$ \rightleftarrows !$ !$ H_2CO_3(aq) !$ !$ K_{eq} !$ !$ = 2,0x10^{-3} !$
!$ H_2CO_3(aq) !$ !$ + !$ !$ H_2O(l) !$ !$ \rightleftarrows !$ !$ H_3O^+(l) !$ !$ + !$ !$ HCO^-_3(aq) !$ !$ K_{al} !$ !$ = 4,3x10^{-7} !$
!$ HCO^-_3(aq) !$ !$ + !$ !$ H_2O(l) !$ !$ \rightleftarrows !$ !$ H_3O^+(l) !$ !$ CO^{2-}_3(aq) !$ !$ K_{a2} !$ !$ = 5,0x10^{-11} !$
As constantes de equilíbrio são dadas para temperatura de 20ºC e pressão de 1 atm.
Dessas informações, podemos observar que a espécie predominante no mar dependerá do pH da água, dos equilíbrios alcançados, da temperatura e da pressão atmosférica.
Desses dados, é CORRETO concluir que
Provas
Questão presente nas seguintes provas
Escala Celsius
Para que possamos medir temperaturas, será necessário graduar o termômetro, isto é, marcar nele as divisões e atribuir números a essas divisões. Quando procedemos dessa maneira, estamos construindo uma escala termométrica.
Na construção de uma determinada escala termométrica, são adotadas convenções arbitrárias. Por isso, várias escalas termométricas diferentes foram surgindo, com o decorrer do tempo, em vários países. Essa variedade de escalas termométricas, naturalmente, acarretava uma série de inconvenientes ao trabalho científico. Para superar essas dificuldades, os cientistas sugeriram a adoção de uma escala única, baseada em convenções internacionais – a escala Celsius (anteriormente denominada escala centígrada), atualmente adotada em quase todos os países do mundo.
LUZ, Antônio Máximo Ribeiro da.; ÁLVARES, Beatriz Alvarenga. Curso de Física, volume 2. 6. ed. São
Paulo: Scipione, 2006.
Paulo: Scipione, 2006.
A leitura deste texto pressupõe o conhecimento da seguinte definição:
Provas
Questão presente nas seguintes provas
A halita é um mineral com hábito cúbico contendo o equivalente a 4 íons de sódio e 4 íons cloretos na sua célula unitária. À temperatura ambiente e a uma pressão superior a 1 atm, a aresta e o volume da célula unitária da halita são, respectivamente, !$ 0,55 !$ !$ nm !$ e !$ 0,166 !$ !$ nm^3 !$.
Nessas condições de temperatura e pressão, a densidade da halita é
Provas
Questão presente nas seguintes provas
Numere a segunda coluna de acordo com a primeira coluna. Faça a correspondência entre as substâncias indicadas pelas fórmulas moleculares na primeira coluna e suas respectivas propriedades químicas, apresentadas na segunda coluna:
(1) !$ NH_4Cl !$
(2) !$ KOH !$
(3) !$ HClO_4 !$
(4) !$ CH_3COONa !$
(5) !$ NaNO_3 !$
(6) !$ (CH_3)_3N !$
(7) !$ HCN !$
( ) Ácido fraco
( ) Sal neutro
( ) Sal de reação básica
( ) Base forte
( ) Ácido forte
( ) Base fraca
( ) Sal de reação ácida
A correspondência CORRETA é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container