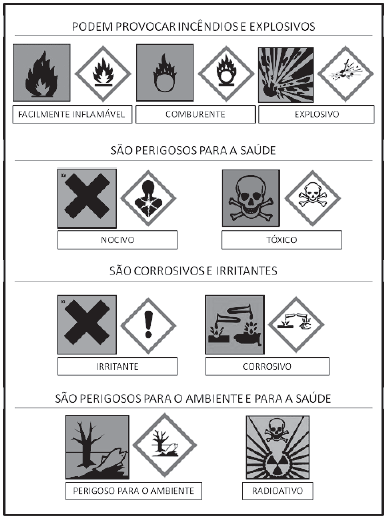
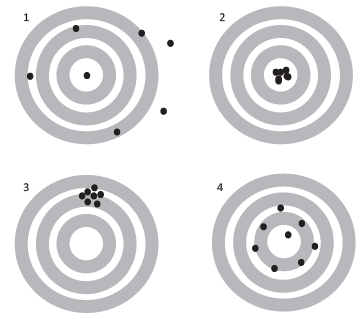
A volumetria de complexação é um método analítico quantitativo que envolve reações químicas entre um grande número de íons e ligantes orgânicos específicos, formando complexos estáveis.
Essa técnica tem alcance de milimols que, com o uso de ligantes auxiliares adequados e controle do pH, permite a seletividade analítica desejada. Essas características conferem ao método um ótimo custo e eficácia na determinação de íons metálicos presentes em soluções aquosas.
Um agente quelante muito empregado nessa técnica, introduzido na segunda metade da década de quarenta do século passado, é o ácido etilenodiaminotetracético (EDTA), fórmula molecular !$ C_{10}H_{16}N_2O_8 !$, que complexa com vários íons, incluindo metais pesados e alcalino terrosos, formando estruturas estáveis do tipo 1:1.
Do processo molecular de complexação do EDTA com íons metálicos, pode-se inferir que
I. a eficiência da volumetria de complexação com o EDTA depende do pH da solução e, para a maioria dos íons metálicos divalentes, deve ser realizada em meio básico.
II. o EDTA é um composto orgânico que tem uma estrutura molecular heterocíclica saturada que permite um arranjo geométrico ideal em torno do centro metálico na complexação.
III. os íons metálicos funcionam como ácidos de Lewis receptores de pares de elétrons de um grupo ou grupos doadores de elétrons do EDTA que funcionam como centros basicos de Lewis.
IV. o EDTA dispõe de 2 (dois) centros de complexão localizado sobre os átomos de nitrogênio e 4 (quatro) outros sobre os átomos de oxigênio dos grupos carboxílicos.
Dessas inferências, está CORRETO o conjunto de inferências: