Foram encontradas 1.390 questões.
A dimensão 78 j7 apresenta os seguintes afastamentos superior e inferior 18 !$ \mu !$m e -12 !$ \mu !$m, respectivamente.
As dimensões máxima e mínima, em mm, são:
Provas
O ajuste 87 H10/f9 apresenta os seguintes afastamentos:
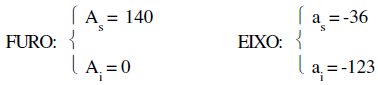
A tolerância de funcionamento do conjunto é:
Provas
A simbologia 65 G9/h8 representa o seguinte ajuste:
Provas
A determinação dos parâmetros da lei de formação da curva característica de funcionamento inerente ao desempenho de um equipamento ou instrumento de medição, de acordo com o INMETRO, é denominado de:
Provas
O conjunto de operações que tem por objetivo determinar o valor de uma grandeza é denominado:
Provas
O ferro é o metal mais usado com 95% em peso da produção mundial de metal. É indispensável devido ao seu baixo preço e dureza, especialmente empregado em automóveis, barcos e componentes estruturais de edifícios. No entanto, o ferro elementar é raramente encontrado na natureza mas pode ser encontrado na forma de óxidos ferroso e férrico (FeO e Fe2O3, respectivamente).
Assim, as configurações eletrônicas do Fe, Fe2+ e Fe3+ são, respectivamente:
Provas
Um método de determinação do teor de titânio em uma amostra de óxido de titânio, TiO2 (massa molar = 80 g/mol), produto químico industrial importante, é reagir a amostra com trifluoreto de bromo líquido. A reação resultante produz tetrafluoreto de titânio sólido, bromo líquido e oxigênio gasoso. Esse gás é liberado de maneira quantitativa e pode ser facilmente capturado e sua massa determinada.
Supondo que 1,6 g de amostra contendo TiO2 libere 0,32 g de O2, a porcentagem em massa de Ti na amostra é aproximadamente:
Provas
Em muitos cursos introdutórios de Química, uma parte do trabalho de laboratório é dedicada à análise qualitativa de soluções aquosas, a identificação de ânions e de cátions.
Com base na tabela de constante de solubilidade, Kps, abaixo:
| Composto | Kps a 25 ºC |
| Ag2S | 6 x 10−51 |
| CuS | 6 x 10−37 |
| PbS | 3 x 10−28 |
| AgCl | 2 x 10−10 |
| PbCl2 | 2 x 10−5 |
o objetivo de um técnico de laboratório é separar os íons metálicos, Ag+, Pb2+ e Cu2+ em três tubos de ensaio diferentes.
Para isso, na primeira etapa, ele adiciona HCl aquoso para formar um precipitado que é transferido para um outro tubo. Na segunda etapa, água quente é adicionada a esse precipitado formado, de forma que uma parte dele se dissolve, enquanto outra permanece insolúvel.
Assim, a ordem de separação dos íons metálicos é, respectivamente:
Provas
O poliacetato de vinila (PVA) é um polímero usado em tintas látex, adesivos e revestimentos têxteis. O seu monômero é o acetato de vinila cuja fórmula molecular é C4H6O2.
Na estrutura deste composto, ocorre que:
Provas
Considere os seguintes valores de pKa e pKb do ácido cítrico:
| Equilíbrio | pKa | pKb |
| H3C6H5O7 !$ \leftrightarrows !$ H+ + H2C6H5O7– | 2,1 | 11,9 |
| H2C6H5O7– !$ \leftrightarrows !$ H+ + HC6H5O72– | 4,8 | 9,2 |
| HC6H5O72– !$ \leftrightarrows !$ H+ + C6H5O73– | 6,4 | 7,6 |
Um técnico de laboratório precisa preparar 1 M de tampão citrato pH 6,4, porém ele só tem disponível em seu laboratório 100 mL de uma solução 1 M de citrato monoácido de sódio e pastilhas de hidróxido de sódio. Considerando que a massa de base adicionada não altere o volume da solução, a massa de hidróxido de sódio, em gramas, que ele deve adicionar àquela solução para preparar o tampão citrato pH 6,4, é:
Provas
Caderno Container