Foram encontradas 351 questões.
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.
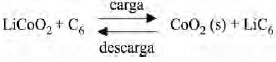
Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
O lítio é o elemento metálico da Tabela Periódica com a menor energia de ionização.
Provas
Para !$ n = 1, 2, 3, \cdots , !$, considere a sequência !$ b_n = 2^{a_n} !$, em que a sequência !$ a_n !$ é uma progressão aritmética (PA). Sabendo que 212 = 4.096, julgue o item seguinte.
Se !$ a_1 !$ = 0 e a soma dos seis primeiros termos da PA for igual a 30, então a soma dos seis primeiros termos da sequência !$ b_n !$ será superior a 1.300.
Provas
Para !$ n = 1, 2, 3, \cdots , !$, considere a sequência !$ b_n = 2^{a_n} !$, em que a sequência !$ a_n !$ é uma progressão aritmética (PA). Sabendo que 212 = 4.096, julgue o item seguinte.
Se a razão da PA for igual a 3, então a sequência !$ b_n !$ será uma progressão geométrica de razão igual a 8.
Provas
Para isolar o salicilato de metila sintetizado a partir do ácido salicílico foi adotado o seguinte procedimento:
I destilação para a remoção do metanol não reagido;
II dissolução da mistura restante em éter dietílico, um solvente orgânico volátil;
III lavagens sucessivas da solução etérea com solução aquosa de bicarbonato de sódio (NaHCO3) na concentração de 0,2 mol/L, para neutralizar e remover o catalisador ácido e o ácido salicílico não reagido;
IV secagem da solução etérea com MgSO4 anidro;
V destilação da solução para a remoção do éter.
As lavagens com a solução de bicarbonato de sódio, na etapa III, foram repetidas até que o ácido salicílico não reagido tivesse sido totalmente removido a partir da fração orgânica. Para essa certificação, a fase aquosa, depois de separada da fase orgânica, foi acidificada e, dessa forma, o equilíbrio mostrado a seguir foi deslocado para a direita, e gerou o ácido na forma não ionizada, que pode ser considerado insolúvel em meio aquoso.

Assim, enquanto a fração aquosa continha o íon salicilato, o ácido precipitava após a acidificação do meio. Terminada a precipitação, considerou-se que não havia mais ácido salicílico na solução e as lavagens puderam ser cessadas.
A partir dessas informações, assinale a opção correta.
O procedimento mais adequado para a separação das fases orgânica e aquosa obtidas na etapa III referida é a
Provas
Para isolar o salicilato de metila sintetizado a partir do ácido salicílico foi adotado o seguinte procedimento:
I destilação para a remoção do metanol não reagido;
II dissolução da mistura restante em éter dietílico, um solvente orgânico volátil;
III lavagens sucessivas da solução etérea com solução aquosa de bicarbonato de sódio (NaHCO3) na concentração de 0,2 mol/L, para neutralizar e remover o catalisador ácido e o ácido salicílico não reagido;
IV secagem da solução etérea com MgSO4 anidro;
V destilação da solução para a remoção do éter.
As lavagens com a solução de bicarbonato de sódio, na etapa III, foram repetidas até que o ácido salicílico não reagido tivesse sido totalmente removido a partir da fração orgânica. Para essa certificação, a fase aquosa, depois de separada da fase orgânica, foi acidificada e, dessa forma, o equilíbrio mostrado a seguir foi deslocado para a direita, e gerou o ácido na forma não ionizada, que pode ser considerado insolúvel em meio aquoso.

Assim, enquanto a fração aquosa continha o íon salicilato, o ácido precipitava após a acidificação do meio. Terminada a precipitação, considerou-se que não havia mais ácido salicílico na solução e as lavagens puderam ser cessadas.
A partir dessas informações, julgue o item.
Uma solução aquosa de bicarbonato de sódio 0,20 mol/L pode ser preparada dissolvendo-se 8,40 g do soluto em água suficiente para a obtenção de 500,0 mL de solução.
Provas
Para isolar o salicilato de metila sintetizado a partir do ácido salicílico foi adotado o seguinte procedimento:
I destilação para a remoção do metanol não reagido;
II dissolução da mistura restante em éter dietílico, um solvente orgânico volátil;
III lavagens sucessivas da solução etérea com solução aquosa de bicarbonato de sódio (NaHCO3) na concentração de 0,2 mol/L, para neutralizar e remover o catalisador ácido e o ácido salicílico não reagido;
IV secagem da solução etérea com MgSO4 anidro;
V destilação da solução para a remoção do éter.
As lavagens com a solução de bicarbonato de sódio, na etapa III, foram repetidas até que o ácido salicílico não reagido tivesse sido totalmente removido a partir da fração orgânica. Para essa certificação, a fase aquosa, depois de separada da fase orgânica, foi acidificada e, dessa forma, o equilíbrio mostrado a seguir foi deslocado para a direita, e gerou o ácido na forma não ionizada, que pode ser considerado insolúvel em meio aquoso.

Assim, enquanto a fração aquosa continha o íon salicilato, o ácido precipitava após a acidificação do meio. Terminada a precipitação, considerou-se que não havia mais ácido salicílico na solução e as lavagens puderam ser cessadas.
A partir dessas informações, julgue o item.
O MgSO4 é um sal inorgânico e sua nomenclatura oficial é sulfeto de magnésio.
Provas
Para isolar o salicilato de metila sintetizado a partir do ácido salicílico foi adotado o seguinte procedimento:
I destilação para a remoção do metanol não reagido;
II dissolução da mistura restante em éter dietílico, um solvente orgânico volátil;
III lavagens sucessivas da solução etérea com solução aquosa de bicarbonato de sódio (NaHCO3) na concentração de 0,2 mol/L, para neutralizar e remover o catalisador ácido e o ácido salicílico não reagido;
IV secagem da solução etérea com MgSO4 anidro;
V destilação da solução para a remoção do éter.
As lavagens com a solução de bicarbonato de sódio, na etapa III, foram repetidas até que o ácido salicílico não reagido tivesse sido totalmente removido a partir da fração orgânica. Para essa certificação, a fase aquosa, depois de separada da fase orgânica, foi acidificada e, dessa forma, o equilíbrio mostrado a seguir foi deslocado para a direita, e gerou o ácido na forma não ionizada, que pode ser considerado insolúvel em meio aquoso.

Assim, enquanto a fração aquosa continha o íon salicilato, o ácido precipitava após a acidificação do meio. Terminada a precipitação, considerou-se que não havia mais ácido salicílico na solução e as lavagens puderam ser cessadas.
A partir dessas informações, julgue o item.
Considere que a solução em questão tenha comportamento ideal e que a constante de acidez do ácido salicílico seja igual a 1,0×10-3. Nesse caso, se o pH de uma solução do ácido salicílico for reduzido a 2,0, então o grau de ionização do ácido será superior a 12%.
Provas
Para isolar o salicilato de metila sintetizado a partir do ácido salicílico foi adotado o seguinte procedimento:
I destilação para a remoção do metanol não reagido;
II dissolução da mistura restante em éter dietílico, um solvente orgânico volátil;
III lavagens sucessivas da solução etérea com solução aquosa de bicarbonato de sódio (NaHCO3) na concentração de 0,2 mol/L, para neutralizar e remover o catalisador ácido e o ácido salicílico não reagido;
IV secagem da solução etérea com MgSO4 anidro;
V destilação da solução para a remoção do éter.
As lavagens com a solução de bicarbonato de sódio, na etapa III, foram repetidas até que o ácido salicílico não reagido tivesse sido totalmente removido a partir da fração orgânica. Para essa certificação, a fase aquosa, depois de separada da fase orgânica, foi acidificada e, dessa forma, o equilíbrio mostrado a seguir foi deslocado para a direita, e gerou o ácido na forma não ionizada, que pode ser considerado insolúvel em meio aquoso.

Assim, enquanto a fração aquosa continha o íon salicilato, o ácido precipitava após a acidificação do meio. Terminada a precipitação, considerou-se que não havia mais ácido salicílico na solução e as lavagens puderam ser cessadas.
A partir dessas informações, julgue o item.
A equação a seguir, em que o H2CO3 gerado pode posteriormente decompor-se em CO2 (g) e H2O (l), é a equação balanceada para a reação de neutralização do ácido sulfúrico pelo bicarbonato de sódio.
H2SO4 (aq) + 2NaHCO3 (aq) → 2H2CO3 (aq) + Na2SO4 (aq)
Provas
A síntese do salicilato de metila foi realizada com a adição de ácido salicílico e metanol em excesso. Como catalisador, foram adicionados 10,0 mL de uma solução concentrada de ácido sulfúrico (H2SO4) com densidade igual a 1,83 g/mL e concentração de 98% em massa.
A respeito desse processo, julgue o item que se segue.
A massa de ácido sulfúrico presente nos 10,0 mL da solução empregada no processo é superior a 18,0 g.
Provas
A síntese do salicilato de metila foi realizada com a adição de ácido salicílico e metanol em excesso. Como catalisador, foram adicionados 10,0 mL de uma solução concentrada de ácido sulfúrico (H2SO4) com densidade igual a 1,83 g/mL e concentração de 98% em massa.
A respeito desse processo, julgue o item que se segue.
O emprego de metanol em excesso desloca o equilíbrio químico da reação no sentido da formação dos produtos e, dessa forma, contribui para aumentar o grau de conversão do ácido salicílico em salicilato de metila.
Provas
Caderno Container