Foram encontradas 375 questões.
Duas crianças X e Y brincam sentadas na extremidade de uma gangorra, conforme mostra o esquema abaixo.
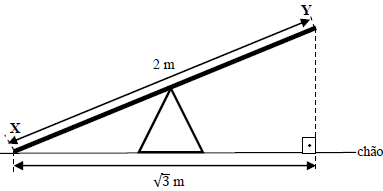
Quando a criança Y estiver no ponto mais alto, qual a distância que ela estará do chão?
Provas
As informações presentes nos rótulos de recipientes que contêm produtos químicos são extremamente valiosas, e a sua leitura atenta poderá evitar o uso inadequado de substâncias que venham causar sérios acidentes. Leia o rótulo abaixo.
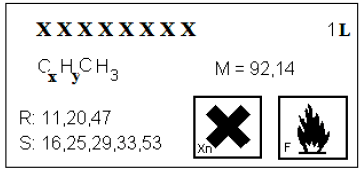
A leitura desse rótulo identifica tratar-se de uma substância
Provas
O vinagre é uma solução de ácido acético de 4 % a 6 % que, além da aplicação na culinária como condimento, possui uma suposta aplicação terapêutica que traria benefícios para artrite, osteoporose, reumatismo entre diversas outras doenças. Pode ser considerado uma solução em que em 1 litro estão dissolvidos 42 g do ácido. Esse ácido é fraco e possui constante de ionização igual a 1,8 x 10-5 a 25 ºC. Nessa temperatura, o grau de ionização do ácido (em %) e a concentração molar de íons H+ no vinagre são, aproximadamente:
Provas
O silício é o segundo elemento mais abundante da crosta terrestre: 26 a 28 % dela são compostos desse elemento. É um componente essencial da grande maioria das rochas que formam a crosta terrestre. Um átomo de silício tem raio de cerca de 111 pm. Considerando os átomos com forma esférica, quantos átomos de silício deveriam ser alinhados para formar uma reta de 11,1 m?
Provas
Analise as quatro soluções aquosas diluídas.
I - Solução 0,01 molal de glicose (mol = 180 g)
II - Solução 0,001 molar de sacarose (mol = 342 g)
III - Solução com 1,8 g/L de frutose (mol = 180 g)
IV - Solução de 17,1 g de maltose (mol = 342 g) em 500 g de água
Assinale a alternativa que melhor relaciona as temperaturas de ebulição (T) das soluções.
Provas
A altas temperaturas, gás nitrogênio reage com gás oxigênio produzindo monóxido de nitrogênio, um poluente atmosférico. Durante a queima de combustível no motor de um carro, por exemplo, a temperatura é muito elevada, fornecendo a energia necessária para que ocorra a formação do monóxido de nitrogênio de forma eficiente:
!$ N_2(g) + O_2(g) \rightleftharpoons 2\,NO(g)\,\,\,\,\,\,\,K_C = 1,0 x10^{-5}à\,1.200^{ \circ} C !$
Com base no exposto, pode-se afirmar:
Provas
Durante o funcionamento de uma célula voltaica para a produção de energia elétrica, são observados, à medida que ela descarrega, ou seja, conforme os reagentes são convertidos em produtos, alguns fatos. Sobre eles, analise as afirmativas.
I - Se a concentração dos produtos aumenta, a reação da célula se torna mais espontânea e a voltagem aumenta.
II - Se a concentração dos produtos diminui, a reação da célula se torna menos espontânea e a voltagem diminui.
III - A voltagem gradualmente cai a partir da voltagem padrão, tornado-se nula quando o equilíbrio é alcançado.
IV - A constante de equilíbrio de uma reação redox pode ser obtida a partir do valor da voltagem padrão para a reação.
Nessa situação, são fatos observados:
Provas
| Dados: Considere, a 25º C e a 1 atm, a tabela:
|
A reação de formação do gás d'água apresenta-se como uma maneira de produzir um combustível gasoso a partir do carvão !$ C(S) + H_2O(g) \rightarrow CO(g) + H_2(g) !$. A temperatura para a qual essa reação está em equilíbrio, é, aproximadamente, em ºC:
Provas
O pentóxido de dinitrogênio, N2O5, é um forte agente oxidante que forma misturas explosivas com compostos orgânicos e sais de amônio. Em temperaturas elevadas, esse instável composto binário se decompõe em dióxido de nitrogênio e oxigênio. Durante a realização de um experimento de decomposição desse pentóxido, um técnico montou uma tabela que apresenta o número de mols dos participantes em função do tempo, cujas lacunas você deve preencher.
| !$ \mathbf{ 2\,N_2O_5 \rightarrow 4 NO_2 + O_2} !$ | |||
| Início | 5 mols | ||
| Reação | |||
| Equilíbrio | 3 mols | ||
O gráfico que representa o número de mols dos participantes da reação na ordenada e o tempo na abscissa, quando a reação alcançar o equilíbrio, é:
Provas
Em relação aos estudos cinéticos de uma reação química, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A molecularidade é igual à ordem de uma reação apenas no caso de processos elementares.
( ) A velocidade de uma reação global, quando composta de várias etapas, é determinada pela soma das velocidades individuais das etapas.
( ) De modo geral, o aumento da velocidade de uma reação, por meio da elevação de temperatura, ocorre porque aumenta a velocidade média das moléculas reagentes.
( ) Toda reação é produzida por colisões, mas nem toda colisão gera uma reação.
Assinale a sequência correta.
Provas
Caderno Container