Foram encontradas 13.241 questões.
Os espectros na região do UV-Visível de dois hidrocarbonetos aromáticos polinucleares, A e B, são mostrados a seguir.
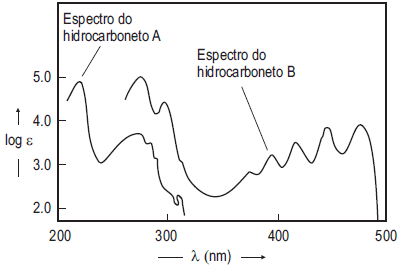
A partir do gráfico acima, considere as afirmativas a seguir.
I - O espectro A corresponde ao hidrocarboneto que apresenta maior conjugação.
II - O hidrocarboneto A é incolor.
III - O hidrocarboneto B é colorido.
Sabendo-se que a região do visível compreende a faixa de 380-780nm, a análise dos espectros permite concluir que está(ão) correta(s) APENAS a(s) afirmativa(s)
Provas
Em relação às temperaturas de transição vítrea, Tg, e de fusão cristalina, Tm, de polímeros, analise as afirmativas a seguir.
I - A Tg é maior que Tm sempre.
II - A Tm é a temperatura onde os cristalitos e esferulitos das cadeias macromoleculares se desagregam e fundem.
III - Em temperaturas inferiores à Tg, a mobilidade das cadeias macromoleculares desaparece, e o material se torna mais rígido.
IV - Todas as borrachas têm Tg acima da temperatura ambiente ( 25 °C).
Estão corretas APENAS as afirmativas
Provas
O gráfico abaixo representa uma curva típica obtida por análise térmica diferencial (DTA) para um sistema vítreo.
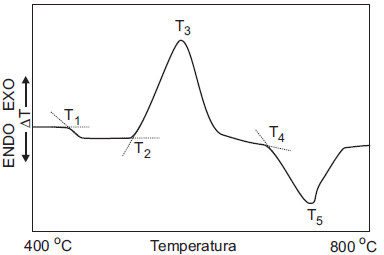
Dentre as temperaturas assinaladas, aquela que pode corresponder à temperatura de transição vítrea (Tg) é
Provas
O gráfico abaixo mostra a curva de neutralização de 50mL de ácido ortofosfórico 0,1 mol/L, com hidróxido de potássio 0,1mol/L, determinada por titulação potenciométrica.
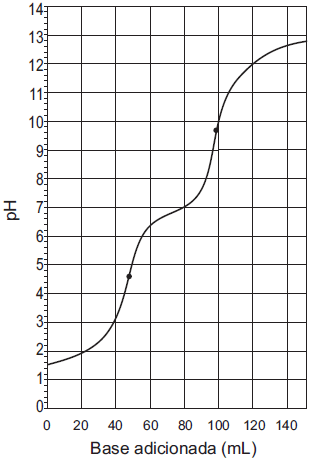
Analisando-se o gráfico, conclui-se que
Provas
A eletrosmose pode influenciar a eficiência e a reprodutibilidade das técnicas de separação eletrocinética. Na eletroforese capilar, a velocidade do fluxo eletrosmótico diminui quando a(o)
Provas
O ácido tereftálico (TPA) é obtido industrialmente pela oxidação de p-xileno. A reação ocorre em fase líquida, em ácido acético, a 204 ºC e 200 psi, em presença dos catalisadores acetato de cobalto e acetato de manganês e de brometo de sódio. O tempo de reação é de cerca de uma hora. O TPA é pouco solúvel em ácido acético e seus cristais são continuamente removidos do meio durante a reação. Uma carga de 318 t de p-xileno e 800 t de oxigênio gera 468 t de TPA nessas condições.
A respeito do processo descrito e das espécies envolvidas, foram feitas as seguintes afirmações:
I - O rendimento da reação situa-se entre 90-95%.
II - Existe um excesso de 30% de p-xileno em relação à estequiometria da reação.
III - Se for utilizado ar atmosférico como fonte de oxigênio, serão injetados 108 mols de nitrogênio no sistema.
Considere:
• Massas molares (em g/mol): C = 12; H = 1; O = 16;
• Composição molar do ar atmosférico: 20% de O2 e 80% de N2
Está(ão) correta(s) APENAS a(s) afirmativa(s)
Provas
A medida da condutância de soluções eletrolíticas, feitas a partir de dois eletrodos de platina imersos numa solução eletrolítica, é afetada pelos seguintes fatores:
Provas
Um técnico preparou uma solução homogênea de um determinado corante azul em balão volumétrico, de tal forma que era possível observar através do frasco. Ele reparou, no entanto, que a coloração da solução era mais intensa na parte inferior do balão e menos intensa no gargalo do frasco. Esse fenômeno é resultado do efeito da (o)
Provas
É procedimento de calibração de um espectrofotômetro ajustar o
Provas
O ferro é um micronutriente para os seres vivos, participando de uma série de processos bioquímicos dentro dos organismos vivos. O estado de oxidação em que se encontra exerce importância fundamental nesses processos, o que torna imprescindível a diferenciação entre as concentrações de Fe2+ e Fe3+ encontradas em solução, cujo procedimento analítico é denominado análise de especiação.
A fim de realizar a determinação das concentrações de Fe2+ e Fe3+ em uma amostra de água de poço, um analista químico explorou a reação entre o íon Fe2+ e o complexante orgânico 1,10-fenantrolina (C12H8N2), em pH 4,5, para formação de um complexo de cor alaranjada, com máximo de absorção em 510 nm. Nessas condições, o íon Fe3+ não reage com a 1,10-fenantrolina. Na reação entre Fe2+ e a 1,10-fenantrolina, apresentada abaixo, X representa a 1,10-fenantrolina e [FeX3]2+, o complexo formado.
Fe2+ + 3X !$ \rightleftharpoons !$ [FeX3]2+
O procedimento experimental adotado envolveu a construção de uma curva analítica, a partir de soluções padrões de Fe a 510 nm, com cubetas de 1,0 cm, cuja equação foi A = 0,50 C (mg Fe/L) + 0,0001; R2 = 0,9998.
As soluções oriundas da amostra foram preparadas a partir de alíquotas de 25,00 mL, acrescidas ou não de soluções tampão, ácido ascórbico a 2%, X a 1% e água deionizada até o traço de aferição do balão de 50,00 mL. Os volumes e as respectivas absorvâncias, nas mesmas condições espectrofotométricas, estão discriminadas na tabela abaixo.
| Volume da |
Tampão (pH=4,5) |
Ac. ascórbico (2% m/v) |
X (1% m/v) |
Volume final (1% m/v) |
A |
| 25,00 mL |
5,00 mL | 2,00 mL | 1,00 mL | 50,00 mL | 0,50 |
| 25,00 mL |
5,00 mL | 0 mL | 1,00 mL | 50,00 mL | 0,20 |
Considerando-se que o ácido ascórbico, nas condições de medida, é capaz de reduzir todo o Fe3+ a Fe2+, as concentrações dessas espécies na água de poço original são, em mg/L, respectivamente,
| Fe2+ | Fe3+ |
Provas
Caderno Container