Foram encontradas 47.565 questões.
Considerando que os medicamentos possuem seus
prazos de validade definidos por meio de estudos de estabilidade e que embalagens multidoses podem apresentar
requisitos especiais de conservação após a sua abertura,
é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
A RDC Nº 658 de 2022 considera que o Sistema de
Qualidade Farmacêutico pode se estender ao estágio
do desenvolvimento tecnológico de forma a fortalecer o
vínculo entre estas partes. Sobre a documentação técnica
da qualidade para fins de registro de medicamentos, é
INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
O desenvolvimento e a validação de métodos analíticos físicos e físico-químicos é parte fundamental de uma
estratégia de controle projetada para garantir que um medicamento de qualidade seja produzido consistentemente.
Uma vez que a RDC Nº 658 de 2022 considera que a
validação de métodos analíticos é um requerimento básico
do controle de qualidade de um medicamento, é INCORRETO afirmar que
Provas
Questão presente nas seguintes provas
Ao apresentar um estudo de estabilidade no peticionamento de um pedido de registro ou pós-registro de um
medicamento, a empresa solicitante deve apresentar os
itens abaixo, EXCETO:
Provas
Questão presente nas seguintes provas
Avalie se as afirmações abaixo são verdadeiras(V) ou
falsas(F) quanto aos estudos de fotoestabilidade:
I- A fotodegradação pode ocorrer por diversos mecanismos, alguns dos quais não são dependentes da quantidade de luz que o sistema é exposto. Assim, pode-se inferir que algumas reações de fotodegradação ocorrem mesmo se a exposição for a pequena quantidade de luz.
II- A luz pode atuar apenas como promotor de uma reação de degradação do ativo em um medicamento, que continua a ocorrer mesmo depois de cessada a exposição.
III- O estudo de fotoestabilidade, de acordo com o preconizado pela RDC 318 de 06 de novembro de 2019, baseia-se na exposição do produto a uma grande quantidade de luz em um curto período de tempo ao passo que na vida real do medicamento a exposição se dá a uma pequena quantidade de luz por um longo período de tempo.
IV- Em um estudo de fotoestabilidade o medicamento em desenvolvimento deve ser exposto tanto à incidência de luz visível (cuja unidade de luminosidade é o lux) quanto para a luz ultravioleta (cuja unidade de radiação é watt.horas/m2).
A ordem correta, de cima para baixo, é:
I- A fotodegradação pode ocorrer por diversos mecanismos, alguns dos quais não são dependentes da quantidade de luz que o sistema é exposto. Assim, pode-se inferir que algumas reações de fotodegradação ocorrem mesmo se a exposição for a pequena quantidade de luz.
II- A luz pode atuar apenas como promotor de uma reação de degradação do ativo em um medicamento, que continua a ocorrer mesmo depois de cessada a exposição.
III- O estudo de fotoestabilidade, de acordo com o preconizado pela RDC 318 de 06 de novembro de 2019, baseia-se na exposição do produto a uma grande quantidade de luz em um curto período de tempo ao passo que na vida real do medicamento a exposição se dá a uma pequena quantidade de luz por um longo período de tempo.
IV- Em um estudo de fotoestabilidade o medicamento em desenvolvimento deve ser exposto tanto à incidência de luz visível (cuja unidade de luminosidade é o lux) quanto para a luz ultravioleta (cuja unidade de radiação é watt.horas/m2).
A ordem correta, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
De acordo com o Guia número 28 de 11 de novembro
de 2019, o estudo de estabilidade de insumos farmacêuticos ativos e de medicamentos tem o objetivo de fornecer
evidências sobre como a qualidade dos produtos varia ao
longo do tempo, quando sob influência de diversos fatores
ambientais. Sobre os estudos de estabilidade de medicamentos, de acordo com a RDC 318 de 06 de novembro de
2019, é correto afirmar que:
Provas
Questão presente nas seguintes provas
Avalie os resultados abaixo, conforme o preconizado pela RDC 318 de 6 de novembro de 2019, que estabelece os
critérios para a realização de estudos de estabilidade de insumos farmacêuticos ativos e medicamentos, exceto biológicos,
e dá outras providências.
Resultados de estudo de estabilidade acelerada (40°C ± 2°C / 75% UR ± 5% UR) do medicamento X 150 mg/comprimidos
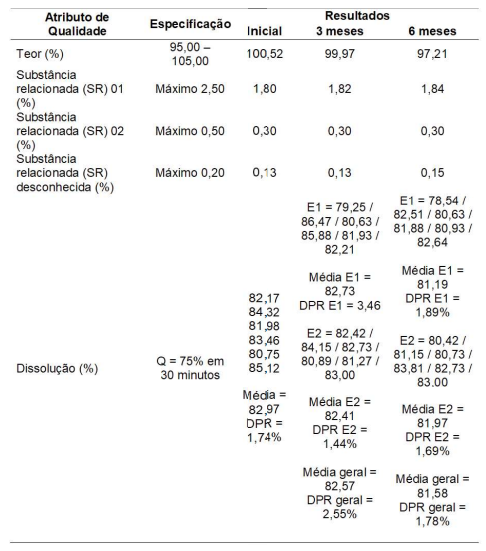
Sobre o estudo de estabilidade acima, avalie se são verdadeiras (V) ou falsas (F) as afirmações a seguir:
I – O medicamento X apresenta queda de teor no estudo de estabilidade acelerada. Por este motivo o estudo de estabilidade está reprovado.
II – É uma hipótese plausível que a SR 02 seja oriunda unicamente da síntese do IFA do medicamento.
III – É uma hipótese plausível que a SR 01 seja oriunda da degradação do fotolítica do IFA.
IV – Pelo conjunto dos resultados, pode-se concluir que o estudo de estabilidade acelerada atende aos requisitos para sua aprovação em conformidade com a zona climática II.
V – O estudo está aprovado frente aos requisitos da RDC 318/2019.
VI – Os resultados do ensaio de dissolução nas frequências de 3 e 6 meses estão reprovados em primeiro estágio.
De cima para baixo a ordem correta é:
Resultados de estudo de estabilidade acelerada (40°C ± 2°C / 75% UR ± 5% UR) do medicamento X 150 mg/comprimidos

Sobre o estudo de estabilidade acima, avalie se são verdadeiras (V) ou falsas (F) as afirmações a seguir:
I – O medicamento X apresenta queda de teor no estudo de estabilidade acelerada. Por este motivo o estudo de estabilidade está reprovado.
II – É uma hipótese plausível que a SR 02 seja oriunda unicamente da síntese do IFA do medicamento.
III – É uma hipótese plausível que a SR 01 seja oriunda da degradação do fotolítica do IFA.
IV – Pelo conjunto dos resultados, pode-se concluir que o estudo de estabilidade acelerada atende aos requisitos para sua aprovação em conformidade com a zona climática II.
V – O estudo está aprovado frente aos requisitos da RDC 318/2019.
VI – Os resultados do ensaio de dissolução nas frequências de 3 e 6 meses estão reprovados em primeiro estágio.
De cima para baixo a ordem correta é:
Provas
Questão presente nas seguintes provas
Foi aberto um projeto de desenvolvimento de um medicamento contendo um antirretroviral da classe II do sistema
de classificação biofarmacêutica, fabricado como comprimidos de liberação imediata. Durante o desenvolvimento do
produto, foram avaliados os perfis de dissolução em 12 cubas nas condições descritas em monografia farmacopeica
sendo elas: 900 mL de meio tampão acetato pH 4,5 com
0,5% de lauril sulfato de sódio a 37 ºC, aparato cesta com
rotação de 75 rpm e com a quantificação por espectroscopia no ultravioleta-visível. Diferentes formulações foram
avaliadas e todas apresentaram semelhança no perfil de
dissolução, porém, foi observado um desvio padrão relativo
maior do que 20% nos primeiros tempos do perfil (5 e 10
minutos) e maior do que 10% nos demais tempos do perfil
(15, 30 e 45 minutos). Sobre o ensaio de perfil dissolução
em questão, pode-se afirmar que:
Provas
Questão presente nas seguintes provas
No desenvolvimento de um medicamento na forma
farmacêutica suspensão oral em veículo aquoso contendo
um insumo farmacêutico ativo (IFA) da classe II do sistema
de classificação biofarmacêutica, foram produzidos três
lotes experimentais sendo cada lote produzido com o IFA de
diferentes fabricantes. O Dossiê de Insumo Farmacêutico
Ativo (DIFA) dos três fabricantes apresenta a informação de
que o IFA é uma forma hidratada e apresenta informações
em relação à posição dos picos de difração em 2 teta. Estão
descritos no DIFA do fabricante A picos de difração em 5,5°,
7,2°, 12,8°, 15,7° e 21,4° com a análise feita com radiação
de cobre (λ =1,5406 Å), no do fabricante B em 5,5°, 7,3°,
12,7°, 15,8° e 21,4° com a análise feita com radiação de
cobre (λ =1,5406 Å) e no do fabricante C em 2,5°, 11,4°,
17,6°, 18,2°, 19,1° e 24,3° com a análise feita com radiação
de cobalto (λ=1,7890 Å). Considerando o exposto, observe
as afirmativas abaixo:
I – É plausível afirmar que o IFA do fabricante B apresenta a mesma forma sólida do fabricante A, não sendo possível garantir que ambos contêm uma única forma sólida, uma vez que os padrões de difração de raios X não foram apresentados.
II – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes B e C podem apresentar diferentes graus de hidratação ou são polimorfos do hidrato de mesma estequiometria.
III – A titulação Karl-Fisher não permite a diferenciação da água de superfície e da água e incorporada na estrutura cristalina do hidrato.
IV – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes A, B e C podem ser selecionados para o desenvolvimento do produto, pois, já que as propriedades físico-químicas dos IFAs são as mesmas não haverá diferenças no desempenho da formulação.
V – É importante a avaliação da interconversão entre as formas sólidas do IFA, uma vez que, em suspensão, pode ocorrer a transição para a forma estável, resultando em crescimento cristalino com consequente alteração na distribuição do tamanho das partículas, o que pode afetar a estabilidade física da suspensão.
Das afirmativas acima:
I – É plausível afirmar que o IFA do fabricante B apresenta a mesma forma sólida do fabricante A, não sendo possível garantir que ambos contêm uma única forma sólida, uma vez que os padrões de difração de raios X não foram apresentados.
II – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes B e C podem apresentar diferentes graus de hidratação ou são polimorfos do hidrato de mesma estequiometria.
III – A titulação Karl-Fisher não permite a diferenciação da água de superfície e da água e incorporada na estrutura cristalina do hidrato.
IV – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes A, B e C podem ser selecionados para o desenvolvimento do produto, pois, já que as propriedades físico-químicas dos IFAs são as mesmas não haverá diferenças no desempenho da formulação.
V – É importante a avaliação da interconversão entre as formas sólidas do IFA, uma vez que, em suspensão, pode ocorrer a transição para a forma estável, resultando em crescimento cristalino com consequente alteração na distribuição do tamanho das partículas, o que pode afetar a estabilidade física da suspensão.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
As embalagens farmacêuticas desempenham papel
crucial na preservação da integridade dos medicamentos,
fornecendo proteção contra fatores ambientais como luz,
umidade e contaminação. Avalie as afirmativas abaixo sobre
materiais de embalagem primária de fármacos:
I – É permitido que a empresa solicite o registro de um medicamento em mais de um material de embalagem primária.
II – O vidro tipo I, também denominado vidro borossilicato, é o único tipo de vidro que pode ser utilizado para medicamentos de uso humano por ser totalmente inerte e não trazer riscos de incompatibilidade com a forma farmacêutica.
III – Polímeros termoplásticos podem ser usados para a tecnologia blow-fill-seal, na qual as etapas de formação da embalagem, enchimento com o produto farmacêutico e selagem do sistema final ocorrem em operação contínua.
IV – Embalagens termomoldáveis devem conter plastificantes em suas composições, permitindo a redução da temperatura de transição vítrea dos polímeros para que as temperaturas de processo possam ser reduzidas. São exemplos de plastificantes de embalagens termomoldáveis os ftalatos.
As afirmativas I, II e III e IV são respectivamente:
I – É permitido que a empresa solicite o registro de um medicamento em mais de um material de embalagem primária.
II – O vidro tipo I, também denominado vidro borossilicato, é o único tipo de vidro que pode ser utilizado para medicamentos de uso humano por ser totalmente inerte e não trazer riscos de incompatibilidade com a forma farmacêutica.
III – Polímeros termoplásticos podem ser usados para a tecnologia blow-fill-seal, na qual as etapas de formação da embalagem, enchimento com o produto farmacêutico e selagem do sistema final ocorrem em operação contínua.
IV – Embalagens termomoldáveis devem conter plastificantes em suas composições, permitindo a redução da temperatura de transição vítrea dos polímeros para que as temperaturas de processo possam ser reduzidas. São exemplos de plastificantes de embalagens termomoldáveis os ftalatos.
As afirmativas I, II e III e IV são respectivamente:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container