Foram encontradas 35.976 questões.
A acidez de um composto orgânico, quantificada pelo seu pKa, é profundamente influenciada por efeitos
eletrônicos que estabilizam sua base conjugada. O efeito indutivo, resultante da polarização de ligações σ por
grupos eletronegativos e o efeito de ressonância, que deslocaliza a carga negativa através de um sistema π,
são determinantes. Considere os quatro ácidos carboxílicos a seguir, cujas estruturas são bem estabelecidas
na literatura química.
Compostos:
I. Ácido acético (CH₃COOH) II. Ácido cloroacético (ClCH₂COOH) III. Ácido tricloroacético (Cl₃CCOOH) IV. Ácido benzóico (C₆H₅COOH)
A ordem crescente de acidez para estes compostos, justificada pela análise dos efeitos eletrônicos que atuam sobre a estabilidade de suas respectivas bases conjugadas, é:
Compostos:
I. Ácido acético (CH₃COOH) II. Ácido cloroacético (ClCH₂COOH) III. Ácido tricloroacético (Cl₃CCOOH) IV. Ácido benzóico (C₆H₅COOH)
A ordem crescente de acidez para estes compostos, justificada pela análise dos efeitos eletrônicos que atuam sobre a estabilidade de suas respectivas bases conjugadas, é:
Provas
Questão presente nas seguintes provas
Em um estudo sobre a bioatividade de enzimas que dependem de cofatores metálicos, um bioquímico precisa
preparar um meio reacional onde a concentração de íons magnésio (Mg²⁺) livres seja mantida abaixo de um
determinado limiar para evitar a inibição da enzima. Para isso, ele utiliza uma solução tampão de pH = 9,00 e
adiciona uma fonte de íons magnésio até o exato ponto de saturação, onde se inicia a precipitação do hidróxido
de magnésio (Mg(OH)₂).
Dados de Referência a 25 °C:
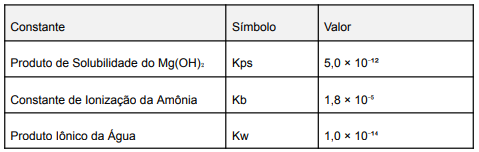
Nessas condições, a concentração máxima de íons magnésio (Mg²⁺) em mol·L⁻¹ que pode ser mantida em solução antes do início da precipitação é:
Dados de Referência a 25 °C:

Nessas condições, a concentração máxima de íons magnésio (Mg²⁺) em mol·L⁻¹ que pode ser mantida em solução antes do início da precipitação é:
Provas
Questão presente nas seguintes provas
O Urânio-238 (²³⁸U) decai naturalmente através de uma longa série radioativa até se estabilizar como
Chumbo-206 (²⁰⁶Pb). Este processo envolve múltiplas emissões de partículas alfa (α) e beta (β). A datação de
rochas ígneas pelo método Urânio-Chumbo baseia-se na razão entre as quantidades de ²⁰⁶Pb formado e de
²³⁸U remanescente. Sabendo que o tempo de meia-vida do ²³⁸U é de aproximadamente 4,5 x 10⁹ anos, um
geólogo analisou uma amostra de zircão e determinou que a razão molar entre o ²⁰⁶Pb e o ²³⁸U na amostra é
de 0,35. Considere log(2) ≈ 0,30 e log(0,74) ≈ -0,13
Considerando que todo o ²⁰⁶Pb na amostra foi formado a partir do decaimento do ²³⁸U, o número de partículas alfa emitidas na série de decaimento completa e a idade aproximada da rocha, respectivamente, são:
Considerando que todo o ²⁰⁶Pb na amostra foi formado a partir do decaimento do ²³⁸U, o número de partículas alfa emitidas na série de decaimento completa e a idade aproximada da rocha, respectivamente, são:
Provas
Questão presente nas seguintes provas
O acetato de trembolona é um éster do esteróide anabolizante trembolona que corresponde à designação
estra-4,9,11-trien-17β-acetato-3-ona (17β-acetoxi-estra-4,9,11-trien-3-ona), e é administrado, frequentemente,
via injeção em animais para aumento de massa muscular. Apesar de algumas pessoas utilizarem esse
composto injetável em humanos, tal prática não é recomendada e é proibida em diversos países, devido aos
riscos à saúde, incluindo alterações hormonais, cardiovasculares e comportamentais. Estudos relatam que, em
homens, o uso desse composto pode estar associado ao aumento da agressividade .
A fórmula estrutural abaixo corresponde ao acetato de trembolona.
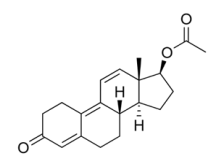
Fórmula estrutural do acetato de trembolona. Fonte: FUNCERN, 2025
Com base na análise dessa estrutura, a opção que indica, corretamente, as funções orgânicas, o tipo de insaturações e a natureza da cadeia carbônica presentes na molécula de acetato de trembolona é:
A fórmula estrutural abaixo corresponde ao acetato de trembolona.

Fórmula estrutural do acetato de trembolona. Fonte: FUNCERN, 2025
Com base na análise dessa estrutura, a opção que indica, corretamente, as funções orgânicas, o tipo de insaturações e a natureza da cadeia carbônica presentes na molécula de acetato de trembolona é:
Provas
Questão presente nas seguintes provas
Em ambientes biológicos, a diferença de concentração de solutos entre o interior da célula e o meio externo
está diretamente relacionada à pressão osmótica. Quando uma célula animal é colocada em uma solução
hipertônica, ocorre perda de água para o meio, levando à retração celular. Já em soluções hipotônicas, a
entrada excessiva de água pode provocar o rompimento da membrana plasmática. A variação de volume
celular em meios com diferentes concentrações de solutos ocorre devido ao fato de que a pressão osmótica
Provas
Questão presente nas seguintes provas
O tratamento de água de piscinas com compostos à base de cloro, como o hipoclorito de cálcio (Ca(OCl)₂),
pode elevar o pH do meio devido à hidrólise do íon hipoclorito (OCl⁻). Para neutralizar a alcalinidade, um sal de
caráter ácido, como o hidrogenossulfato de sódio (NaHSO₄), é adicionado.
Em uma piscina com 5,0 × 10⁵ litros de água, foram adicionados 1,2 kg de NaHSO₄. Assumindo a dissociação iônica completa do sal em solução e considerando as massas molares para Na, H, S e O como 23 g/mol, 1 g/mol, 32 g/mol e 16 g/mol, respectivamente, a concentração em mol por litro do íon sódio (Na⁺) resultante é
Em uma piscina com 5,0 × 10⁵ litros de água, foram adicionados 1,2 kg de NaHSO₄. Assumindo a dissociação iônica completa do sal em solução e considerando as massas molares para Na, H, S e O como 23 g/mol, 1 g/mol, 32 g/mol e 16 g/mol, respectivamente, a concentração em mol por litro do íon sódio (Na⁺) resultante é
Provas
Questão presente nas seguintes provas
A energia livre de Gibbs representa a máxima energia disponível para a realização de trabalho. A tabela a
seguir mostra os valores termodinâmicos para cálculo do ΔGº
reação
Tabela - Valores Termodinâmicos.

(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010).
Utilizando os valores de ΔH º f e Sº disponibilizados nessa tabela, o ΔGº reação para reação de formação de etino a 298K é de, aproximadamente:
Tabela - Valores Termodinâmicos.

(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010).
Utilizando os valores de ΔH º f e Sº disponibilizados nessa tabela, o ΔGº reação para reação de formação de etino a 298K é de, aproximadamente:
Provas
Questão presente nas seguintes provas
O ciclo do nitrogênio permite a ciclagem deste elemento no ambiente, disponibilizando-o para os seres vivos.
Os animais necessitam do nitrogênio incorporado em compostos orgânicos, enquanto plantas e algas
necessitam do nitrogênio sob a forma de íons nitrato ou amônio. Sobre este ciclo biogeoquímico, é correto
afirmar que a
Provas
Questão presente nas seguintes provas
Em uma certa reação química, obteve-se como um dos produtos uma substância gasosa. Após análise, foi
comprovado que tinha em sua massa 80% de carbono e 20% de hidrogênio. Verificou-se também que 0,5 L do
gás, nas CNTP, pesava 670 mg. A partir desses valores, considerando a constante dos gases ideais como
sendo R = 0,082 L.atm/K.mol, conclui-se que o valor aproximado da massa molar do gás e sua fórmula
empírica e molecular, respectivamente, são
Provas
Questão presente nas seguintes provas
Considere os dados apresentados a seguir.
CH3CH2CHO(g) + H2 (g) -→ CH3CH2CH2OH(g)
Tabela - Dados das Energias de Ligação Médias para ligações Simples e Múltiplas
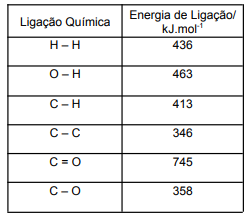
(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010.)
Estima-se que o valor da entalpia para reação de hidrogenação do propanal é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container