Foram encontradas 35.976 questões.
Leia o fragmento a seguir.
A qualidade da água de consumo humano é constantemente monitorada, e a determinação do teor de cloreto é uma etapa fundamental desse controle. Além do método de Mohr, outra estratégia clássica é o método de Volhard, no qual se adiciona excesso conhecido de solução padrão de nitrato de prata (AgNO₃) à amostra contendo íons cloreto. Após a formação completa do precipitado de cloreto de prata (AgCl), o excesso de prata em solução é titulado com solução padrão de tiocianato de potássio (KSCN), utilizando íons férricos (Fe³⁺) como indicador.
(Adaptado de VOGEL, Arthur I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020.)
Uma amostra de 25,0 mL de água de rio foi analisada pelo método de Volhard. Inicialmente, adicionou-se 30,0 mL de solução de AgNO₃ 0,0200 mol·L⁻¹ e após a precipitação de todo o Cl⁻ como AgCl, o excesso de Ag⁺ foi titulado com 8,0 mL de solução de KSCN 0,0150 mol·L⁻¹.
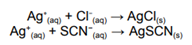
e as massas molares aproximadas: Ag = 108 g/mol, Cl = 35,5 g/mol, C = 12 g/mol, S = 32 g/mol e N = 14g/mol. A concentração de cloreto em mg·L⁻¹ na amostra é
Considerando as reações:
A qualidade da água de consumo humano é constantemente monitorada, e a determinação do teor de cloreto é uma etapa fundamental desse controle. Além do método de Mohr, outra estratégia clássica é o método de Volhard, no qual se adiciona excesso conhecido de solução padrão de nitrato de prata (AgNO₃) à amostra contendo íons cloreto. Após a formação completa do precipitado de cloreto de prata (AgCl), o excesso de prata em solução é titulado com solução padrão de tiocianato de potássio (KSCN), utilizando íons férricos (Fe³⁺) como indicador.
(Adaptado de VOGEL, Arthur I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020.)
Uma amostra de 25,0 mL de água de rio foi analisada pelo método de Volhard. Inicialmente, adicionou-se 30,0 mL de solução de AgNO₃ 0,0200 mol·L⁻¹ e após a precipitação de todo o Cl⁻ como AgCl, o excesso de Ag⁺ foi titulado com 8,0 mL de solução de KSCN 0,0150 mol·L⁻¹.
e as massas molares aproximadas: Ag = 108 g/mol, Cl = 35,5 g/mol, C = 12 g/mol, S = 32 g/mol e N = 14g/mol. A concentração de cloreto em mg·L⁻¹ na amostra é
Considerando as reações:
Provas
Questão presente nas seguintes provas
Na fase de purificação de um determinado composto orgânico obtido por síntese química, foi escolhida a
cristalização fracionada como método de separação. Sobre esse procedimento, é correto afirmar que
Provas
Questão presente nas seguintes provas
Em uma disciplina de Análise Química, os estudantes realizaram simulações virtuais de uma titulação
ácido-base. Durante a prática, observaram que o ponto de viragem indicado pelo software coincidia
exatamente com o ponto de equivalência teórico, sem apresentar variações. Quando a mesma titulação foi
realizada em um laboratório real, as titulações mostraram valores de volume gasto no ponto final ligeiramente
diferentes, mesmo entre grupos que usaram o mesmo ácido e a mesma base padronizada.
A discrepância entre o ambiente simulado e o ambiente real, pode ser explicada pelo fato de que,
A discrepância entre o ambiente simulado e o ambiente real, pode ser explicada pelo fato de que,
Provas
Questão presente nas seguintes provas
Um laboratorista que trabalha no controle de qualidade de uma indústria de bebidas, utiliza a
espectrofotometria UV-Vís, para determinar o teor de corante em bebidas artificiais. Considerando o princípio
da Lei de Lambert - Beer e suas limitações, assinale a opção correta.
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
A Espectrometria de Absorção Atômica (AAS) é uma técnica instrumental amplamente utilizada para determinar metais em baixas concentrações em amostras ambientais, alimentícias e biológicas. O princípio básico consiste em atomizar os elementos presentes na amostra — geralmente em uma chama ou em um forno de grafite — e medir a absorção de radiação emitida por uma lâmpada específica para o elemento de interesse. Como cada átomo possui níveis de energia eletrônica bem definidos, a absorção de luz em determinado comprimento de onda é característica de cada elemento químico, permitindo tanto a identificação quanto a quantificação.
(Adaptado de HARRIS,Daniel C. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020)
A técnica de Absorção Atômica é frequentemente aplicada em análises de metais pesados em alimentos e águas. Sobre o princípio de funcionamento da Espectrometria de Absorção Atômica, é correto afirmarmos que,
A Espectrometria de Absorção Atômica (AAS) é uma técnica instrumental amplamente utilizada para determinar metais em baixas concentrações em amostras ambientais, alimentícias e biológicas. O princípio básico consiste em atomizar os elementos presentes na amostra — geralmente em uma chama ou em um forno de grafite — e medir a absorção de radiação emitida por uma lâmpada específica para o elemento de interesse. Como cada átomo possui níveis de energia eletrônica bem definidos, a absorção de luz em determinado comprimento de onda é característica de cada elemento químico, permitindo tanto a identificação quanto a quantificação.
(Adaptado de HARRIS,Daniel C. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020)
A técnica de Absorção Atômica é frequentemente aplicada em análises de metais pesados em alimentos e águas. Sobre o princípio de funcionamento da Espectrometria de Absorção Atômica, é correto afirmarmos que,
Provas
Questão presente nas seguintes provas
Em uma aula de Análise Química, um estudante realizou a determinação gravimétrica do teor de cloreto (Cl
-
)
em uma amostra de água de uma lagoa. Para isso, diluiu a amostra em água destilada, isenta de cloretos, e
adicionou excesso de solução de nitrato de prata (AgNO3
), formando um precipitado branco de cloreto de prata
(AgCl), insolúvel em meio aquoso:
Ag⁺(aq) + Cl⁻(aq) → AgCl(s)
Após filtração, lavagem, secagem e pesagem, obteve-se 0,286 g de AgCl. Considerando as massa molares aproximadas: Ag = 108 g/mol; Cl = 35,5 g/mol; a massa de cloreto (Cl-) presente na amostra original é de
Ag⁺(aq) + Cl⁻(aq) → AgCl(s)
Após filtração, lavagem, secagem e pesagem, obteve-se 0,286 g de AgCl. Considerando as massa molares aproximadas: Ag = 108 g/mol; Cl = 35,5 g/mol; a massa de cloreto (Cl-) presente na amostra original é de
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
A contaminação por mercúrio em rios da Amazônia, decorrente do garimpo ilegal, é uma ameaça crescente à biodiversidade e à saúde das populações ribeirinhas. Uma das formas de identificar a presença desse metal em amostras ambientais é recorrer a métodos analíticos clássicos de análise sistemática de cátions, empregados historicamente em laboratórios para caracterização de íons metálicos em solução.
(Adaptado de reportagem – Agência Brasil, 2024)
Na análise sistemática de cátions, os íons metálicos são separados em grupos, de acordo com a formação de precipitados característicos, frente a reagentes específicos. O íon Hg²⁺ (mercúrio II) pertence ao primeiro grupo de cátions.
Considere uma amostra de água coletada em área de garimpo ilegal, suspeita de contaminação por mercúrio. Para caracterizar a presença de Hg²⁺, utilizando a análise sistemática, deve-se adicionar à amostra uma solução de
A contaminação por mercúrio em rios da Amazônia, decorrente do garimpo ilegal, é uma ameaça crescente à biodiversidade e à saúde das populações ribeirinhas. Uma das formas de identificar a presença desse metal em amostras ambientais é recorrer a métodos analíticos clássicos de análise sistemática de cátions, empregados historicamente em laboratórios para caracterização de íons metálicos em solução.
(Adaptado de reportagem – Agência Brasil, 2024)
Na análise sistemática de cátions, os íons metálicos são separados em grupos, de acordo com a formação de precipitados característicos, frente a reagentes específicos. O íon Hg²⁺ (mercúrio II) pertence ao primeiro grupo de cátions.
Considere uma amostra de água coletada em área de garimpo ilegal, suspeita de contaminação por mercúrio. Para caracterizar a presença de Hg²⁺, utilizando a análise sistemática, deve-se adicionar à amostra uma solução de
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
O cromo (VI), frequentemente presente em resíduos industriais, é altamente tóxico, mutagênico e carcinogênico, representando risco grave para o meio ambiente e para a saúde humana quando descartado de forma inadequada. Em contrapartida, o cromo (III) apresenta muito menor toxicidade e até funções biológicas em pequenas concentrações. Assim, processos de tratamento de efluentes buscam reduzir compostos de Cr(VI) a Cr(III), tornando-os menos nocivos antes do descarte. Um exemplo desse processo envolve a reação do dicromato de potássio (K₂Cr₂O₇) em meio ácido com ácido clorídrico, gerando sais de Cr(III), cloro gasoso e água.
(Adaptado de reportagem ambiental – Revista Pesquisa FAPESP, 2024)
A reação de redução do cromo (VI) para cromo (III), em meio ácido, pode ser representada pela seguinte equação não balanceada:
K₂Cr₂O₇ + HCl → KCl + CrCl₃ + Cl₂ + H₂O
O balanceamento dessa reação por oxirredução é fundamental para entender a proporção estequiométrica dos reagentes e produtos no tratamento de resíduos. O número total de moléculas de HCl consumidas para cada molécula de K₂Cr₂O₇ é
O cromo (VI), frequentemente presente em resíduos industriais, é altamente tóxico, mutagênico e carcinogênico, representando risco grave para o meio ambiente e para a saúde humana quando descartado de forma inadequada. Em contrapartida, o cromo (III) apresenta muito menor toxicidade e até funções biológicas em pequenas concentrações. Assim, processos de tratamento de efluentes buscam reduzir compostos de Cr(VI) a Cr(III), tornando-os menos nocivos antes do descarte. Um exemplo desse processo envolve a reação do dicromato de potássio (K₂Cr₂O₇) em meio ácido com ácido clorídrico, gerando sais de Cr(III), cloro gasoso e água.
(Adaptado de reportagem ambiental – Revista Pesquisa FAPESP, 2024)
A reação de redução do cromo (VI) para cromo (III), em meio ácido, pode ser representada pela seguinte equação não balanceada:
K₂Cr₂O₇ + HCl → KCl + CrCl₃ + Cl₂ + H₂O
O balanceamento dessa reação por oxirredução é fundamental para entender a proporção estequiométrica dos reagentes e produtos no tratamento de resíduos. O número total de moléculas de HCl consumidas para cada molécula de K₂Cr₂O₇ é
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
“O branqueamento massivo de corais que vem ocorrendo há dois anos continua a bater recordes, com quase 84% dos recifes do mundo danificados, uma enorme ameaça para esses ecossistemas vitais para a vida marinha e para centenas de milhões de pessoas. Os corais são muito vulneráveis ao aumento das temperaturas da água. E desde 2023, as temperaturas dos oceanos se mantêm em níveis sem precedentes, devido ao aquecimento global. Como consequência deste superaquecimento e da acidificação dos mares provocada pelas emissões de gases de efeito estufa da humanidade, há dois anos ocorre um episódio de branqueamento global, o quarto desde 1998, que se estende pelos oceanos Atlântico, Pacífico e Índico.”
(Folha de São Paulo, 23/04/2025)
A acidificação dos oceanos, mencionada no texto, ocorre porque parte do dióxido de carbono (CO₂) atmosférico se dissolve na água, formando ácido carbônico (H₂CO₃). Esse ácido, ao se dissociar, libera íons H⁺ que reagem com o carbonato de cálcio (CaCO₃) presente nos esqueletos dos corais, como mostrado nas equações a seguir.
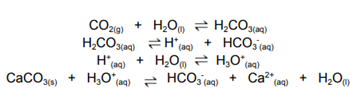
Esse processo químico afeta diretamente a sobrevivência dos corais porque
“O branqueamento massivo de corais que vem ocorrendo há dois anos continua a bater recordes, com quase 84% dos recifes do mundo danificados, uma enorme ameaça para esses ecossistemas vitais para a vida marinha e para centenas de milhões de pessoas. Os corais são muito vulneráveis ao aumento das temperaturas da água. E desde 2023, as temperaturas dos oceanos se mantêm em níveis sem precedentes, devido ao aquecimento global. Como consequência deste superaquecimento e da acidificação dos mares provocada pelas emissões de gases de efeito estufa da humanidade, há dois anos ocorre um episódio de branqueamento global, o quarto desde 1998, que se estende pelos oceanos Atlântico, Pacífico e Índico.”
(Folha de São Paulo, 23/04/2025)
A acidificação dos oceanos, mencionada no texto, ocorre porque parte do dióxido de carbono (CO₂) atmosférico se dissolve na água, formando ácido carbônico (H₂CO₃). Esse ácido, ao se dissociar, libera íons H⁺ que reagem com o carbonato de cálcio (CaCO₃) presente nos esqueletos dos corais, como mostrado nas equações a seguir.
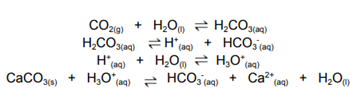
Esse processo químico afeta diretamente a sobrevivência dos corais porque
Provas
Questão presente nas seguintes provas
Um estudante de um curso técnico em química, numa aula de química analítica, foi instado por seu professor a
preparar uma solução de um padrão primário, para realização de uma atividade prática de análise volumétrica.
Ao pesquisar na internet, em sítios não confiáveis, o estudante encontrou um conjunto de supostas
características associadas às substâncias que poderiam ser utilizadas como padrão primário. Ao apresentar o
resultado de sua pesquisa ao seu professor, este sugeriu que o estudante refizesse a pesquisa, pois entre as
características apresentadas pelo estudante, não se enquadra nas de um padrão primário,
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container