Foram encontradas 36.167 questões.
O elemento fósforo (Z = 15) recebeu esse nome, que significa “trazer luz”, porque entra em combustão
espontaneamente ao ar, emitindo brilho. O fósforo foi isolado pela primeira vez por H. Brandt, em 1669, a partir de
urina. Por muito tempo, seu descobridor manteve esse feito em segredo, pensando que havia descoberto a Pedra
Filosofal. O alótropo mais reativo é o fósforo branco. Normalmente, esse sólido é recoberto com uma camada de óxido,
produto da reação de fósforo com oxigênio molecular.
Qual é o produto da reação desse alótropo com oxigênio?
Qual é o produto da reação desse alótropo com oxigênio?
Provas
Questão presente nas seguintes provas
Um pesquisador está em busca de uma técnica que o auxilie na caracterização da estrutura eletrônica e da composição
orbitalar de uma série de compostos orgânicos derivados de poliinas e cumulenas.
Qual a técnica de caracterização que fornece os dados necessários para esse pesquisador?
Qual a técnica de caracterização que fornece os dados necessários para esse pesquisador?
Provas
Questão presente nas seguintes provas
Ao se deparar com um frasco de reagente que foi utilizado em um experimento de laboratório, o técnico analisa as
informações contidas no rótulo, em busca de conhecimento quanto a manipulação, armazenamento e descarte desse
produto químico. Os pictogramas constantes no rótulo do frasco são os seguintes:

Com base nas informações fornecidas pelos pictogramas, o técnico concluiu que são indispensáveis:

Com base nas informações fornecidas pelos pictogramas, o técnico concluiu que são indispensáveis:
Provas
Questão presente nas seguintes provas
Em um processo de purificação em pequena escala do alumínio a partir do minério bauxita, procedeu-se da seguinte
maneira:
1. Ao minério, foi adicionada solução concentrada de soda cáustica, e essa mistura foi mantida em aquecimento por 3 horas, a fim de produzir Al(OH)4–(aq). Ao término, a mistura foi separada (SEPARAÇÃO I).
2. À fração contendo alumínio, foi adicionado H2SO4, de modo a formar Al(OH)3(s). A mistura resultante foi separada (SEPARAÇÃO II).
3. À fração contendo alumínio, foi adicionado KOH concentrado. A mistura foi aquecida até total dissolução e, por fim, foi adicionado H2SO4 até pH 2, e a solução foi resfriada. O produto final KAl(SO4)2(s) foi isolado (SEPARAÇÃO III).
De acordo com o procedimento, os métodos apropriados para as separações I, II e III são, respectivamente:
1. Ao minério, foi adicionada solução concentrada de soda cáustica, e essa mistura foi mantida em aquecimento por 3 horas, a fim de produzir Al(OH)4–(aq). Ao término, a mistura foi separada (SEPARAÇÃO I).
2. À fração contendo alumínio, foi adicionado H2SO4, de modo a formar Al(OH)3(s). A mistura resultante foi separada (SEPARAÇÃO II).
3. À fração contendo alumínio, foi adicionado KOH concentrado. A mistura foi aquecida até total dissolução e, por fim, foi adicionado H2SO4 até pH 2, e a solução foi resfriada. O produto final KAl(SO4)2(s) foi isolado (SEPARAÇÃO III).
De acordo com o procedimento, os métodos apropriados para as separações I, II e III são, respectivamente:
Provas
Questão presente nas seguintes provas
O diagrama (ou diamante) de Hommel, também conhecido pelo código NFPA 704, apesar de não ser obrigatório, é
bastante empregado para identificação de riscos de substâncias. Ele é constituído de quatro regiões indicadas pelas
cores vermelho, azul, amarelo e branco, como mostra a figura. Este diagrama estava no rótulo de um frasco de um
reagente, no qual não estava legível o nome da substância.
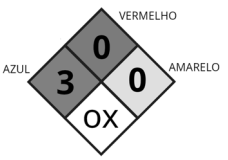
O diagrama da figura informa que essa substância:

O diagrama da figura informa que essa substância:
Provas
Questão presente nas seguintes provas
Lobelina, estrutura química mostrada a seguir, é um alcaloide extraído de uma variedade de plantas, especialmente do
gênero Lobelia. Tribos de povos originários das Américas fumavam suas folhas secas com intuito de aliviar problemas
respiratórios. Atualmente, tem sido comercializado para auxiliar pessoas a parar de fumar e também para combater
outras dependências, como de anfetaminas, cocaína ou álcool. No entanto, são limitadas as evidências clínicas de
qualquer eficácia.
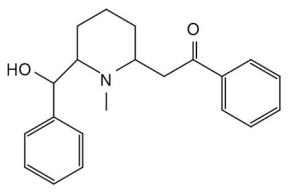
Na estrutura desse alcaloide, estão presentes as funções orgânicas:

Na estrutura desse alcaloide, estão presentes as funções orgânicas:
Provas
Questão presente nas seguintes provas
O tampão fosfato de sódio é amplamente utilizado na homogeneização de órgãos e tecidos animais para ensaios
enzimáticos. Durante seu treinamento em um laboratório, um estagiário recebeu a tarefa de preparar uma solução tampão
a 50 mM, pH 7,4. Ele seguiu os seguintes procedimentos:
1. Pesou 12 g de NaH2PO4, adicionou 100 mL de água, misturou e rotulou como “Solução de NaH2PO4 1 M”.
2. Pesou 142 g de Na2HPO4, dissolveu em 80 mL de água e completou para 100 mL, rotulando como “Solução de Na2HPO4 1 M”.
No dia seguinte, ao retornar ao laboratório, percebeu que as soluções que havia preparado tinham sido utilizadas. Com autorização, utilizou soluções estoque de NaH2PO4 e Na2HPO4 preparadas a 1 M, disponibilizadas por um técnico experiente do laboratório. Ele prosseguiu da seguinte forma:
3. Misturou 100 mL da solução de NaH2PO4 com 60 mL da solução de Na2HPO4, rotulando como “Tampão fosfato de sódio 1 M, pH 7,4”.
4. Diluiu 5 mL do tampão preparado em “3” com 100 mL de água, rotulando como “Tampão fosfato de sódio 50 mM, pH 7,4”.
Para todos os procedimentos, o estagiário considerou as seguintes informações presentes no livro de protocolos do laboratório:
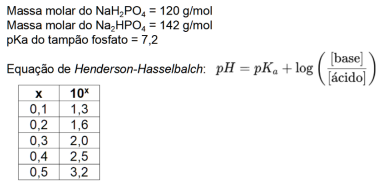
Durante esses dois dias, quantos procedimentos exatamente foram realizados de forma incorreta?
1. Pesou 12 g de NaH2PO4, adicionou 100 mL de água, misturou e rotulou como “Solução de NaH2PO4 1 M”.
2. Pesou 142 g de Na2HPO4, dissolveu em 80 mL de água e completou para 100 mL, rotulando como “Solução de Na2HPO4 1 M”.
No dia seguinte, ao retornar ao laboratório, percebeu que as soluções que havia preparado tinham sido utilizadas. Com autorização, utilizou soluções estoque de NaH2PO4 e Na2HPO4 preparadas a 1 M, disponibilizadas por um técnico experiente do laboratório. Ele prosseguiu da seguinte forma:
3. Misturou 100 mL da solução de NaH2PO4 com 60 mL da solução de Na2HPO4, rotulando como “Tampão fosfato de sódio 1 M, pH 7,4”.
4. Diluiu 5 mL do tampão preparado em “3” com 100 mL de água, rotulando como “Tampão fosfato de sódio 50 mM, pH 7,4”.
Para todos os procedimentos, o estagiário considerou as seguintes informações presentes no livro de protocolos do laboratório:
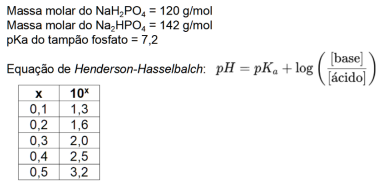
Durante esses dois dias, quantos procedimentos exatamente foram realizados de forma incorreta?
Provas
Questão presente nas seguintes provas
Uma pessoa foi incumbida de preparar 100 mL de uma solução aquosa de peróxido de hidrogênio (H2O2) a 10 mM, que
será utilizada como controle positivo em um ensaio de morte celular. Ao consultar o rótulo do frasco do reagente estoque,
ela verificou as seguintes informações:
Fórmula química: H2O2
Massa molar: 34 g/mol
Concentração: 31% (m/m) (w/w)
Densidade: 1,1 g/cm³
Forma física: líquido
Armazenamento: 2 a 8 ºC
Tipo de reagente: oxidante
Uso em ensaios com células: aprovado
Considere: 1000 cm³ = 1 L; m/m = massa/massa (do inglês w/w = weight/weight)
Com base nas informações fornecidas, qual volume da solução estoque de peróxido de hidrogênio deve ser utilizado?
Fórmula química: H2O2
Massa molar: 34 g/mol
Concentração: 31% (m/m) (w/w)
Densidade: 1,1 g/cm³
Forma física: líquido
Armazenamento: 2 a 8 ºC
Tipo de reagente: oxidante
Uso em ensaios com células: aprovado
Considere: 1000 cm³ = 1 L; m/m = massa/massa (do inglês w/w = weight/weight)
Com base nas informações fornecidas, qual volume da solução estoque de peróxido de hidrogênio deve ser utilizado?
Provas
Questão presente nas seguintes provas
Classificado como um composto halogenado, o hipoclorito de sódio (NaOCl) pode ser encontrado em uma série
de produtos, contendo concentrações e aditivos variáveis.
Assinale a alternativa correta em relação ao Líquido de Dakin.
Assinale a alternativa correta em relação ao Líquido de Dakin.
Provas
Questão presente nas seguintes provas
Considere a seguinte reação química:
H3 PO4 + Ca3 (BO3)2 → H3 BO3 + Ca3 (PO4)2
Nesse tipo de reação química, denominada de dupla troca, participam substâncias químicas que pertencem, respectivamente, às seguintes funções químicas:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container